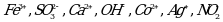План-конспект интегрированного урока физика-химия по теме: Электрический ток в растворах.
Тип урока: Изучения нового материала.
Цели урока
Личностные (Воспитательная) : создание условий для овладения навыками самоконтроля и умения управлять своей познавательной деятельностью, необходимостью в познании наук химии и физики в целом и отведение им одного из первых мест в практической, технологической и бытовой деятельности.
Метапредметные ( Развивающая).: создать условия для овладения культурой речи, навыков диалога и полилога; создание условий для совершенствования навыков анализа и синтеза, поиска способов решения проблем, осуществления межпредметного переноса.
Предметные(обучающая):создать условия для овладения понятиями: электролит, неэлектролит, электролитическая диссоциация, анион, катион, познакомить с причинами электрического тока в растворах
Оборудование урока: прибор для электролиза, растворы электролитов, лампа, ключ, выпрямитель, электроды.
1).Организационный
2).Подготовка к работе на основном этапе
Учитель физики: В физике исследуются самые общие закономерности материального мира, и эти закономерности могут применяться в любой науке о природе. Физические законы используют и в химии, и в астрономии, и в биологии, и в геодезии, и в географии и во многих других науках.
Такие науки как физика и химия очень тесно связаны. Про некоторые разделы этих наук даже трудно сказать к чему они относятся к физике или химии. На стыке этих наук находится физическая химия. В этом году на уроках физики вы изучали темы «Электричество. Электрический ток».
Учитель химии.
Но с электрическими явлениями мы будем сталкиваться и на уроках химии.
Учитель физики:
Ребята на прошлых уроках мы с вами говорили об электрическом токе в металлах.
-Почему металлы являются хорошими проводниками?
3).Усвоения новых знаний и умений (основной этап)
Учитель физики:
Вспомните из своей повседневной жизни, какие еще вещества проводят электрический ток? (почему на коробках с нагревательными приборами, а девочки наверное видели надписи на коробках с феном пишут- не пользоваться в воде? наводящий вопрос)
Учитель химии:
А что будет, если мы опустим электроды в раствор хлорида натрия?
Учитель физики. Показать опыт электропроводность раствора хлорида натрия.
Учитель химии:
- Почему загорелась лампочка?
Учитель физики:
Об этом и других подобных явлениях мы сегодня будем говорить на уроке.
-Итак как можно сформулировать тему сегодняшнего урока ?
Электрический ток в растворах.
Работа в группах. Опыты.
Изучение электрических свойств жидкости
Разделить класс на 4 группы и проделать следующие опыты.
1 группа.
Цель работы: убедиться в том, что дистиллированная вода является диэлектриком; убедиться в электропроводности растворов солей, кислот и оснований в воде.
Оборудование: вода дистиллированная; металлические электроды - 2 шт.; провода соединительные; источник тока; низковольтная лампочка на подставке; ключ; соляная кислота HCl.
Ход работы
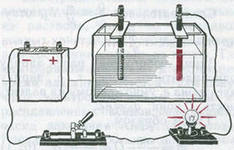
1. Соберите установку, изображённую на рисунке, налив в кювету дистиллированную воду.
2. Замкните цепь и пронаблюдайте за свечением лампочки.
3. Добавьте в воду соляной кислоты HCl и вновь пронаблюдайте за свечением лампочки.
4. Сделайте вывод.
2 группа.
Цель работы: убедиться в том, что дистиллированная вода является диэлектриком; убедиться в электропроводности растворов солей, кислот и оснований в воде.
Оборудование: вода дистиллированная; металлические электроды - 2 шт.; провода соединительные; источник тока; низковольтная лампочка на подставке; ключ; гидроксид натрия NaOH.
Ход работы

1. Соберите установку, изображённую на рисунке, налив в кювету дистиллированную воду.
2. Замкните цепь и пронаблюдайте за свечением лампочки.
3. Добавьте в воду гидроксид натрия NaOH и вновь пронаблюдайте за свечением лампочки.
4. Сделайте вывод.
3 группа.
Цель работы: убедиться в том, что дистиллированная вода является диэлектриком; убедиться в том, что при растворении глюкозы в воде она все-равно осталось не проводящим веществом.
Оборудование: вода дистиллированная; металлические электроды - 2 шт.; провода соединительные; источник тока; низковольтная лампочка на подставке; ключ; глюкоза C6H12O6.
Ход работы

1. Соберите установку, изображённую на рисунке, налив в кювету дистиллированную воду.
2. Замкните цепь и пронаблюдайте за свечением лампочки.
3. Добавьте в воду глюкозу C6H12O6 и вновь пронаблюдайте за свечением лампочки.
4. Сделайте вывод.
4 группа.
Цель работы: убедиться в том, что спирт является диэлектриком, даже после того, когда в нем растворили хлорид натрия NaCl.
Оборудование: спирт; металлические электроды - 2 шт.; провода соединительные; источник тока; низковольтная лампочка на подставке; ключ; соль поваренная NaCl.
Ход работы

1. Соберите установку, изображённую на рисунке, налив в кювету спирт.
2. Замкните цепь и пронаблюдайте за свечением лампочки.
3. Добавьте в воду хлорид натрия NaCl и вновь пронаблюдайте за свечением лампочки.
4. Сделайте вывод.
Учащиеся делают опыты. И рассказывают об увиденном.
Вывод из проведенных опытов
Учитель физики.
На практике вы увидели, что растворы одних веществ, проводят электрический ток, а другие растворы не проводят.
В металлах переносчиками электрических зарядов являются свободные электроны (проводниках первого рода). Сегодня мы делали опыты и наблюдали электропроводность водных растворов хлорида натрия, соляной кислоты, гидроксида натрия. В растворах этих веществ переносчиками электрических зарядов являются свободные ионы( проводники второго рода) В проводниках электричества заряженные частицы (электроны, ионы) могут свободно перемещаться .Поэтому их называют свободными зарядами. Под действием электрического поля свободные заряды приходят в направленное движение, т.е. создают электрический ток. В непроводниках электричества заряды или не могут перемещаться по веществу или противоположно заряженные частицы объединяются в нейтральные частицы.
Учитель химии.
-Все ли растворы проводили электрический ток?
-В каком случае сила тока была выше?(в разбавленном или там где больше растворенного вещества?)
-Как вы думаете, откуда появились свободные ионы –переносчики электрических зарядов?
(Образование свободных ионов в растворах произошло под действием молекул воды, молекулы спирта (мы это видели) не расщепляют вещества на ионы .)
-А если бы мы взяли очень концентрированный раствор, то на ваш взгляд что бы вы смогли сказать о силе тока в нем? Почему?
Учитель химии.
Вещества, растворы и расплавы которых проводят электрический ток, называются электролитами и там переносчиками электрических зарядов являются свободные ионы. Вещества, растворы и расплавы которых не проводят электрический ток, называются неэлектролитами.
Электролитическая диссоциация – процесс распада электролита на анионы и катионы при растворении его в воде или расплавлении.
Так выглядит с точки зрения химии процесс распада на ионы веществ из наших опытов.
KOH  K+ + OH-
K+ + OH-
NaCl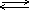 Na+ + Cl-
Na+ + Cl-
HCl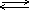 H+ + Cl-
H+ + Cl-
Параллельно с диссоциацией идет процесс соединения ионов(ассоциация).
Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставится знак обратимости.
Диссоциация оснований:
Ba(OH)2 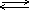 Ba2++ 2OH-
Ba2++ 2OH-
Основания диссоциируют на положительно заряженные ионы металла и отрицательно заряженные гидроксид-ионы.
Диссоциация солей:
Na3PO4  3Na+ + PO3-4
3Na+ + PO3-4
BaCl2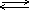 Ba2+ + 2Cl-
Ba2+ + 2Cl-
K2CO3 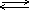 2K+ + CO32-
2K+ + CO32-
Соли диссоциируют на положительно заряженные ионы металлов и отрицательно заряженные ионы кислотного остатка
Диссоциация кислот:
Н3РО4  3Н+ + РО43 -
3Н+ + РО43 -
H2SO4 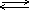 2H+ + SO42-
2H+ + SO42-
Кислоты диссоциируют на положительно заряженные ионы водорода и отрицательно заряженные ионы кислотного остатка
Учитель физики:
Под действием электрического поля ионы приобретают направленное движение: положительно заряженные ионы движутся к катоду и называются катионами, отрицательно заряженные ионы движутся к аноду и называются анионами. Так же на опыте мы увидели выделение вещества на катоде- этот процесс называется электролиз. Применение: получение алюминия и меди; очистка металлов от примесей; получение водорода.
4).Первичной проверки понимания изученного
Учитель физики:
-Какие из ионов являются катионами, а какие анионами:
H+ , Li+ , NO3− , S2− , Fe3+ , HCO3− , Ba2+ , Cu2+ ,H+ , SO42− , Na+ , CO32− , S2− , Ca2+ , HCO3−
-Какие из ионов будут двигаться к АНОДУ:

-Какие из ионов будут двигаться к КАТОДУ:
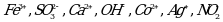
5).Подведение итогов урока.
Учитель физики: И так ребята, что мы сегодня узнали про ток.
В каких средах он протекает?
Может ли ток существовать только в металлах? А где еще?
Учитель химии:
На сегодняшнем уроке мы лишь в общих чертах коснулись химизма электролитической диссоциации. Подробнее об этом процессе мы будем говорить в 9 классе. А сегодня мы попытались вам показать, как наши 2 науки физика и химия тесно связаны друг с другом.
6).Информация о домашнем задании. В каких средах может еще существовать ток узнайте самостоятельно?
11