КОНСПЕКТ 6: КЛАССИФИКАЦИЯ ХИМ.РЕАКЦИЙ ПО Р. ОСНОВАНИЯМ.
Химические элементы, из которых состоит живая и неживая природа, находятся в непрерывном взаимодействии между собой, образуя различные по составу и свойствам вещества. Эти вещества под воздействием различных факторов постоянно видоизменяются или превращаются в другие. Именно по этому признаку все изменения, происходящие с веществами, можно условно поделить на физические изменения и химические изменения (явления).
– А как классифицируются явления? (Явления делятся на физические и химические).
В чём отличие химического явления от физического? (В результате химического явления изменяется состав вещества, а в результате физического явления состав вещества остается без изменения, а меняется лишь его агрегатное состояние или форма и размеры тел).
*Физические явленияе - это яв-я, в рез-те которых изменяются размеры, форма тел и агрегатное состояние веществ, но состав вещества остается постоянным.
Примеры: Удар молотком о гвоздь или согнуть алюмин. проволку, растворение сахара в воде. Распространение запаха духов в классе. Плавление парафиновой свечи. Таяние льда. Кипение воды в чайнике.
*Химические явл-я (хим. реакции) - явления, при к-х из одних веществ образуются другие, новые вещества, отличающиеся от исходных и по составу, и по св-вам.
Примеры: Взаимодействие мрамора с соляной кислотой. Потемнение картин. Протухание яйца. Взаимод-е соды и уксуса. Ржавление гвоздя из железа.
В отличие от физических явлений при химических явлениях, или химических реакциях, происходит превращение одних веществ в другие. Главным итогом хим. реакции является обр-е новых веществ, а у новых веществ, будут и новые свойства.
Поэтому, химические реакции часто сопровождаются внешними признаками.
Какие признаки химических реакций вы знаете?
Изменение окраски (цвета)
Появление запаха
Образование осадка
Выделение газа
Выделение или поглощение тепла,
Выделение света.
Образование воды
Условия возникновения и протекания химических реакций:
Соприкосновение (измельчение, перемешивание, растворение)
Нагревание
Действие электрического тока, света.
Что может помочь нам в изучении многообразия химических реакций? (Классификация химических реакций) Что такое классификация? (Деление на группы)
В окруж.мире протекают миллионы р-ций. Все хим.р-ции классиф-ся по определенным признакам:
| Признак | Виды |
По пр-ку поглощения или выделения теплоты (тепловому эффекту): | - ЭКЗОтермические (+Q) с выделение теплоты в том числе р-ции горения (выделение теплоты и света) - ЭНДОтермические (-Q) с поглощением теплоты |
По числу и составу исходных веществ и продуктов р-ции | - Р-ции РАЗЛОЖЕНИЯ -Р-ции СОЕДИНЕНИЯ -Р-ции ЗАМЕЩЕНИЯ - Р-ции ОБМЕНА |
По использованию катализатора | -каталитические (в том числе ферментативные) – реакции, которые идут с участием катализатора *Катализатор – вещество, к-е изменяет скорость Х.Р., ускоряя её, но в реакцию не вступающий. - НЕкаталитические – без участия катализатора |
По направлению | -обратимые ↔ (этот знак изображаем двумя отдельными стрелками, как на уроке записывали!!!) -Необратимые → |
По наличию границы раздела между веществами | - гомогенные (в одном агрегатном состоянии) - гетерогенные (в разных агрегатных состояниях) |
По изм-ю степеней окисления элементов | - ОВР (окислительно-восстановительные р-ции) - без имз-я степеней окисления |
По тепловому эффекту
Экзотермические (+ Q) с выделением теплоты, в основном это р-ции соединения.
в том числе р-ции горения (это выделение теплоты и света одновременно)
2Mg + O2 →2MgO + Q
ИСКЛ: Разложение дихромата аммония (NH4)2Cr2O7 → Cr2O3 +4H2O +N2↑+Q
реакции щелочных металлов (Ме IАгр. и IIА гр.) с водой;
реакции, сопровождающиеся взрывом; реакции горения;
образование аммиака: N2 + 3H2 ↔2NH3;
реакции нейтрализации KOH+ H2SO4 → K2SO4 + H2O взаимод-е щёлочь+вода→
синтез метанола; алюмотермия;
в органической химии — реакции присоединения, реакции горения, окисления и др.
Эндотермические (-Q) с поглощением теплоты, в основном это р-ции разложения
свет
2HgO →2Hg + O2 – Q
эл.разряд t t
ИСКЛ: N2 + О2 →2NO – Q H2 + I2 ↔ 2 HI – Q С + СО2↔ 2 СО – Q
реакции гидролиза;
реакции, идущие только при нагревании;
реакции, протекающие только при очень высоких температурах или под действием электрического разряда.
По числу и составу исходных веществ и продуктов реакции
* РЕАКЦИИ СОЕДИНЕНИЯ – это такие реакции, в результате которых из двух или нескольких исходных веществ образуется одно сложное вещество. Все реакции соединения явл-ся экзотермическими!
Например, в реакции магния с кислородом образуется оксид магния. Эта реакция сопровождаются выделением света и тепла. Поэтому её ещё называют реакцией горения. 2Mg + O2 → 2MgO t, Fe
Реакция образования аммиака: N2+H2↔NH3↑
В реакцию соединения могут вступать и два сложных вещества с образованием одного сложного. Н-р, гашение извести. СаО + Н2О → Са(ОН)2 - гашёная известь
NH3↑+HCl↑ →NH4Cl↑ дым без огня, обр-е белого дыма
*РЕАКЦИИ РАЗЛОЖЕНИЯ – это реакции, в результате которых из одного сложного вещества образуется два или более простых, или сложных новых веществ.
Запомните, все реакции разложения протекают с поглощением тепла!
Например, реакция разложения оксида ртути (II) при t. 2HgO→2Hg + O2↑
Разложение оснований при t.: Cu(OH)2 → CuO + H2O
*РЕАКЦИИ ЗАМЕЩЕНИЯ – это реакции м/д сложным и простым веществом, в результате которых атомы простого вещества замещают один из атомов сложного вещества.
Это реакции взаимодействия металлов с кислотами и металлов с солями.
ЗАПОМНИ: Металлы при взаимодействии с кислотами всегда будут вытеснять водород! Так как Ме и Водород имеют положительные заряды! Все металлы, стоящие ДО ВОДОРОДА вытесняют водород из разбавленных кислот!
Zn + H2SO4 → ZnSO4 + H2↑(цинк стоит до водорода в ряду напряжения Ме
ЗАПОМНИ: Металлы при взаимодействии с растворами солей: каждый предыдущий металл вытесняет каждый последующий из растворов его солей. Или Ме, который стоит ЛЕВЕЕ, вытесняет Ме, стоящий правее из их солей в растворе.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓ (Медь стоит левее серебра в ряду активности Ме)
*РЕАКЦИИ ОБМЕНА - это такие реакции, в результате которых два сложных вещества обмениваются своими составными частями. Т.е. вступает в реакцию два сложных вещества и образуются в после реакции тоже два сложных вещества, в рез-те обмена своими ионами.
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓ - есть осадок
KOH+ H2SO4 → K2SO4 + H2O - образовалась вода
CuS +2HCl → CuCl2 + Н2S↑ - есть газ
ЗАПОМНИ: Условия протекания реакций до конца - Правило Бертолле: Образование воды или Образование осадка или Образование газа
По наличию катализатора
*Каталитические реакции – это реакции, протекающие с участием катализатора.
*Катализатор – это вещество, к-е изменяет скорость Х.Р., ускоряя её, но в реакцию не вступающий.
Например, реакция получения оксида серы (VI) из оксида серы (IV) является каталитической, т.к. необходимым условием её протекания является наличие катализатора оксида ванадия (V).
t,V2O5 t,Fe t, Hg2+
2SO2+O2 ↔ 2SO3 N2 + 3H2 ↔ 2NH3 2Al+6H2O → 2Al(OH)3↓ + 3H2↑
MnO2 Fe2O3 H2O
H2O2→ H2O +O2↑ CO +H2O↔CO2↑ +H2↑ 2Al + 3I2 → 2AlI3
Некаталитические – если над стрелкой не указано вещество, большинство реакций протекает без участия катализатора
По признаку обратимости (по направлению)
Обратимые реакции – протекают одновременно в двух противоположных направлениях. В этих реакциях вместо знака равенства ставится знак обратимости.
N2 + 3H2 ↔ 2NH3↑ образование и разложение аммиака
СО2 + Н2О ↔ Н2СО3 образование и разложение угольной кислоты
SO2 + H2O ↔ H2SO3 образование и разложение сернистой кислоты
NH3 + H2O ↔ NH4OH образование и разложение гидрата аммиака
свет
H2 +Cl2 ↔ 2 HCl↑ при участии света
t t t
H2 +Br2 ↔ 2 HBr↑ H2 +I 2 ↔ 2 HI↑ H2 + O2 ↔ H2O
Необратимые реакции – протекают только в одном направлении, т.е идут до конца, т.к. в рез-те этих реакций образуется газ, осадок, вода, слабый электролит (малодиссициируемого вещ-ва)
Например, в реакции соляной кислоты и карбоната калия образуется углекислый газ и вода, т.е. реакция прошла до конца.
H2 +F2 → 2HF↑ 2HCl + K2CO3 → 2KCl + CO2↑ + H2O
По агрегатному состоянию веществ
Гетерогенные реакции – протекают в неоднородной среде, на поверхности раздела фаз ,т.е. в разных фазах (т-г, т-ж, ж-г, т-т).
Гетеро, означает разный, поэтому в этих реакциях вещества находятся в разных агрегатных состояниях.
это реакции, в которых реагирующие вещества и продукты находятся в разных фазах. При этом столкновение реагирующих частиц происходит только на границе соприкосновения фаз. К таким реакциям относятся взаимодействия газ-жидкость, газ-твердая фаза, твердая-твердая, и твердая фаза — жидкость.
t
S(тв.) + O2(г.) → SO2(г) CO2(г) + Ca(OH)2(р-р) → CaCO3↓(тв) + H2O
это такие реакции, в которых реагирующие вещества и продукты находятся в одной фазе, и столкновение реагирующих частиц происходит во всем объеме реакционной смеси. К гомогенным реакциям относят взаимодействия жидкость-жидкость и газ-газ.
Гомо, означает одинаковый, поэтому в гомогенных реакциях вещества находятся в одинаковом агрегатном состоянии.
HCl(р-р) + NaOH(р-р) →NaCl(р-р) + H2O
Получение синтез-газа происходит при очень высоких температурах, при которых вода — пар: паровая конверсия метана — гомогенная реакция.
CH4(г) + H2O(г) →CO(г) + 3H2(г)
ПОДСКАЗКА: Вещества с ионной, атомной или металлической кристаллической решеткой, как правило твердые при обычных условиях; вещества с молекулярной решеткой, как правило, жидкости или газы при обычных условиях.
По изменению степеней окисления химических элементов
Окислительно-восстановительные - реакции, протекающие с изменением ст.ок
Zn + H2SO4 → ZnSO4 + H2↑
Zn0 - 2ē → Zn+2 1 в-ль, окисление С.О. повысилась, значит -ē
H2 +1 + 1ē → H2 0 2 ок-ль, в-ие С.О. понизилась, значит +ē
Cu(OH)2 →CuO+H2O
Разбор примера: 8 класс
«Характеристика химической реакции по разным признакам»
CuSO4(р-р) + Fe(тв.) → FeSO4(р-р) + Cu↓
Охарактеризуем эту реакцию по всем признакам.
реакция экзотермическая, т.к. протекает с выделением незначительного количества теплоты, ведь в опыте не требуется нагревание.
реакция замещения, потому что из исходного сложного вещества (сульфата меди (II)) и исходного простого (железа) образуется новое сложное (сульфат железа (II)) и новое простое вещество (медь).
Реакция является некаталитической, т.к. катализатор не участвует в этой реакции.
реакция необратимая. Она протекает только в одном направлении (между левой и правой частью уравнения стоит знак →).
реакция гетерогенная. Она протекает между твёрдым веществом и раствором.
реакция окислительно-восстановительная, потому что медь и железо изменили свои степени окисления: медь с +2 до 0, железо с 0 до +2, медь является окислителем, а железо восстановителем.
 ДОМАШНЕЕ ЗАДАНИЕ:
ДОМАШНЕЕ ЗАДАНИЕ:
Задание 1. Определите типы химических реакций по всем признакам (по 5 признакам из таблицы!) Расставьте степени окисления и коэффициенты.
Na + Cl₂ →
Н2СО3 →
N2 + H2 →
Ca(OH)₂+Na₃PO₄→
Al + Cl₂ →
Fe(ОH)₃↓→ (над стрелкой укажите знак t)
SO3 + H2O→
Al+H2O→
Fe(ОH)₃↓+H₂SО₄→
K₂О+H₂О→
H2 + I2 →
AlBr₃+Cl₂→AlCl₃+Br₂
FeCl₂ + Cl₂ → FeCl₃
Са(ОН)2 +Н3РО4→
Mg + H2SO4→
SO2+O2 →
Задание 2. Определите типы химических реакций по всем признакам. Расставьте степени окисления и коэффициенты. Если реакция является ОВР – уравняйте методом электронного баланса.
Ca+O2→
Al2O3 + H2SO4 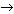
Н2SО3 →
Li+S→
Mg+HCl→
Cu(NO3) 2 → CuO + NO2 + O2
AgBr расплав→
С + СО2→2 СО
MgCO3 расплав →
K+H₂О → KOH +H2
Na2SO4+BaCl2→
CaO+H2O→
Fe(OH)3+HCl→
P₂О₃+H₂O→H₃PО₃
Mn₂О₇→MnО₂+О₂
AgNO3 + MgCl2 →
NO₂→NO+O₂
Fe+HCl→
N2 + О2 →
CaCO3 расплав →
Fe(OH)2 + O2 +Н2О → Fe(OH)3
10








 Zn0 - 2ē → Zn+2 1 в-ль, окисление С.О. повысилась, значит -ē
Zn0 - 2ē → Zn+2 1 в-ль, окисление С.О. повысилась, значит -ē ДОМАШНЕЕ ЗАДАНИЕ:
ДОМАШНЕЕ ЗАДАНИЕ:
















