
Лекция 4

- Автопротолиз воды.
- Понятие рН растворов.
- Индикаторы.
- Гидролиз солей. Типы гидролиза.

Вода типичный амфолит:
H 2 O H + + OH -
Автопротолиз – реакции, в которых одна и та же молекула растворителя может вести себя как и кислота, и как основание.
Константа диссоциации воды равна:
![K В = [H + ]·[OH - ] = 1·10 -14 при 25 ° С Произведение равновесных концентраций ионов водорода и гидроксид-ионов в воде и разбавленных водных растворах (при постоянной температуре) есть величина постоянная – ионное произведение воды (K В ) .](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img3.jpg)
K В = [H + ]·[OH - ] = 1·10 -14 при 25 ° С
Произведение равновесных концентраций ионов водорода и гидроксид-ионов в воде и разбавленных водных растворах (при постоянной температуре) есть величина постоянная –
ионное произведение воды (K В ) .

- При увеличении температуры K В значительно возрастает:
t, ° С
0
K В ·10 - 14
0,1139
18
25
0,5702
1,0008
30
50
1,469
60
5,474
9,614
 [OH - ], т.е. [ H + ] 1·10 -7 моль/л В щелочных растворах: [OH - ] [H + ], [H + ] " width="640"
[OH - ], т.е. [ H + ] 1·10 -7 моль/л В щелочных растворах: [OH - ] [H + ], [H + ] " width="640"
K В = [H + ]·[OH - ] = 10 -14 при 25 ° С
[H + ] = [OH - ] = 10 -7 моль/л
[H + ] [OH - ], т.е. [ H + ] 1·10 -7 моль/л
[OH - ] [H + ], [H + ]
![Для удобства вместо значений [H + ] используют водородный показатель pH . Водор o дный показатель есть отрицательный десятичный логарифм числового значения молярной концентрации ионов водорода : pH = -lg[H + ]](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img6.jpg)
- Для удобства вместо значений [H + ] используют водородный показатель pH .
- Водор o дный показатель есть отрицательный десятичный логарифм числового значения молярной концентрации ионов водорода :
pH = -lg[H + ]
![По аналогии используют гидроксильный показатель (pOH) : pOH = -lg[OH - ] Поскольку при 25 °С K В = [H + ]·[OH - ] = 1·10 -14 , то pH + pOH = -lg K В pH + pOH = -lg 1·10 -14 = 14 pH = 14 - pOH](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img7.jpg)
- По аналогии используют гидроксильный показатель (pOH) :
pOH = -lg[OH - ]
Поскольку при 25 °С K В = [H + ]·[OH - ] = 1·10 -14 , то
pH + pOH = -lg K В
pH + pOH = -lg 1·10 -14 = 14
pH = 14 - pOH
 7. " width="640"
7. " width="640"
Величина pH используется как мера кислотности, нейтральности или щёлочности водных растворов:
- в кислой среде pH
- в нейтральной среде pH = 7,
- в щелочной среде pH 7.
![Расчет равновесной концентрации [Н + ] и [ОН - ] 1.Пример , концентрация ионов Н + в 0,001М р-ре НС l равна [Н + ] = 0,001 моль/л, Концентрация ОН - в 0,01М растворе NаОН равна [ОН - ] = 0,01 моль/л. 2. Если концентрация ионов водорода в растворе равна 10 -3 г-ион/л, реакция среды кислая, величину [ОН - ] в таком растворе можно рассчитать из уравнения ионного произведения воды: [Н + ][ОН - ] = 10 -14 г-ион/л, следовательно, [ОН - ] =10 -14 /[Н + ] = 10 -14 /10 -3 =10 -11 г-ион/л. При этом рН=3, а рОН=11](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img9.jpg)
Расчет равновесной концентрации [Н + ] и [ОН - ]
1.Пример ,
концентрация ионов Н + в 0,001М р-ре НС l равна [Н + ] = 0,001 моль/л,
Концентрация ОН - в 0,01М растворе NаОН равна
[ОН - ] = 0,01 моль/л.
2. Если концентрация ионов водорода в растворе равна 10 -3 г-ион/л, реакция среды кислая, величину [ОН - ] в таком растворе можно рассчитать из уравнения ионного произведения воды:
[Н + ][ОН - ] = 10 -14 г-ион/л, следовательно,
[ОН - ] =10 -14 /[Н + ] = 10 -14 /10 -3 =10 -11 г-ион/л.
При этом рН=3, а рОН=11

Кислотно-основные индикаторы - слабые органические кислоты HInd или основания IndOH , подвергающиеся ионизации в водных растворах, причем нейтральная и ионизированная формы индикатора обладают различной окраской .

Уравнение диссоциации кислотных индикаторов:
Н Ind + Н 2 О ↔ Н 3 О + + Ind -
Донор
протона
Окраска 1 Окраска 2
Уравнение диссоциации основных индикаторов:
Ind ОН + Н + ↔ Н 2 О + Ind +
Акцептор
протона
Окраска 1 Окраска 2
 4,4 фиолетовый 5 бесцветный рН синий рН 8 бледно-малиновый 8,0 малиновый рН 9,8 " width="640"
4,4 фиолетовый 5 бесцветный рН синий рН 8 бледно-малиновый 8,0 малиновый рН 9,8 " width="640"
Интервал индикатора - область значений рН, в которой становится видимым изменение окраски индиатора.
- Обычно стараются подобрать индикатор с узким интервалом перехода (не более двух единиц pH).
Индикатор
Цвет индикатора в различных растворах
Метиловый оранжевый
кислый р-р
Лакмус
красный
рН
нейтральный р-р
Фенолфталеин
щелочной р-р
оранжевый
3,1
красный
рН
желтый
рН 4,4
фиолетовый
5
бесцветный
рН
синий
рН 8
бледно-малиновый
8,0
малиновый
рН 9,8

Широко применяются смеси индикаторов, позволяющие определить значение рН растворов в большом диапазоне концентраций (1-10; 0-12). Растворами таких смесей - «универсальных индикаторов» обычно пропитывают полоски «индикаторной бумаги».

- Наиболее точным методом определения pH является потенциометрический , основанный на измерении зависимости потенциала электрода от концентрации ионов водорода в исследуемом растворе.
рН-метры

- называют растворы, обладающие свойством достаточно стойко сохранять постоянство концентрации ионов водорода как при добавлении кислот или щелочей, так и при разведении.
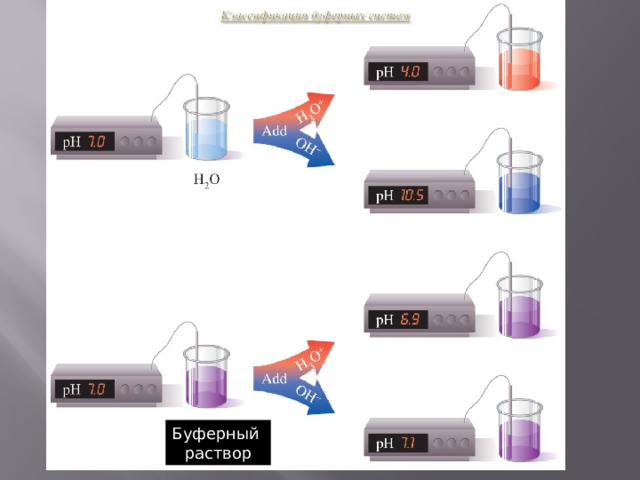
Буферный
раствор

Классификация буферных систем
Кислотные – состоят из слабой кислоты и соли этой кислоты, образованной сильным основанием.
Ацетатный буфер: СН 3 СООН СН 3 СОО Na
Гидрокарбонатный Н 2 СО 3
буфер: NaHCO 3
Основные – состоят из слабого основания и соли этого основания, образованной сильной кислотой.
Аммиачный буфер: NH 4 OH
NH 4 Cl
Солевые – состоят из гидрофосфата и дигидрофосфата Na или К.
Фосфатный буфер: NaH 2 PO 4
роль слабой к-ты Na 2 HPO 4

При растворении солей в воде происходит не только диссоциация на ионы и гидратация этих ионов, но и взаимодействие молекул воды с ионами, приводящее к разложению молекул воды на Н + и ОН – с присоединением одного из них к иону соли и освобождением другого ( гидролиз ).

Гидролиз солей – это взаимодействие солей с водой
В результате гидролиза соли в растворе появляется некоторое избыточное количество ионов Н⁺ или ОН⁻
- При этом изменяется рН раствора .

Al 3+ ; Fe 3+ ; Bi 3+ и др.
CO 3 2- ; SO 3 2– ; NO 2 – ; CN – ; S 2– и др.

- Катион сильного основания
Na + ; Ca 2+ ; K + и др.
Cl – ; SO 4 2– ; NO 3 – ; и др.

Проходит по катиону , при этом рН раствора уменьшится .
AlCl 3 + H 2 O → Al(OH)Cl 2 + HCl
Al 3+ + Н + ОН – → Al ( OH ) 2+ + H +
Cl - + H 2 O → не идет
среда кислая рН

Fe Cl 3 + H 2 O → Fe(OH)Cl 2 + HCl
Fe 3+ + Н + ОН – → Fe ( OH ) 2+ + H +
среда кислая рН
 7 " width="640"
7 " width="640"
Проходит по аниону , при этом может образоваться слабая кислота или кислая соль. рН раствора увеличится .
NaSO 3 + H 2 O → Na HSO 3 + Na ОН
SO 3 2– + Н + ОН – → HSO 3 – + ОН –
среда щелочная рН 7
 7 " width="640"
7 " width="640"
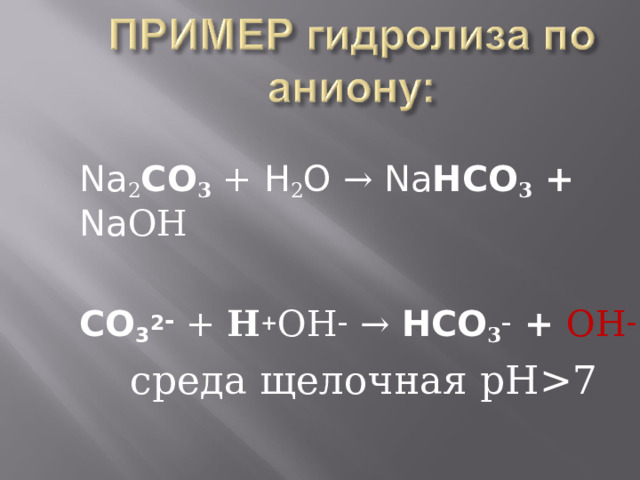
Na 2 CO 3 + H 2 O → Na HCO 3 + Na ОН
CO 3 2 - + Н + ОН – → HCO 3 – + ОН –
среда щелочная рН 7

Проходит полностью ; рН 7 :
Al 2 (SO 3 ) 3 + 6H 2 O 2Al(OH) 3 + 3H 2 SO 3
H 2 SO 3 → H 2 O + SO 2 ↑

Реакция в этом случае идет до конца, так как при гидролизе катиона образуется Н + :
Al 3+ + Н + ОН – → Al ( OH ) 2+ + H +
при гидролизе аниона ОН – :
SO 3 2– + Н + ОН – → HSO 3 – + ОН –
далее происходит образование из них Н 2 О (с выделением энергии), что и смещает равновесие гидролиза вправо .

Na 2 SO 4 + H 2 O → не идет

Протекает:
- Гидролиз соли слабого основания и сильной кислоты
- Гидролиз соли слабой кислоты и сильного основания
- Гидролиз соли слабой кислоты и слабого основания
Не протекает:
- Гидролиз соли сильного основания и сильной кислоты

- Степень гидролиза г (доля гидролизованных единиц)
- К онстант а гидролиза - К г .

- Степень гидролиза г – показатель глубины протекания гидролиза
- На степень гидролиза влияют :
- природа соли концентрация раствора (чем меньше концентрация, тем сильнее гидролиз) температура (чем выше температура, тем сильнее гидролиз) рН среды
- природа соли
- концентрация раствора (чем меньше концентрация, тем сильнее гидролиз)
- температура (чем выше температура, тем сильнее гидролиз)
- рН среды









![K В = [H + ]·[OH - ] = 1·10 -14 при 25 ° С Произведение равновесных концентраций ионов водорода и гидроксид-ионов в воде и разбавленных водных растворах (при постоянной температуре) есть величина постоянная – ионное произведение воды (K В ) .](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img3.jpg)

 [OH - ], т.е. [ H + ] 1·10 -7 моль/л В щелочных растворах: [OH - ] [H + ], [H + ] " width="640"
[OH - ], т.е. [ H + ] 1·10 -7 моль/л В щелочных растворах: [OH - ] [H + ], [H + ] " width="640"
![Для удобства вместо значений [H + ] используют водородный показатель pH . Водор o дный показатель есть отрицательный десятичный логарифм числового значения молярной концентрации ионов водорода : pH = -lg[H + ]](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img6.jpg)
![По аналогии используют гидроксильный показатель (pOH) : pOH = -lg[OH - ] Поскольку при 25 °С K В = [H + ]·[OH - ] = 1·10 -14 , то pH + pOH = -lg K В pH + pOH = -lg 1·10 -14 = 14 pH = 14 - pOH](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img7.jpg)
 7. " width="640"
7. " width="640"
![Расчет равновесной концентрации [Н + ] и [ОН - ] 1.Пример , концентрация ионов Н + в 0,001М р-ре НС l равна [Н + ] = 0,001 моль/л, Концентрация ОН - в 0,01М растворе NаОН равна [ОН - ] = 0,01 моль/л. 2. Если концентрация ионов водорода в растворе равна 10 -3 г-ион/л, реакция среды кислая, величину [ОН - ] в таком растворе можно рассчитать из уравнения ионного произведения воды: [Н + ][ОН - ] = 10 -14 г-ион/л, следовательно, [ОН - ] =10 -14 /[Н + ] = 10 -14 /10 -3 =10 -11 г-ион/л. При этом рН=3, а рОН=11](https://fsd.multiurok.ru/html/2022/07/19/s_62d64ff792dec/img9.jpg)


 4,4 фиолетовый 5 бесцветный рН синий рН 8 бледно-малиновый 8,0 малиновый рН 9,8 " width="640"
4,4 фиолетовый 5 бесцветный рН синий рН 8 бледно-малиновый 8,0 малиновый рН 9,8 " width="640"











 7 " width="640"
7 " width="640"
 7 " width="640"
7 " width="640"























