
Мыло.
Синтетические моющие средства.

Содержание:
- Что такое мыло?
- Как получают мыло?
- Омыление.
- Хозяйственное мыло.
- Туалетное мыло.
- Моющее действие мыла.
- Недостатки мыла.
- Синтетические моющие средства.
- Получение СМС.
- Состав СМС.
- ДЛЯ ЧЕГО НУЖНЫ СОСТАВНЫЕ ЧАСТИ СМС.
- Влияет ли температура на моющее действие СМС.
- Вывод:
- Используемая литература.

Что такое мыло?
Мыла – это натриевые или калиевые соли высших карбоновых кислот: пальмитиновой, стеариновой, олеиновой, лауриновой.
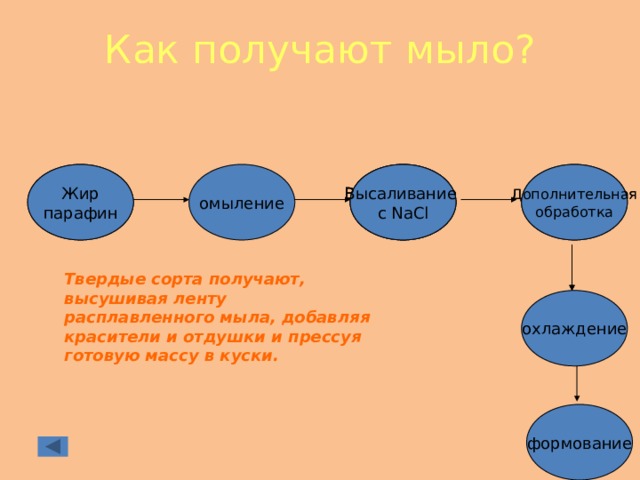
Как получают мыло?
Высаливание
Дополнительная
Жир
Дополнительная
Высаливание
Высаливание
Жир
омыление
с NaCl
с NaCl
обработка
с NaCl
парафин
обработка
парафин
Твердые сорта получают, высушивая ленту расплавленного мыла, добавляя красители и отдушки и прессуя готовую массу в куски.
охлаждение
формование

Омыление.
В результате омыления образуется ядровое мыло из которого изготавливают хозяйственное и туалетное мыло.
С 3 Н 5 (С 13 Н 35 СОО) 3 +3NaOH 3C 17 H 35 COONa+C 3 H 5 (OH) 3
2С 15 Н 31 СООН+Na 2 СО 3 2С 15 Н 31 СООNa+Н 2 О+СО 2

Хозяйственное мыло.
Твердые хозяйственные мыла в зависимости от сорта содержат 40-72% основного вещества, 0,1-0,2% свободной щелочи, 1-2% свободных карбонатов Na или К, 0,5-1,5% нерастворимого в воде остатка

Туалетное мыло.
Получают путем дополнительной обработки ядрового мыла с добавлением: красителей, антисептиков, талька, соды, каолина, душистых веществ.
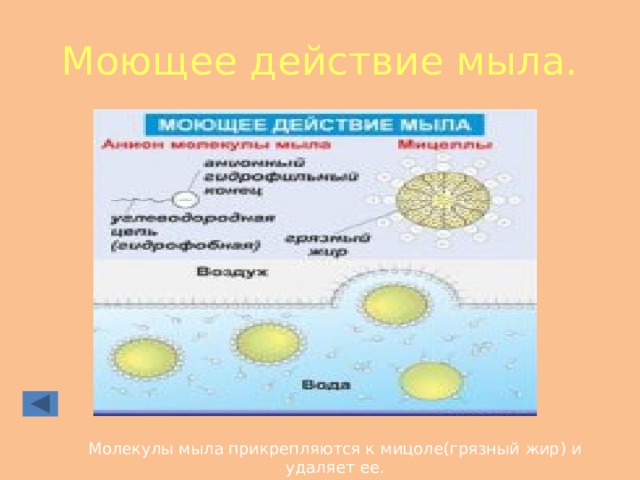
Моющее действие мыла.
Молекулы мыла прикрепляются к мицоле(грязный жир) и удаляет ее.
Недостатки мыла.
- Не отстирывает в жесткой воде.
- Мало пенится.

Синтетические моющие средства.
Синтетические моющие средства - это натриевые соли кислых сложных эфиров высших спиртов и серной кислоты.

Получение СМС.
R-CH 2 -OH + H-O-SO 2 -OH=R-CH 2 -O-SO 2 -OH + H 2 O
R-CH 2 -O-SO 2 -OH + NaOH=R-CH 2 -O-SO 2 -ONa + H 2 O
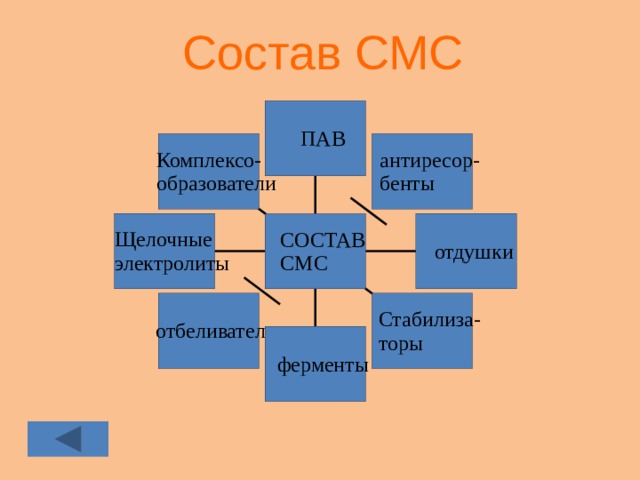
Состав СМС

ДЛЯ ЧЕГО НУЖНЫ СОСТАВНЫЕ ЧАСТИ СМС.
- Катионоактивные ПАВ-обладает, кромеиоющего, еще и дезинфицирующим действием.
Неионогенные ПАВ образуют сравнительно мало пены, и на их основе готовят средства для машинной стирки.
2. Комплексообразователи(Триполифосфат натрия)-одно из немногих хорошее растворимых в воде соединений фосфорной кислоты)
Взаимодействуя с находящимися в воде ионами кальция и магния, фосфат-ион переводит их в осадок состава Са 3 (РО 4 ) 2 и Mg 3 (РО 4 ) 2
 7),потому что в растворе увеличивается концентрация ионов ОН. Гидролиз по аниону соли гидролизуется обратимо. Химическое равновесие в таких реакциях сильно смещается влево; При гидролизе солей, образованных слабыми многоосновными кислотами, получаются кислые соли. Гидролиз зависит от температуры: при нагревании раствора усиливается гидролиз, усиливается эндотермическая диссоциация воды: Н 2 О Н + ОН - 57 кДж, значит, увеличивается количество ионов Н и ОН . Чтобы подавить гидролиз, нужно охладить раствор. " width="640"
7),потому что в растворе увеличивается концентрация ионов ОН. Гидролиз по аниону соли гидролизуется обратимо. Химическое равновесие в таких реакциях сильно смещается влево; При гидролизе солей, образованных слабыми многоосновными кислотами, получаются кислые соли. Гидролиз зависит от температуры: при нагревании раствора усиливается гидролиз, усиливается эндотермическая диссоциация воды: Н 2 О Н + ОН - 57 кДж, значит, увеличивается количество ионов Н и ОН . Чтобы подавить гидролиз, нужно охладить раствор. " width="640"
3. Щелочное отбеливание(процесс гидролиза)-это реакция обменного разложения веществ водой.
Рассмотрим подробнее гидролиз слабой кислоты-Na2CO3 –карбонат натрия.
NaОН Na 2 CO 3 Н 2 CO 3
Сильное однокислотное основание слабая двухосновная кислота
Гидролиз соли происходит по аниону CO 3 .
2Na + CO 3 + Н 2 О НCO 3 + 2Na + ОН
Продукт гидролиза - NaН CO 3 и NaОН.
Среда водного раствора Na -Na 2 CO 3 CO 3 –щелочная (рН 7),потому что в растворе увеличивается концентрация ионов ОН.
Гидролиз по аниону соли гидролизуется обратимо.
Химическое равновесие в таких реакциях сильно смещается влево;
При гидролизе солей, образованных слабыми многоосновными кислотами, получаются кислые соли.
Гидролиз зависит от температуры: при нагревании раствора усиливается гидролиз, усиливается эндотермическая диссоциация воды:
Н 2 О Н + ОН - 57 кДж, значит, увеличивается количество ионов Н и ОН .
Чтобы подавить гидролиз, нужно охладить раствор.

4.отбеливатели-для удаления цветных загрязнений, оставщихся после стирки, и отбеливания.
5.отдушки-впринципе не имеет отношение к стирке, а просто придает белью приятный запах.
6. стабилизаторы(Карбоксиметилцелюллоза (КМЦ)) выполняет роль стабилизатора пены.

Влияет ли температура на моющее действие СМС.
Сделав раствор порошка , разделить раствор на 4 части.
В первую часть раствора добавить несколько капель фенолфталеина. Он дает порошку малиновый цвет и показывает щелочную среду. При нагревании цвет раствора усиливается.
Во вторую часть добавить лакмус. Он дает раствору синий цвет и выявляет щелочную среду. При нагревание так же усиливается цвет.
В третью часть раствора порошка добавляем метил оранжевый. Он дает раствору оранжевый оттенок и выявляет щелочную среду.
В четвертую часть порошкового раствора при t=20C o опустить РН-полоску (полоска показала РН=10;это значит, что уже в холодной воде щелочная среда высокая). Далее подогреть раствор t=60C O и так же опустить РН-полоску (РН=12;это максимально высокая щелочная среда).
Отсюда , чем выше t o , тем сильнее выражена щелочность раствора. Поэтому не желательно стирать вещи из деликатных и синтетических тканей в горячей воде, так как гидролиз с повышением температуры происходит сильнее и это может привести к разрушению волокон ткани.

Вывод:
Вообще говоря, для стирки можно использовать разные средства : в каких-то случаях подойдет и мыло, и сода, и стиральный порошок (а в полном отрыве от цивилизации можно попробовать стирку с древесной золой, которая , как известно, подщелачивает воду). Главное, чтобы выбранное моющее средство более или менее успешно выполняло две функции: * удаление частиц грязи с очищаемой поверхности и * перенос их в раствор .

Используемая литература.
- www.xumuk.ru
- www.scincetechnics.ru
Юркина К. «Исследовательская работа"




















 7),потому что в растворе увеличивается концентрация ионов ОН. Гидролиз по аниону соли гидролизуется обратимо. Химическое равновесие в таких реакциях сильно смещается влево; При гидролизе солей, образованных слабыми многоосновными кислотами, получаются кислые соли. Гидролиз зависит от температуры: при нагревании раствора усиливается гидролиз, усиливается эндотермическая диссоциация воды: Н 2 О Н + ОН - 57 кДж, значит, увеличивается количество ионов Н и ОН . Чтобы подавить гидролиз, нужно охладить раствор. " width="640"
7),потому что в растворе увеличивается концентрация ионов ОН. Гидролиз по аниону соли гидролизуется обратимо. Химическое равновесие в таких реакциях сильно смещается влево; При гидролизе солей, образованных слабыми многоосновными кислотами, получаются кислые соли. Гидролиз зависит от температуры: при нагревании раствора усиливается гидролиз, усиливается эндотермическая диссоциация воды: Н 2 О Н + ОН - 57 кДж, значит, увеличивается количество ионов Н и ОН . Чтобы подавить гидролиз, нужно охладить раствор. " width="640"






















