Просмотр содержимого документа
«Презентация к уроку химии на тему "Алкены"»

Алкены
Автор: преподаватель химии ГБПОУ ВМТ Дзагоева Ф.Б.

Полиэтилен. Изделия из полиэтилена.

Применение алкенов
- В овощехранилищах для ускорения созревания плодов.
- Производство органических соединений:
- полиэтилена, полипропилена, поливинилхлорида (ПВХ);
- растворителей;
- уксусной кислоты;
- спиртов.

«Поли» - греч. « рoly » – много.
Полиэтилен получают из этилена под действием высокой температуры и давления. При этом двойные углерод - углеродные связи разрываются, и атомы углерода соединяются друг с другом:
… + СН 2 =СН 2 + СН 2 =СН 2 + СН 2 =СН 2 + … →
→ … - СН 2 – СН 2 – СН 2 – СН 2 – СН 2 - СН 2 - …
Фрагменты – СН 2 – СН 2 – образуют длинные цепи.
Упрощенно уравнение реакции можно записать так:
nСН 2 =СН 2 → (- СН 2 – СН 2 –) n
Этилен Полиэтилен
Исходное вещество (этилен) называют мономером, а продукт реакции (полиэтилен ) – полимером.
Реакции, в которых происходит соединение множества одинаковых молекул исходного вещества в огромную макромолекулу, называют реакцией полимеризации .

Химические свойства
1) Реакция гидрирования (+Н 2 ):
СН 2 =СН 2 + Н 2 → СН 3 -СН 3
этилен этан
2) Реакция бромирования (+ Br 2 - бромная вода ) – качественная реакция на двойную связь. Бромная вода обесцвечивается.
СН 2 =СН 2 + Br 2 → СН 2 Br-СН 2 Br
этилен 1,2-дибромэтан
3) Реакция гидратации:
СН 2 =СН 2 + Н 2 О → СН 3 -СН 2 -ОН
этилен этиловый спирт
![Химические свойства II. Реакции окисления: 1) Окисление этилена раствором перманганата калия KMnO 4 – качественная реакция на двойную связь. Раствор KMnO 4 обесцвечивается. СН 2 =СН 2 + [ О ] + Н 2 О → СН 2 - СН 2 этилен | | ОН ОН этиленгликоль 2) Реакция горения этилена (светящееся пламя) СН 2 =СН 2 + 3О 2 → 2СО 2 + 2Н 2 О + Q](https://fsd.multiurok.ru/html/2017/10/01/s_59d121a4df51b/img5.jpg)
Химические свойства
1) Окисление этилена раствором перманганата калия KMnO 4 – качественная реакция на двойную связь. Раствор KMnO 4 обесцвечивается.
СН 2 =СН 2 + [ О ] + Н 2 О → СН 2 - СН 2
этилен | |
ОН ОН
этиленгликоль
2) Реакция горения этилена (светящееся пламя)
СН 2 =СН 2 + 3О 2 → 2СО 2 + 2Н 2 О + Q

Получение алкенов
- В лабораторных условиях этилен получают реакцией дегидратации этилового спирта (- H 2 O):
H 2 SO 4 (конц), t
CH 3 -CH 2 -OH ―――→ CH 2 =CH 2 + H 2 O
2. Дегидрирование этилена ( - Н 2 ):
Al 2 O 3
CH 3 - CH 3 ―――→ CH 2 =CH 2 + H 2
- Деполимеризация полиэтилена:
(- СН 2 – СН 2 –) n → nСН 2 =СН 2
Полиэтилен Э тилен

Определение
Алкены – это непредельные углеводороды. В молекулах которых содержится одна двойная связь и подчиняющиеся общей формуле C n H 2n
C 2 H 4 этен (этилен)
C 3 H 6 пропен )пропилен)
C 4 H 8 бутен (бутилен)
C 5 H 10 пентен (амилен)
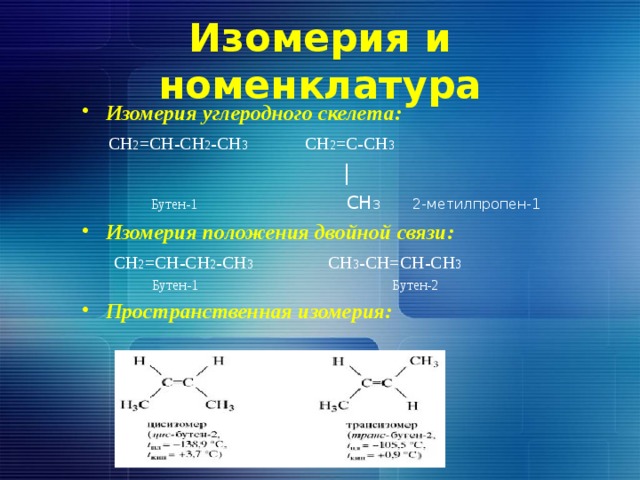
Изомерия и номенклатура
- Изомерия углеродного скелета:
CH 2 =CH-CH 2 -CH 3 СН 2 =С-СН 3
|
Бутен-1 СН 3 2-метилпропен-1
- Изомерия положения двойной связи:
CH 2 =CH-CH 2 -CH 3 CH 3 -CH=CH-CH 3
Бутен-1 Бутен-2
- Пространственная изомерия:

Задания
- Найдите общие черты и различия между этаном и этиленом.
- Напишите уравнения реакций получения пропилена из пропана и пропилового спирта СН 3 -СН 2 -СН 2 -ОН.
- 1,2-Дихлорэтан используют в качестве растворителя пластмасс. А также для обеззараживания зернохранилищ, зерна, почвы. Предложите способ получения этого вещества из этилена, напишите уравнение реакции. Сколько литров этилена (н.у.) потребуется для получения 1 кг 1,2-Дихлорэтан ?












![Химические свойства II. Реакции окисления: 1) Окисление этилена раствором перманганата калия KMnO 4 – качественная реакция на двойную связь. Раствор KMnO 4 обесцвечивается. СН 2 =СН 2 + [ О ] + Н 2 О → СН 2 - СН 2 этилен | | ОН ОН этиленгликоль 2) Реакция горения этилена (светящееся пламя) СН 2 =СН 2 + 3О 2 → 2СО 2 + 2Н 2 О + Q](https://fsd.multiurok.ru/html/2017/10/01/s_59d121a4df51b/img5.jpg)




















