Просмотр содержимого документа
«Презентация к уроку в 10 классе "Галогены. Общая характеристика галогенов"»

Галогены. Общая характеристика галогенов.

Цель урока:
- Повторить свойства металлов и неметаллов
- Изучить строениеатомов, свойства галогенов на основании их сравнительной характеристики.


Ответы теста
1 вариант – неметаллы
- 1 вариант – неметаллы
- 1 вариант – неметаллы
- 1 вариант – неметаллы
- 1 вариант – неметаллы
2, 4, 5, 7, 10, 11, 13, 15
2 вариант – металлы
1, 2, 3, 6, 8, 9, 12, 14
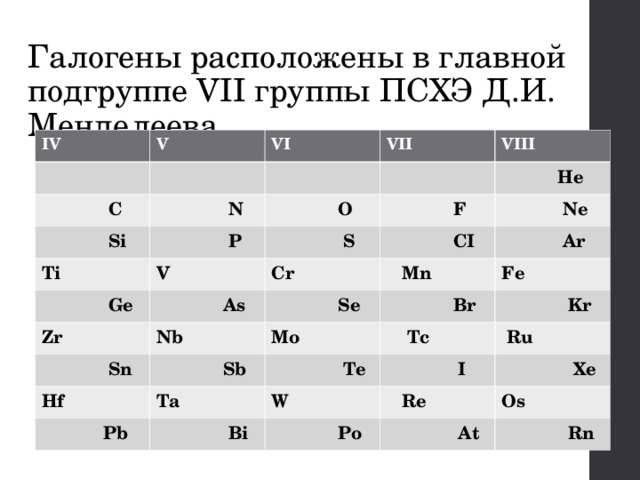
Галогены расположены в главной подгруппе VII группы ПСХЭ Д.И. Менделеева
IV
V
VI
C
VII
N
Si
P
O
VIII
Ti
F
V
He
S
Ge
Zr
As
Cr
CI
Ne
Nb
Mn
Ar
Se
Sn
Hf
Sb
Mo
Br
Fe
Tc
Ta
Te
Kr
Pb
I
Ru
W
Bi
Re
Xe
Po
Os
At
Rn
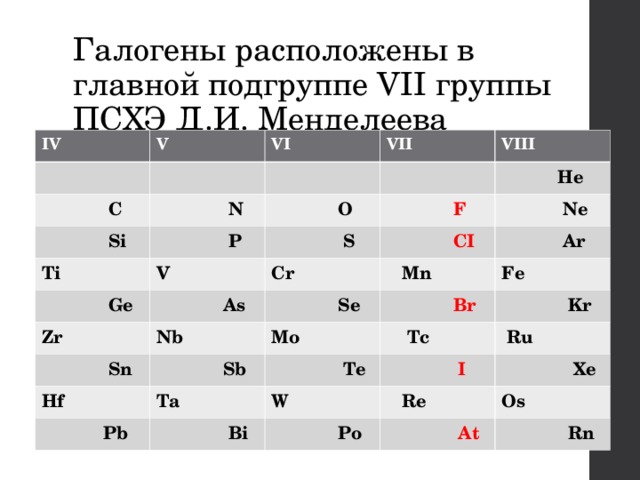
Галогены расположены в главной подгруппе VII группы ПСХЭ Д.И. Менделеева
IV
V
VI
C
VII
N
Si
P
O
VIII
Ti
F
V
He
S
Ge
Zr
As
Cr
CI
Ne
Nb
Mn
Ar
Se
Sn
Hf
Sb
Mo
Br
Fe
Tc
Ta
Te
Kr
Pb
I
Ru
W
Bi
Re
Xe
Po
Os
At
Rn
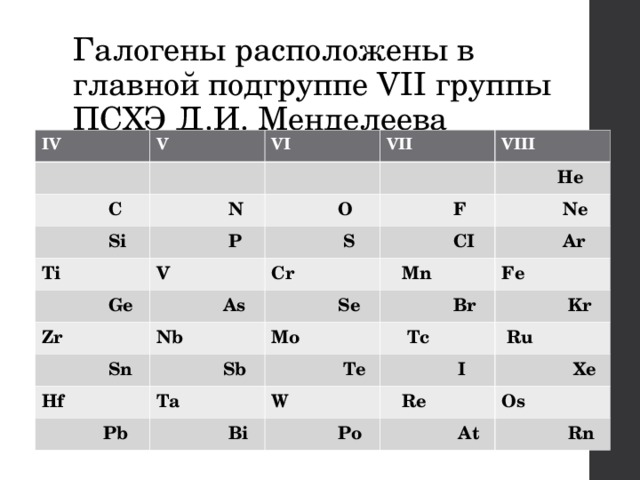
Галогены расположены в главной подгруппе VII группы ПСХЭ Д.И. Менделеева
IV
V
VI
C
VII
N
Si
P
O
VIII
Ti
F
V
He
S
Ge
Zr
As
Cr
CI
Ne
Nb
Mn
Ar
Se
Sn
Hf
Sb
Mo
Br
Fe
Tc
Ta
Te
Kr
Pb
I
Ru
W
Bi
Re
Xe
Po
Os
At
Rn
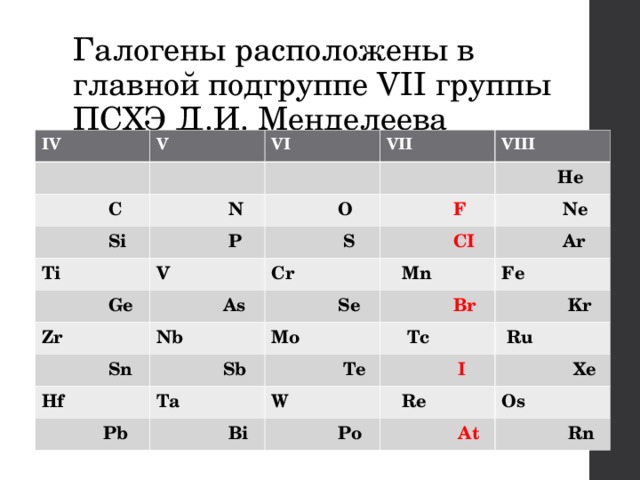
Галогены расположены в главной подгруппе VII группы ПСХЭ Д.И. Менделеева
IV
V
VI
C
VII
N
Si
P
O
VIII
Ti
F
V
He
S
Ge
Zr
As
Cr
CI
Ne
Nb
Mn
Ar
Se
Sn
Hf
Sb
Mo
Br
Fe
Tc
Ta
Te
Kr
Pb
I
Ru
W
Bi
Re
Xe
Po
Os
At
Rn
Галогены
«рождающие соли»

Распространенность галогенов в природе
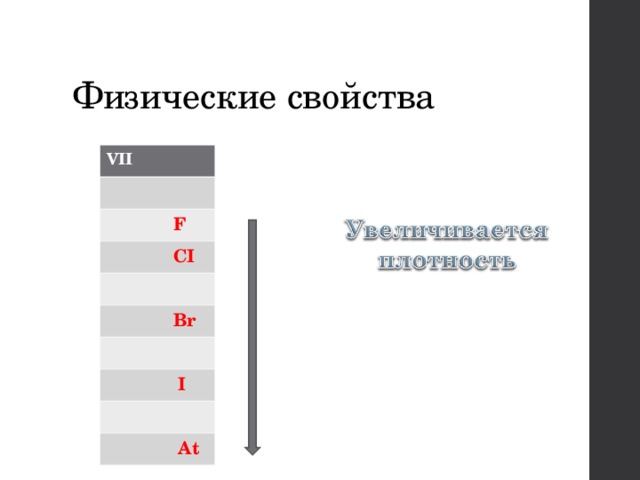
Физические свойства
VII
F
CI
Br
I
At
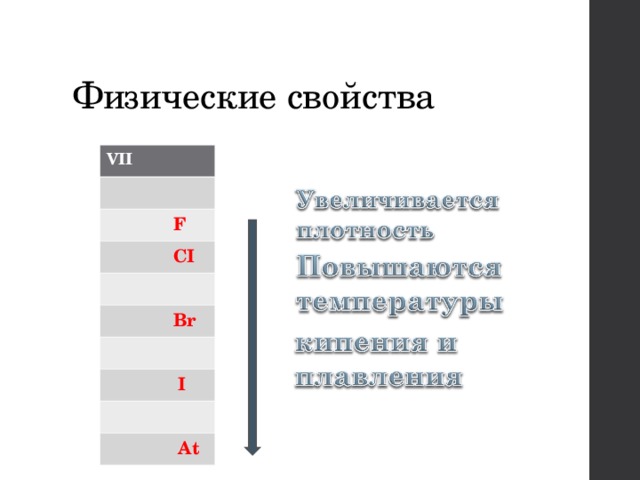
Физические свойства
VII
F
CI
Br
I
At
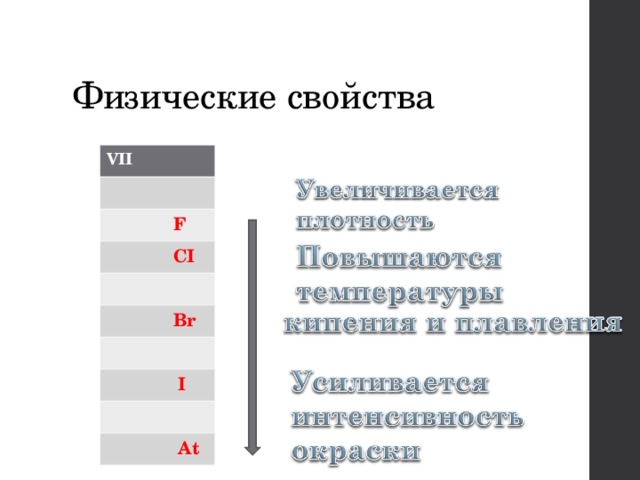
Физические свойства
VII
F
CI
Br
I
At

Фтор
газ
светло-
зелёного
цвета

Хлор
CI 2 -
Ядовитый
газ
жёлто-зеленого цвета

Бром
Токсичная
тяжёлая
жидкость
красно- бурого цвета

йод
- I 2 –
- Твёрдое кристаллическое
- вещество
- с металлическим
- блеском
- При нагревании образует пары фиолетового цвета

Ответьте на вопросы.
- Число электронов на внешнем энергетическом уровне атома;
- Изменение радиуса атомов и окислительно-восстановительных свойств галогенов в подгруппе;
- Возможные степени окисления.
- Тип химической связи
- Тип кристаллической решетки

Проверка:
- На внешнем энергетическом уровне галогены содержат 7 электронов.
- В главной подгруппе с увеличением зарядов ядер, увеличиваются радиусы атомов, нарастают восстановительные свойства.
- Возможные степени окисления: -1, +7.
- Ковалентная неполярная связь
- Молекулярная кристаллическая решетка.

Химические свойства
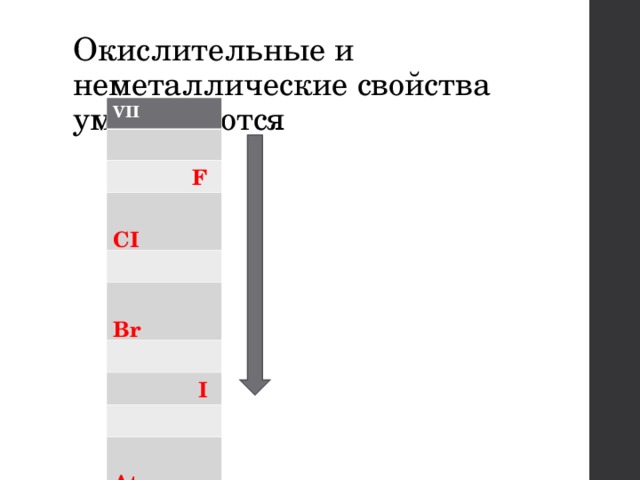
Окислительные и неметаллические свойства уменьшаются
VII
F
CI
Br
I
At

Более активный галоген вытесняет менее активный из его соединений с металлами и водородом
- 2KI + Br 2 = 2 KBr + I 2 ,
- но KBr + I 2
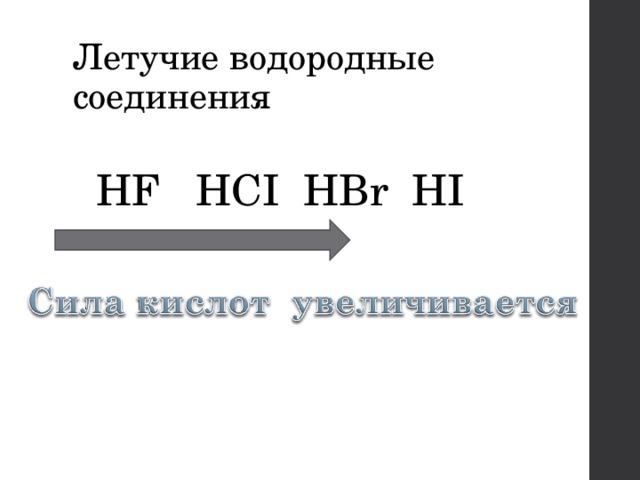
Летучие водородные соединения
HF HCI HBr HI

Л. О. №2 Вытеснение одних галогенов другими из их соединений Оформите результаты работы в виде таблицы
Что делаю?
Что наблюдаю?
Запишите уравнения реакций
Сделайте вывод . Как изменяются окислительные свойства галогенов?

Л. О. №3 Растворимость йода в органических растворителях Оформите результаты работы в виде таблицы
Что делаю ?
Что наблюдаю?
Запишите уравнения реакций.
Сделайте вывод о растворимости галогенов.

Вопросы и задания
- Перечислите галогены.
- Фтор, хлор, бром, йод, астат.
- Где в ПСХЭ располагаются галогены?
- в VII группе, главной подгруппе.
Чему равно число валентных электронов в атомах галогенов ?
- Число валентных электронов равно семи.

Вопросы и задания
- Сопоставьте :
- Хлор красно – бурая жидкость
- Бром светло – зеленый газ
- Йод жёлто – зелёный газ
- Фтор твёрдый с металлическим
блеском пары фиолетового цвета

Вопросы и задания
- Дополните:
- Самый сильный неметалл –
фтор.
Самая сильная бескислородная кислота –
HI.
Как изменяются окислительные свойства галогенов?
Уменьшаются в ряду F CI Br I




















































