
ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
Выполнила: Гуня Марина Александровна, учитель химии МБОУ Дубровская СОШ им. Н.П.Сергеенко, 2015 год

Цели урока:
- 1.Сформулировать основные положения теории электролитической диссоциации.
- 2.Закрепить понятия: ион, катион, анион, гидратированные и негидратированные ионы.
- 3.Рассмотреть примеры диссоциации солей, кислот и щелочей.

ПРОВЕРЬ СВОИ ЗНАНИЯ
- Вещества, растворы которых проводят электрический ток, называют ………
- Процесс распада электролита на ионы называют ……..
- Вещества, растворы которых не проводят электрический ток, называют ……….
- Отношение числа частиц, распавшихся на ионы, к общему числу растворенных частиц называют …………

ПРОВЕРЬ СВОИ ЗНАНИЯ
- Вещества, растворы которых проводят электрический ток, называют электролитами
- Процесс распада электролита на ионы называют электролитической диссоциацией
- Вещества, растворы которых не проводят электрический ток, называют неэлектролитами
- Отношение числа частиц, распавшихся на ионы, к общему числу растворенных частиц называют степенью диссоциации

Задание
Распределите вещества на электролиты и неэлектролиты:
NaCl (р-р), глюкоза(р-р), NaOH (р-р), HCl (р-р), спирт(р-р), сахар(р-р)

Испытание веществ на электрическую проводимость ( видеофрагмент )

С каким типом связи характерны этапы растворения веществ:
А. 1)ориентация молекул
2)гидратация молекул
3)диссоциация кристалла электролита.
Б. 1)ориентация молекул
2)гидратация молекул
3) ионизация молекул
4)диссоциация кристалла электролита.
Ответ обоснуйте.

ПРОВЕРЬ СВОИ ЗНАНИЯ (дополните схему)
ЭЛЕКТРОЛИТЫ
(по степени электролитической диссоциации )

Вопрос
Кто является основателем теории электролитической диссоциации?

История открытия теории электролитической диссоциации
В 1887 году шведский химик Сванте Аррениус сформулировал основные положения теории электролитической диссоциации

Основные положения ТЭД
- При растворении в воде электролиты диссоциируют (распадаются) на положительные и отрицательные ионы.
NaCl = Na + + Cl -
Ионы – это одна из форм существования химического элемента

ИОНЫ (по составу)
ПРОСТЫЕ
Например:
СЛОЖНЫЕ
Например:

Основные положения ТЭД
2. Причиной диссоциации электролита в водном растворе является его гидратация, т.е. взаимодействие электролита с молекулами воды и разрыв химической связи в нем.

ИОНЫ (по наличию водной оболочки)
(в растворах и кристаллогидратах)
Например:
CuSO 4 * 5H 2 O
(в безводных солях)
Например:
Cu 2+ SO 4 2-
Na + NO 3 -

Основные положения ТЭД
3 . Под действием электрического тока положительно заряженные ионы движутся к отрицательному полюсу источника тока – катоду, поэтому их называют катионами, а отрицательно заряженные ионы движутся к положительному полюсу источника тока – аноду, поэтому их называют анионами.

ИОНЫ (по знаку заряда)
положительно заряженные частицы
отрицательно заряженные частицы

Основные положения ТЭД
4. Электролитическая диссоциация – процесс обратимый для слабых электролитов.
Наряду с процессом диссоциации протекает и обратный процесс – ассоциация (соединение ионов)
HNO 2 H + + NO 2 -

Основные положения ТЭД
5 . Не все электролиты в одинаковой мере диссоциируют на ионы.

ЭЛЕКТРОЛИТЫ
(по степени диссоциации)
СЛАБЫЕ СИЛЬНЫЕ

Основные положения ТЭД
6. Химические свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.

ЭЛЕКТРОЛИТЫ (по характеру образующихся ионов)
КИСЛОТЫ ОСНОВАНИЯ
СОЛИ

КИСЛОТЫ
- электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка.
HCl = H + + Cl -
HNO 3 = H + + NO 3 -

ОСНОВАНИЯ
- электролиты, которые при диссоциации образуют катионы металла и гидроксид- анионы .
NaOH = Na + + OH -
KOH = K + + OH -
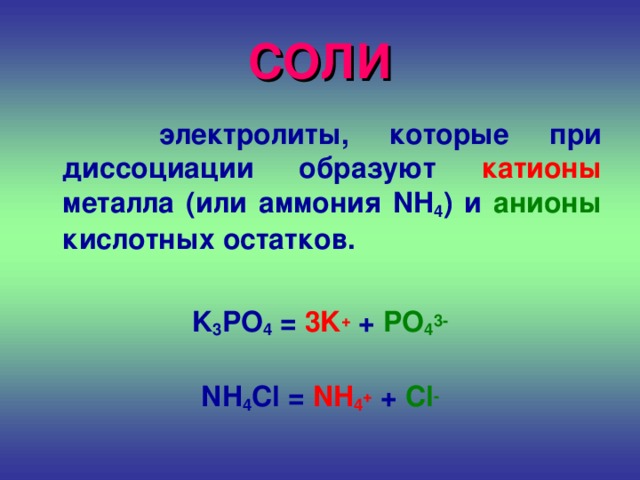
СОЛИ
электролиты, которые при диссоциации образуют катионы металла (или аммония NH 4 ) и анионы кислотных остатков.
K 3 PO 4 = 3K + + PO 4 3-
NH 4 Cl = NH 4 + + Cl -

Закрепление
Вариант 1
Вариант 2
1. Катион - это
А) положительно заряженный ион
Б) отрицательно заряженный ион
В) ион, не имеющий заряда
Г) нейтрально заряженный ион
2. Анион - это
А) положительно заряженный ион
Б) отрицательно заряженный ион
В) ион, не имеющий заряда
Г) нейтрально заряженный ион
3. Хлорид-анион имеет заряд:
А) +2 Б) +1 В) -1 Г) -2
4. Катион магния имеет заряд:
А) 0 Б) +1 В) +2 Г) +3
5. Укажите правильное уравнение диссоциации сульфата натрия
А ) Na 2 SO 4 = 2Na 1+ + SO 4 2-
Б ) Na 2 SO 3 = 2Na 1+ + SO 3 2-
В ) Na 2 SO 4 = Na 2+ + SO 4 2-
Г ) NaSO 4 = Na 1+ + SO 4 2-
1. Анион – это
А) ион, не имеющий заряда Б) положительно заряженный ион
В) отрицательно заряженный ион Г) нейтрально заряженный ион
2. Катион – это
А) ион, не имеющий заряда Б) положительно заряженный ион
В) отрицательно заряженный ион Г) нейтрально заряженный ион
3. Сульфат-анион имеет заряд:
А) +2 Б) +1 В) -1 Г) -2
4. Катион алюминия имеет заряд:
А) 0 Б) +1 В) +2 Г) +3
5. Укажите правильное уравнение диссоциации фосфата натрия
А) Na 3 Р O 4 = 3 Na 1+ + Р O 4 3-
Б) Na 3 Р O 3 = 3 Na 1+ + Р O 3 3-
В) Na 3 Р O 4 = Na 3+ + Р O 4 3-
Г) Na Р O 4 = Na 1+ + Р O 4 3-

Ответы
Вариант 1
Вариант 2
1. А
2. Б
3. В
4. В
5. А
1. В
2. Б
3. Г
4. Г
5. А

ДОМАШНЕЕ ЗАДАНИЕ
§ 36, упр. 1(б, в), 3, 4, 5 ( по учебнику Габриеляна О.С., 8 класс)

Ответьте на утверждение
«да» или «нет»:
1. На уроке было над
чем подумать
2. Я понял(а) новую тему
3. На все возникшие у меня
вопросы я получил(а) ответы
4. На уроке я поработал(а)
добросовестно
5. Оцените свою работу на уроке по пятибалльной системе.

СПАСИБО за урок!





















































