Проверочная работа по теме «Фосфор и его соединения» 9 класс
Вариант № 1
Тест. К каждому заданию дается 4 варианта ответов, из которых только один правильный
1. Распределение электронов по энергетическим уровням в атоме фосфора
А) 2,8,3 В) 2,5 С) 2,8,5 D) 2,8,8,5
2.Оксид фосфора (V) не взаимодействует с
A) нитратом серебра B) водой C) гидроксидом кальция D) оксидом кальция
3. Сумма коэффициентов в уравнении взаимодействия магния с фосфором: A) 5 B) 7 C) 6 D) 8
4. Фосфор является восстановителем при взаимодействии с
А) магнием В) водородом С) хлором D) натрием
5. Массовая доля кислорода ( в %) в ортофосфорной кислоте равна: A) 3,1 B) 31,5 C)16,3 D) 65,3
6.Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения: P 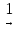 P2O5
P2O5 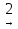 К3PO4
К3PO4  Ag3PO4. Последнее уравнение запишите в ионном полном и сокращенном видах.
Ag3PO4. Последнее уравнение запишите в ионном полном и сокращенном видах.
Задача. Определите массу фосфата натрия, полученного при взаимодействии 200 г 10% - ного раствора гидроксида натрия с фосфорной кислотой.
Ъ
Проверочная работа по теме «Фосфор и его соединения» 9 класс
Вариант № 2
Тесты. К каждому заданию дается 4 варианта ответов, из которых только один правильный
1. Число электронов на внешнем уровне атома фосфора A) 15 B) 2 C) 3 D) 5
2. Оксид фосфора (V) взаимодействует с
A) оксидом серы (VI) B) кислородом C) оксидом натрия D) азотной кислотой
3. Сумма коэффициентов в уравнении взаимодействия кальция с фосфором A) 5 B) 6 C) 10 D) 8
4. Чему равна степень окисления фосфора в Н3РО4 А) +3 В) +5 С) +5 D)+3
5. Массовая доля кислорода ( в %) в оксиде фосфора (V) равна: A) 56,3 B) 43,7 C) 11,3 D) 21,8
Упражнения. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:P2O5 -----H3PO4 ---- K3PO4 ----Ca3(PO4)2 . Второе уравнение запишите в ионном полном и сокращенном видах..
Задача. Какая масса фосфата серебра образуется при взаимодействии нитрата серебра с 250 г 20 % - ного раствора фосфорной кислоты?
Проверочная работа по теме «Углерод и его соединения» 9 класс
Вариант№1
Тесты. К каждому заданию дается 4 варианта ответов, из которых только один правильный
1.Распределение электронов по энергетическим уровням в атоме углерода А) 2,4 B)2, 8,5 C)2,6 D)2,7
2.Аллотропная модификация углерода
A) aлмаз, графит, кокс B) aлмаз, графит, карбин C) aлмаз, графит, сажа D) aлмаз, графит, уголь
3.Атомы кремния и атомы углерода сходны между собой А)зарядом ядра В)числом валентных электронов
С) числом энергетических уровней D) общим количеством электронов
4. В лаборатории углекислый газ получают А) сжиганием метана В) сжиганием угля в избытке кислорода
С) обжигом известняка D) взаимодействие мрамора с соляной кислоты
5. При взаимодействии карбоната кальция с соляной кислотой одним из продуктов реакции образуется :А)С(т) В)О2(г) С)СО (г) D)СО2(г)
Упражнения. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения CaO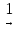 Са(NO3)2
Са(NO3)2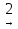 CaCO3
CaCO3 CO2. Второе уравнение запишите в ионном полном и сокращенном видах.
CO2. Второе уравнение запишите в ионном полном и сокращенном видах.
Задача. 1.Вычислить объём углекислого газа, полученного при взаимодействии карбоната натрия с 300 г 5 % - ного раствора соляной кислоты..
Проверочная работа по теме «Углерод и его соединения» 9 класс
Вариант№2
Тесты. К каждому заданию дается 4 варианта ответов, из которых только один правильный
1.Электронная формула атома углерода А)1s22s22p63s23p3 В)1s22s22p2 С)1s22s22p4 D) 1s22s22p6
2.Аллотропная модификация углерода A) алмаз, графит, кокс B) алмаз, графит, сажа C) алмаз, графит, фуллерен D) алмаз, графит, уголь
3.Oксид углерода (II) имеет характер А)кислотный В)амфотерный С)основной D) несолеобразующий
4. Карбонат-ион можно обнаружить с помощью А) КОН В) HCl С) NaCl D) КCl
5.Оксид углерода (IV) НЕ реагирует с :А) магнием В)водой С) фосфорной кислотой D)гидроксидом калия
Упражнения. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения CO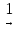 CO2
CO2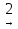 K2CO3
K2CO3 CO2. Второе уравнение запишите в ионном полном и сокращенном видах.
CO2. Второе уравнение запишите в ионном полном и сокращенном видах.
Задача. Определите объём углекислого газа, полученного при взаимодействии серной кислоты с 500 г карбоната кальция, содержащего 10 % примесей.
Проверочная работа по теме «Углерод. Кремний.» (9 класс)
1 вариант
Заряд ядра кремния: 1)+12 2) +14 3) +28 4) +15
Электронная формула кремния?
1) 1s22s22p63s23p3 2) 1s22s22p63s23p4 3) 1s22s22p2 4) 1s22s22p63s23p2
Степени окисления углерода: 1) -3,+3,+5 2) -4,+2,+4 3) +2,+4,+6 4) -3,+5
Соли кремневой кислоты называют: 1) нитраты 2) карбонаты 3) фосфаты 4) силикаты
Формула кремнезема: 1) MgSiO3 2) SiO2 3) Mg2Si 4) Na2SiO3
Аллотропная модификация углерода – алмаз:
1) твердое, прозрачное, бесцветное, аморфное вещество
2) мягкое, прозрачное, серое, кристаллическое вещество
3) твердое, прозрачное, бесцветное, кристаллическое вещество
4) твердое, непрозрачное, бесцветное, кристаллическое вещество
Высший оксид состава RO2 образует: 1) азот 2) углерод 3) сера 4) бром
Число формул соединений кремния, в которых степень окисления этого элемента + 4, в следующем перечне: Na2SiO3, SiO, SiF4, SiO2, SiH4 равно:
1) одному 2) двум 3) трём 4) четырём
По какому уравнению нельзя получить углекислый газ:
C + H2O =
С + O2 =
CaCO3 =
CaCO3 + HCl =
При фотосинтезе в атмосферу выделяется: 1) O2 2) CO2 3) H2O 4) N2
Какая реакция используется для получения кремниевой кислоты:
1) H2O + SiO2 =
2) Na2SiO3 + HCl =
3) K2SiO3 + H2O =
4) H2 + SiO2 =
12.Сокращенное ионное уравнение реакции 2H+ + SiO32- = H2SiO3 соответствует взаимодействию:
1) соляной кислоты с силикатом натрия
2) азотной кислоты с силикатом кальция
3) угольной кислоты с силикатом магния
4) фосфорной кислоты с силикатом вария
13. Из данного перечня выберите вещества, с которыми взаимодействует кремний и составьте уравнения реакций: магний, сера, вода, кислород, водород, хлор, углерод, гидроксид натрия, плавиковая кислота, серная кислота, оксид железа (II).
14. Расставьте коэффициенты методом электронного баланса:
NaNO2 + KMnO4 + H2SO4 = MnSO4 + NaNO3 + K2SO4 + H2O
15. Вычислите массу карбоната кальция, который образуется при пропускании через избыток известковой воды (Ca(OH)2) углекислого газа объёмом 11.2л.
Проверочная работа по теме «Углерод. Кремний.» (9 класс)
2 вариант
Заряд ядра атома углерода: 1)+12 2) +6 3) +28 4) +15
Электронная формула атома углерода С ?
1) 1s22s22p2 2) 1s22s22p63s23p2 3) 1s22s12p3 4) 1s12s22p3
Степени окисления кремния: 1) -3,+3,+5 2) -4, +2 ,+4 3) +2,+4,+6 4) -3,+5
Соли угольной кислоты называют:
1) нитраты 2) карбонаты 3) фосфаты 4) силикаты
Оксид кремния - вещество:
1) твердое, цветное, прозрачное
2) твердое, кристаллическое вещество полимерного строения
3) мягкое, бесцветное, прозрачное
4) твердое, бесцветное, непрозрачное
Формула кварца: 1) MgSiO3 2) SiO2 3) Mg2Si 4) Na2SiO3
Оксид кремния не применяется при производстве:
1) стекла 2) керамических изделий 3) жаропрочных сталей 4)топлива
Аллотропная модификация углерода – графит:
1) твердое, прозрачное, бесцветное, аморфное вещество
2) мягкое, непрозрачное, серое, кристаллическое вещество
3) твердое, прозрачное, бесцветное, кристаллическое вещество
4) твердое, непрозрачное, бесцветное, кристаллическое вещество
Какая реакция практически осуществима:
1) CaCO3 + H2О =
2) CaCO3 + NaOH =
3) C + O2 =
4) CaCO3 + K2O =
При добавлении к карбонатам кислот образуется газ:
1) O2 2) CO2 3) H2O 4) N2
Выберите реакцию, которая неосуществима:
1) SiO2 + NaOH = 2) SiO2 + CaO =
3) SiO2 + K2CO3 = 4) SiO2 + H2O =
Сокращенное ионное уравнение реакции 2H+ + SiO32- = H2SiO3 соответствует взаимодействию:
1) серной кислоты с силикатом кальция
2) серной кислоты с силикатом натрия
3) угольной кислоты с силикатом кальция
4) угольной кислоты с силикатом натрия
13. Из данного перечня выберите вещества, с которыми взаимодействует углерод и составьте уравнения реакций: кальций, вода, кислород, водород, кремний, гидроксид натрия, азотная кислота, серная кислота (к), оксид меди (II).
14. Расставьте коэффициенты методом электронного баланса:
KMnO4 +Na2SO3 + H2SO4 = MnSO4 + Na2SO4 + K2SO4 + H2O
15. Вычислите массу карбоната кальция, который образуется при пропускании через избыток известковой воды (Ca(OH)2) углекислого газа объёмом 44.8 л.























