
Свинец и олово –
Металлы древности

Олимпиодр (VI в.), греческий философ и астролог, профессор Александрийской школы. Он соотнес 7 планет древности с 7 металлами и ввел обозначение.
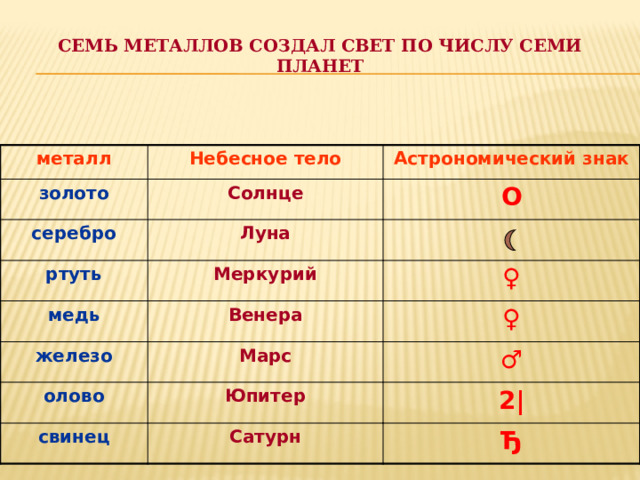
Семь металлов создал свет по числу семи планет
металл
Небесное тело
золото
Астрономический знак
Солнце
серебро
Луна
O
ртуть
медь
Меркурий
Венера
♀
железо
♀
Марс
олово
Юпитер
♂
свинец
2|
Сатурн
Ђ

Свинец (лат. Plumbum)
- Свинец – это синевато-серый мягкий и тяжелый металл, это цветной металл.
- Содержание свинца в земной коре 1,6×10-3% по массе. Самородный свинец встречается крайне редко. Относительная атомная масса ( A r = 207,2) является усредненной из масс нескольких изотопов: 204 Pb (1,4%), 206 Pb (24,1%), 207 Pb (22,1%) и 208 Pb (52,4%). Последние три нуклида – конечные продукты естественных радиоактивных превращений урана, актиния и тория. Чаще всего свинец встречается в виде в виде сульфида PbS . Этот хрупкий блестящий минерал серого цвета называют галенитом, или свинцовым блеском.
- Плавится свинец при температуре 327,4°С, а кипит при 1725°С. Плотность его 11,34 г/см. Свинец – пластичный, мягкий металл: он режется ножом, царапается ногтем.
- Свинец на свежем разрезе синевато-серого цвета, быстро тускнеет на воздухе, покрываясь пленкой окиси.

Химические свойства свинца
По химическим свойствам свинец – малоактивный металл: в электрохимическом ряду напряжений он стоит непосредственно перед водородом. Поэтому свинец легко вытесняется другими металлами из растворов его солей.
Наиболее типична для свинца степень окисления +2; соединения свинца(IV) значительно менее устойчивы. В разбавленных соляной и серной кислотах свинец практически не растворяется, в том числе из-за образования на поверхности нерастворимой пленки хлорида или сульфата. С крепкой серной кислотой (при концентрации более 80%) свинец реагирует с образованием растворимого гидросульфата Pb(HSO 4 ) 2
![Тонкоизмельченный свинец обладает пирофорными свойствами – вспыхивает на воздухе. При продолжительном нагревании расплавленного свинца он постепенно переходит сначала в желтый оксид PbO (свинцовый глет), а затем (при хорошем доступе воздуха) – в красный сурик Pb 3 O 4 или 2PbO·PbO 2 . Это соединение можно рассматривать также как свинцовую соль ортосвинцовой кислоты Pb 2 [PbO 4 ].](https://fsd.multiurok.ru/html/2023/03/29/s_6423c26bcd825/img5.jpg)
Тонкоизмельченный свинец обладает пирофорными свойствами – вспыхивает на воздухе. При продолжительном нагревании расплавленного свинца он постепенно переходит сначала в желтый оксид PbO (свинцовый глет), а затем (при хорошем доступе воздуха) – в красный сурик Pb 3 O 4 или 2PbO·PbO 2 . Это соединение можно рассматривать также как свинцовую соль ортосвинцовой кислоты Pb 2 [PbO 4 ].

Разбавленной азотной кислотой свинец легко окисляется:
Pb + 4HNO 3 → Pb(NO 3 ) 2 + 2NO 2 + H 2 O.
Разложение нитрата свинца(II) при нагревании – удобный лабораторный метод получения диоксида азота:
2Pb(NO 3 ) 2 → 2PbO + 4NO 2 + O 2 .
В присутствии кислорода свинец растворяется также в ряде органических кислот . При действии уксусной кислоты образуется легкорастворимый ацетат Pb(CH 2 COO) 2 (старинное название – «свинцовый сахар»). Свинец заметно растворим также в муравьиной, лимонной и винной кислотах. Растворимость свинца в органических кислотах могло раньше приводить к отравлениям, если пищу готовили в посуде, луженной или паянной свинцовым припоем.
Растворимые соли свинца (нитрат и ацетат) в воде гидролизуются:
Pb(NO 3 ) 2 + H 2 O → Pb(OH)NO 3 + HNO 3 .
Взвесь основного ацетата свинца («свинцовая примочка») имеет ограниченное медицинское применение в качестве наружного вяжущего средства.

В прошлом свинец довольно широко применялся в различных областях прикладного искусства. Например, в средневековой Англии и Франции он применялся для крыш и водосточных труб дворцов и соборов.
Из свинца и его сплавов выделывались художественная посуда, а также предметы домашнего обихода - гребни, ложки и т. п. Иногда из него отливали скульптуры и декоративные детали архитектуры. Например, знаменитый Петергофский "Самсон, раздирающий пасть льва", первоначально был отлит из свинца (1714 г.) и простоял до 1798 г., после чего был заменен бронзовым.

Свинец употреблялся как составная часть хрусталя для повышения его блеска, а также для усиления яркости цвета и блеска при варке художественных эмалей и смальты. Сейчас в этих производствах свинец заменяется калием и другими элементами, не обладающими такими ядовитыми свойствами, как свинец.

Свинец проникает в организм через желудочно-кишечный тракт или дыхательную систему и разносится затем кровью по всему организму. Причем вдыхание свинцовой пыли значительно опаснее присутствия свинца в пище. В воздухе городов содержание свинца составляет в среднем от 0,15 до 0,5 мкг/м 3 . В районах, где расположены предприятия по переработке полиметаллических руд, эта концентрация выше.
Свинец накапливается в костях, частично замещая кальций в фосфате Са 3 (РО 4 ) 2 . Попадая в мягкие ткани – мышцы, печень, почки, головной мозг, лимфатические узлы, свинец вызывает заболевание – плюмбизм .
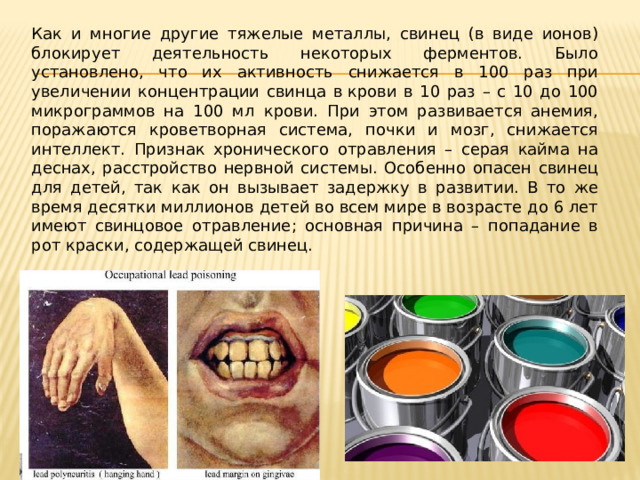
Как и многие другие тяжелые металлы, свинец (в виде ионов) блокирует деятельность некоторых ферментов. Было установлено, что их активность снижается в 100 раз при увеличении концентрации свинца в крови в 10 раз – с 10 до 100 микрограммов на 100 мл крови. При этом развивается анемия, поражаются кроветворная система, почки и мозг, снижается интеллект. Признак хронического отравления – серая кайма на деснах, расстройство нервной системы. Особенно опасен свинец для детей, так как он вызывает задержку в развитии. В то же время десятки миллионов детей во всем мире в возрасте до 6 лет имеют свинцовое отравление; основная причина – попадание в рот краски, содержащей свинец.

Применение свинца
Несмотря на ядовитость свинца, отказаться от него невозможно. Свинец дешев – вдвое дешевле алюминия, в 11 раз дешевле олова. После того как в 1859 французский физик Гастон Планте изобрел свинцовый аккумулятор, для изготовления аккумуляторных пластин с тех пор израсходовали миллионы тонн свинца; в настоящее время на эти цели уходит в ряде стран до 75% всего добываемого свинца!

Постепенно снижается применение свинца для изготовления очень ядовитого антидетонатора – тетраэтилсвинца. Способность тетраэтилсвинца улучшать качество бензина было открыто группой молодых американских инженеров в 1922; в своих поисках они руководствовались периодической таблицей элементов, планомерно приближаясь к наиболее эффективному средству. С тех пор производство тетраэтилсвинца непрерывно росло; максимум приходится на конец 1960-х, когда только в США ежегодно с выхлопами выбрасывались сотни тысяч тонн свинца – по килограмму на каждого жителя! В последние годы применение этилированного бензина запрещено во многих регионах, и его производство снижается.

Мягкий и пластичный свинец, не ржавеющий в присутствии влаги, – незаменимый материал для изготовления оболочек электрических кабелей; на эти цели в мире расходуется до 20% свинца.
Тяжелый свинец хорошо задерживает губительные для человека излучения и потому свинцовые экраны используются для защиты работников рентгеновских кабинетов, в свинцовых контейнерах хранят и перевозят радиоактивные препараты. Свинец содержат также подшипниковые сплавы баббиты, «мягкие» припои (самый известный – «третник» – сплав свинца с оловом).
Олово (лат. Stannum)
- Олово – один из металлов , известных людям с древности. Сплав олова с медью – бронза – был впервые получен более 4000 лет назад. Бронза и в наши дни остается главным сплавом олова. Олово – средний по распространенности элемент, в природе он встречается в составе 24 минералов, 2 из них – касситерит и станин – имеют промышленное значение.
- Олово – достаточно пластичный серебристо-белый металл, плавится при 231,9°С, кипит при 2270°С.
- Это всем известное белое олово – знакомый и привычный металл, из которого раньше отливали оловянных солдатиков, делали посуду и которым до сих пор покрывают изнутри консервные банки. Процесс превращения белого олова в серое быстрее всего идет при -33°С. Это превращение получило образное название «оловянной чумы». В прошлом оно не раз приводило к драматическим последствиям.
- Химическая стойкость олова достаточно высока. При температуре до 100°С оно практически не окисляется кислородом воздуха – лишь поверхность покрывается тонкой оксидной пленкой состава SnO2. Растворяет олово и азотная кислота, даже разбавленная, и на холоде.
- Большая часть олова идет на производство припоев и сплавов, главным образом типографских и подшипниковых.

При понижении температуры воздуха ниже 0 °С белое олово переходит в модификацию серого олова. При этом объем вещества увеличивается почти на четверть, оловянное изделие трескается и превращается в серый порошок. Это явление стали называть «оловянной чумой».
Некоторые историки считают, что «оловянная чума» послужила одной из причин поражения армии Наполеона в России, так как превратила пуговицы на одежде французских солдат и пряжки для ремней в порошок, и тем самым оказала на армию деморализующее влияние.

Олово считается безопасным для человека, оно есть в нашем организме и каждый день мы получаем его в минимальных количествах с пищей.
Пары олова и его аэрозольные частицы опасны, так как при длительном и регулярном вдыхании оно может вызвать заболевания легких; ядовиты также органические соединения олова, поэтому работать с ним и его соединениями надо в средствах защиты.
Такое соединение олова как оловянистый водород, SnH 4 , может служить причиной тяжелых отравлений при употреблении в пищу очень старых консервов, в которых органические кислоты вступили в реакцию со слоем олова на стенках банки (жесть, из которой делают консервные банки — это тонкий лист железа, покрытый с двух сторон оловом). Отравление оловянистым водородом может быть даже смертельным. К его симптомам относятся судороги и чувство потери равновесия.

Применение олова
— Большая часть выплавляемого олова используется в металлургии для производства различных сплавов. Эти сплавы идут на изготовление подшипников, фольги для упаковки, белой пищевой жести, бронзы, припоев, проводов, литер типографских шрифтов.
— Олово в виде фольги (станиоль) востребовано в производстве конденсаторов, посуды, изделий искусства, органных труб.

Из олова получается также двусернистое олово, представляющее собой блестящую массу, очень похожую по цвету на золото. Это вещество под названием "серного золота", "муссивного" или "сусального золота" в виде тончайших листков или порошка применяется для отделки под золото различных металлических, деревянных или гипсовых изделий. Двусернистое олово очень стойко и надолго сохраняет блеск при применении его не только в интерьере, но и в экстерьерных условиях.












![Тонкоизмельченный свинец обладает пирофорными свойствами – вспыхивает на воздухе. При продолжительном нагревании расплавленного свинца он постепенно переходит сначала в желтый оксид PbO (свинцовый глет), а затем (при хорошем доступе воздуха) – в красный сурик Pb 3 O 4 или 2PbO·PbO 2 . Это соединение можно рассматривать также как свинцовую соль ортосвинцовой кислоты Pb 2 [PbO 4 ].](https://fsd.multiurok.ru/html/2023/03/29/s_6423c26bcd825/img5.jpg)
































