ОКСИДЫ
1. Допишите уравнения реакций:
CuO + HNO3 → BeO + KOH (р-р) →
Cr2O3 + Ba(OH)2 → BeO + HNO3 →
CaO + H2SO4 → CO2 + NaOH →
Составьте уравнения возможных реакций.
2. С какими из веществ, формулы которых приведены ниже, взаимодействует оксид бария:
HNO3, КОН, Н2О, НCl, Са(ОН)2?
Составьте уравнения возможных реакций.
3. Выберите формулы веществ, с которыми взаимодействует оксид фосфора (V):
НCl, NaOH, Н2О, H2SO4, Ba(OH)2.
Составьте уравнения возможных реакций.
4. Возможно ли взаимодействие между следующими веществами:
SO2 и PbO, Li2O и Cr2O3, BaO и CO2,
CO2 и CuO, SO2 и Al2O3, SnO и SiO2?
Напишите уравнения соответствующих реакций.
5. Приведите уравнения реакций, характеризующих химические свойства основных оксидов на примере:
а) SrO, б) FeO.
6. Приведите уравнения реакций, характеризующих химические свойства кислотных оксидов, на примере:
а) SO2, б) SiO2.
7. Приведите уравнения реакций, характеризующих химические свойства амфотерных оксидов, на примере:
а) Al2O3, б) ZnO.
8. С какими из перечисленных веществ взаимодействует Р2О5:
Li2O, H2SO4, SO3, Ba(OH)2, ZnO, SiO2, Fe2O3, Н2О, Cr2O3?
Напишите уравнения возможных реакций, укажите условия их протекания.
9. С какими из перечисленных веществ взаимодействует СаО:
HNO3, Н2О, Р2О5, NaOH, FeO, H2SO4?
Напишите уравнения возможных реакций, укажите условия их осуществления.
10. Зная свойства оксидов, приведите уравнения реакций, с помощью которых можно получить следующие вещества:
а) Ba(OH)2, в) Na2СО3 (2 способа),
б) Н2CrО4, г) Са3(РО4)2 (2 способа).
ОСНОВАНИЯ
1. Допишите уравнения возможных реакций. Составьте полные и краткие ионные уравнения реакций:
1) КОН + СО2 → 4) Fe(OН)3 + К2SO4 →
2) Fe(OН)3 + HNO3 → 5) NaOH + Са3(РО4)2 →
3) КОН + ZnSO4 → 6) NaNO3 + КОН →
2. Приведите уравнения реакций, характеризующих химические свойства: а) гидроксида калия, б) гидроксида железа (II).
3. С какими из веществ, формулы которых указаны ниже, взаимодействует гидроксид никеля (II):
HNO3, КОН, Mg(OН)2, H2SO4, CuSO4, FeО?
Составьте уравнения соответствующих реакций.
4. С какими из соединений, формулы которых приведены ниже, взаимодействует гидроксид калия:
НCl, FeCl3, Cu(ОН)2, СО2, Р2О5, ZnO?
Составьте уравнения соответствующих реакций.
5. Как осуществить следующие превращения:
Fe(ОН)3 → Fe(NO3)3; Fe(ОН)3 → Fe2(SO4)3; Fe(ОН)3 → FeО?
Составьте уравнения реакций в молекулярной и ионной формах.
6. Зная свойства оксидов и оснований, приведите по два уравнения реакций получения:
а) Ва3(РО4)2; б) CuSO4.
КИСЛОТЫ
1. Допишите уравнения возможных реакций. Какие из них являются окислительно-восстановительными? Укажите окислитель в каждой из них:
1) Cr(ОН)3 + HNO3 → 5) Ba(NO3)2 + НCl →
2) ZnO + H2SO4 → 6) Al2O3 + HNO3 →
3) Нg + НCl → 7) H2SO4 (разб.) + Al →
4) Нg + HNO3 (конц.) →
2. С какими из веществ, формулы которых указаны ниже, реагирует разбавленная серная кислота:
Fe2O3, Мg, Са(ОН)2, Zn(OН)2, Cu, Р2О5, Нg?
Приведите молекулярные и ионные уравнения реакций.
3. Как осуществить следующие превращения:
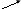 CuSO4
CuSO4
C uО
uО
CuCl2
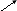 Cu(NO3)2 (3 способа)
Cu(NO3)2 (3 способа)
H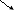 NO3
NO3
КNO3 ?
4. Приведите уравнения реакций, с помощью которых можно получить следующие соли:
а) хлорид алюминия,
б) сульфат цинка.
АМФОТЕРНЫЕ ГИДРОКСИДЫ
1. С какими из веществ, формулы которых приведены ниже, взаимодействует гидроксид цинка:
HNO3, Cu(ОН)2, Н2О, СО2, КNO3, КОН?
Составьте уравнения соответствующих реакций в молекулярной и ионной формах.
2. Как осуществить следующие превращения:
A l(ОН)3 → Al2О3 → Al(NO3)3 → Al(ОН)3 → К3[Al(ОН)6] ?
l(ОН)3 → Al2О3 → Al(NO3)3 → Al(ОН)3 → К3[Al(ОН)6] ?
К3[Al(ОН)6]
Приведите молекулярные и ионные уравнения реакций.
СОЛИ
1. Какие из предложенных процессов возможны в растворе и осуществляются до конца? Приведите молекулярные и ионные уравнения реакций:
1) К2СО3 + NaOH → 5) КСl + Sr(OН)2 →
2) Al(ОН)3 + NaСl → 6) Са(NO3)2 + КОН →
3) CuSO4 + Ва(ОН)2 → 7) Fe(ОН)3 + ZnСl2 →
4) PbS + Са(ОН)2 → 8) КОН + Fe2(SO4)3 →
2. Какие из предложенных процессов возможны в растворе и осуществляются до конца? Приведите уравнения реакций в молекулярной и ионной формах. Объясните направленность процессов:
1) ZnSO4 + НСl → 4) NaNO3 + Н2S →
2) FeS + H2SO4 → 5) К2SiO3 + НСl →
3) ВаСО3 + HNO3 → 6) H2SO4 + ВаСl2 →
3. Напишите уравнения возможных реакций в молекулярной и ионной формах. Объясните направленность процессов:
1) Na2S + КСl → 5) NН4NО3 + ZnСl2 →
2) ВаS + CuSO4 → 6) PbСl2 + К2S →
3) Cr2(SO4)3 + FeCl3 → 7) АgNO3 + CuCl2 →
4) СаСО3 + КNO3 → 8) Na2СО3 + Са(NO3)2 →
4. Какие из приведённых соединений реагируют с содой (Na2СО3) в растворе:
К2СО3, НСl, СаСl2, H2SO4, CuО, Na2SiO3, КСl, Са(ОН)2, Ва(NO3)2?
Составьте молекулярные и ионные уравнения возможных реакций.
5. Как осуществить превращения? Приведите уравнения реакций в молекулярной и ионной формах:
Мg(ОН)2 → МgSO4 → МgСО3 → МgCl2.
6. Какова реакция среды в растворах следующих солей: Ва(NO3)2, AlCl3, Na2S, ZnSO4?
Приведите соответствующие уравнения реакций гидролиза в молекулярной и ионной формах.
ГЕНЕТИЧЕСКАЯ ВЗАИМОСВЯЗЬ МЕЖДУ ВЕЩЕСТВАМИ
1. Составьте уравнения возможных реакций:
1
 ) Fe(ОН)3 t 6) МgСО3 t
) Fe(ОН)3 t 6) МgСО3 t
2
 ) Zn + О2 t 7) Al(NO3)3 t
) Zn + О2 t 7) Al(NO3)3 t
3
 ) Cu(NO3)2 t 8) H2SO3 t
) Cu(NO3)2 t 8) H2SO3 t
4
 ) Cl2 + О2 t 9) Аu + О2 t
) Cl2 + О2 t 9) Аu + О2 t
5
 ) С + О2 t 10) HNO3 t
) С + О2 t 10) HNO3 t
Какие из этих реакций являются окислительно-восстановительными? К каким типам реакций они относятся?
2. Как осуществить следующие превращения? Приведите уравнения соответствующих реакций:
1) ВаСО3 → СО2 (2 способа)
2) HNO3 → NO2 (2 способа)
3) К2SO3 → SO2
4) ZnS → ZnО
3. Какими способами можно получить каждый из следующих оксидов:
Al2O3, Р2О5, PbО, NO, CuО?
Составьте уравнения соответствующих реакций.
4. Можно ли получить указанные соли взаимодействием соответствующих основных оксидов с кислотами:
ZnCl2, CuS, Na2SO4, К2СO3?
Приведите уравнения возможных реакций.
5. Какие из указанных солей нельзя получить реакцией нейтрализации:
Cu(NO3)3, FeCl3, Fe2(СO3)3, Al2S3, Cr2(СO3)3, ZnSO4?
Напишите уравнения возможных реакций.
6. Укажите, какие из предлагаемых схем реакций могут быть использованы для получения солей:
1) Cu(NO3)2 + ВаSO4 → 5) Ва(ОН)2 + H2SO4 →
2) HNO3 + К2SO4 → 6) Na2СO3 + СаCl2 →
3) КCl + H2SO4 (р-р) → 7) SO3 + КОН →
4) Cu(ОН)2 + ZnCl2 → 8) КОН + Na2SO4 →
Приведите уравнения этих реакций. Объясните их направленность.
7. Как осуществить следующие превращения:
1) CuSО4 → Cu(NO3)2 → CuО → Cu(ОН)2 → CuО,
2) СаСО3 → СаО → СаCl2 → Са3(РО4)2,
3) Р2О5 → Na3РO4 → NaСl → NaNO3?
Приведите молекулярные и ионные уравнения реакций.
8. Даны следующие оксиды: Р2О5, Na2O, СаО, Al2О3, SiO2, МgО.
Какие из них могут попарно взаимодействовать? Сколько новых веществ может быть при этом получено? Напишите уравнения соответствующих процессов.
9. Даны вещества: медь, соляная кислота, хлор, кислород. Как, используя их, получить хлорид меди (II) двумя способами?
10. Как осуществить следующие превращения:
К
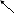 2SО4 КСl
2SО4 КСl

КNO3
11. Приведите уравнения реакций возможных способов получения следующих солей:
а) хлорида железа (II), сульфида свинца, хлорида кальция, хлорида железа (III);
б) нитрата цинка, сульфата калия, фосфата меди, фосфата натрия.
12. Допишите уравнения соответствующих реакций:
1) ВаСО3 + Н2О + СО2 →
2) Са(Н2РО4)2 + NaОН →
3) [PbОН]NO3 + HNO3 →
Составьте ионные уравнения реакций.
13. С помощью каких реакций можно осуществить следующие превращения:
1) Мg(НСО3)2 → МgСО3 → Мg(НСО3)2,
2) ZnCl2 → [ZnОН]Cl → ZnCl2,
3) Н3РО4 → Са3(РО4)2 → СаНРО4 → Са(Н2РО4)2 → Са3(РО4)2?
Составьте уравнения реакций.







 CuSO4
CuSO4 uО
uО Cu(NO3)2 (3 способа)
Cu(NO3)2 (3 способа)  NO3
NO3 l(ОН)3 → Al2О3 → Al(NO3)3 → Al(ОН)3 → К3[Al(ОН)6] ?
l(ОН)3 → Al2О3 → Al(NO3)3 → Al(ОН)3 → К3[Al(ОН)6] ?

 2SО4 КСl
2SО4 КСl

















