Анна Валерьевна Дзенис
Задачи на вывод молекулярной формулы углеводородов
I. По массовым долям элементов
Опорная информация:
1) Пусть имеется углеводород СхНу, тогда ω%(C) – массовая доля углерода 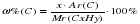 ,
,
преобразуя эту формулу, можно выразить «х» - число атомов углерода: 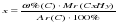 .
.
Аналогично: 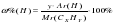 ,
,
преобразуем эту формулу, выражая число атомов водорода («у»):
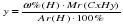 .
.
[Примечание: если по условию задачи известна массовая доля только одного элемента, то массовую долю второго элемента можно определить из формулы:  .]
.]
2) Относительную молекулярную массу углеводорода можно вычислить, зная величину относительной плотности данного углеводорода по какому-либо газу «А» (водород, кислород, гелий, азот или воздух и др):
Mr(СхНу ) = DА(СхНу) · Mr (А),
где DА(СхНу) - относительная плотность газообразного углеводорода СхНу по газу «А»; Mr ср.(воздуха) =29
DА(СхНу) - относительная плотность газообразного углеводорода СхНу по газу «А»; Mr ср.(воздуха) =29
Задача-образец: Определите молекулярную формулу углеводорода, содержащего 84% углерода, если относительная плотность данного вещества по азоту = 3,57.
| Общая схема решения задачи | Решение задачи-образец |
| Дано: а) ω % (C) или ω % (Н) б) DА (СXHY) или ρ Найти: СхНу
Последовательность действий: 1) Находим Mr (СXHY) : Если известна DА (СXHY), то Mr(СXHY) = DА (СXHY) • Mr(A) 2) Находим индексы (х и у): а) 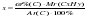
б) ω % (H) = 100 % - ω % (C)
в) 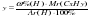 | Дано: а) ω % (C) = 84% б) DN2 (СXHY) = 3,57 Найти: СхНу
Решение: 1) Находим Mr (СXHY) : Mr(СXHY) = DN2 (СXHY) • Mr(N2) = 3,57 • 28 = 99,96
2) Находим индексы (х и у): а) 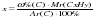 = = 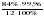 = 6,99 = 6,99
б) ω % (H) = 100 % - ω % (C) = 100 % - 84%= 16%
в)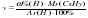 = =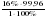 = 15,99 = 15,99
Ответ: С7Н16 |
1) Задача: Массовая доля углерода в углеводороде составляет 83,3%. Относительная плотность паров этого углеводорода по водороду = 36. Определите молекулярную формулу этого углеводорода.
2) Задача: Определите молекулярную формулу углеводорода, если массовая доля углерода в нем составляет 85,71%, а относительная плотность данного вещества по кислороду равна 1,3125.
3) Задача: Определите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 15,79%. Относительная плотность паров этого вещества по воздуху равна 3,93.
4) Задача: Определите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 18,2%. Относительная плотность данного вещества по азоту равна 1,57.
II. По продуктам сгорания
Задача-образец: При сгорании 92,8 г углеводорода образовалось 143,36 л оксида углерода (IV) и 144 г воды. Относительная плотность углеводорода по воздуху равна двум. Определите молекулярную формулу данного вещества.
| Общая схема решения задачи | Решение задачи-образец |
| Дано: а) m(CXHY) или V(CXHY) б) m(CO2) или V(CO2) в) m(H2O) г) DА (СXHY) Найти: СхНу
Последовательность действий: 1) а) Если известна m (CXHY), то сначала определяют М(CXHY): Mr(СXHY) = DА (СXHY) • Mr(A) б) Если известен V(CXHY), то переходим ко 2 действию.
2) Вычисляем : а) n (CXHY) ; б) n(CО2) ; в) n (H2O) по одной из формул: n(A) 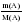 или n(A) или n(A) 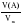 3) Вычисляем: а) n (C) = n (CО2) ; б) n (H) = 2• n (H2O). (Примечание: проверка на наличие атомов кислорода: m (О)= m (в-ва) - m (С) - m (Н) = m (в-ва) - 12 · n (C) - 1 · n (Н) )
4) Записываем соотношение: n (CXHY) : n (C) : n(H) Делим на наименьшее число.
5) Ответ: в 1 молекуле CXHY содержится …. атомов углерода и …. атомов водорода.
| Дано: а) m(CXHY) = 92,8 г б) V(CO2) = 143,36 л в) m(H2O) = 144 г г) Dвоздух (СXHY) = 2 Найти: СхНу
Решение:
1) Так как известна m (CXHY), то сначала определяют М(CXHY): Mr(СXHY) = Dвоздух (СXHY) • Mr(воздух) = 2 • 29 = 58
2) Вычисляем : а) n (CXHY) = = = 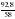 = 1,6 = 1,6 б) n(CО2) =  = = 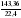 = 6,4 = 6,4 в) n (H2O) = 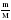 = = 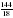 = 8 = 8
3) Вычисляем: а) n (C) = n (CО2) = 6,4 б) n (H) = 2 • n (H2O) = 2 • 8 = 16
(Так как по условию задачи известно, что сожгли углеводород, проверку на кислород делать не нужно)
4) Записываем соотношение: n (CXHY) : n (C) : n(H) 1,6 : 6,4 : 16 Делим на наименьшее число – на 1,6 :  : :  : : 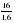 1 : 4 : 10
5) Ответ: С4Н10 |
5) Задача: Относительная плотность углеводорода по водороду равна
14. Определите молекулярную формулу этого вещества, если при сгорании 42 г его образовалось 54 г воды и 67,2 л углекислого газа.
6) Задача: 20,16 л углеводорода сожгли, в результате чего было получено 80,64 л оксида углерода (IV) и 64,8 г воды. Какова молекулярная формула исходного углеводорода?
7) Задача: При сжигании 6,72 л некоторого углеводорода образовалось 26,4 г оксида углерода (IV) и 10,8 г воды. Определите молекулярную формулу данного вещества.
8) Задача: Относительная плотность паров некоторого углеводорода по водороду = 64. В результате сгорания 3,2 г этого вещества образовалось 9,9 г углекислого газа и 4,5 г воды. Определите молекулярную формулу этого углеводорода.
9) Задача: При сжигании 28 л углеводорода было получено 84 л оксида углерода (IV) и 67,5 г воды. Плотность газа по водороду равна 21. Найти молекулярную формулу газа.
10) Задача: При сгорании 17,6 г углеводорода образовалось 52,8 г углекислого газа и 28,8 г воды. Относительная плотность исходного вещества по воздуху равна 1,517. Какова его молекулярная формула?







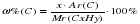 ,
, 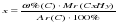 .
. 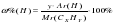 ,
, 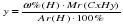 .
. .]
.] DА(СхНу) - относительная плотность газообразного углеводорода СхНу по газу «А»; Mr ср.(воздуха) =29
DА(СхНу) - относительная плотность газообразного углеводорода СхНу по газу «А»; Mr ср.(воздуха) =29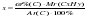
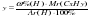
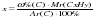 =
= 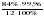 = 6,99
= 6,99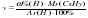 =
=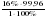 = 15,99
= 15,99 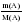 или n(A)
или n(A) 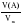
 =
= 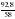 = 1,6
= 1,6 =
= 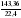 = 6,4
= 6,4 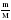 =
= 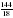 = 8
= 8 :
:  :
: