Согласован Утверждаю
на заседании ПЦК 18.02.07. зам. директора по УР
«___»________ «____»_____________
пр. ПЦК Павлинова Н.П. __________Улуханова И.В.
Проверочная работа №2
дисциплина физическая химия
«___»__________группа______ ______________
преподаватель Павлинова Н.П.
V вариант
1. Закону Гесса соответствует следующая формулировка:
1) Теплота расходуется на изменение внутренней энергии и совершение работы
2) Теплота не может переходит от холодного тела к горячему
3) Суммарный тепловой эффект химической реакции зависит от начального и конечного состояния систем, но не зависит от пути реакции и промежуточных стадий
4) Тепловой эффект химической реакции равен сумме теплот образования продуктов минус сумма теплот образования исходных веществ с учетом их коэффициентов.
2.Какая схема характеризует адиабатный процесс?
1)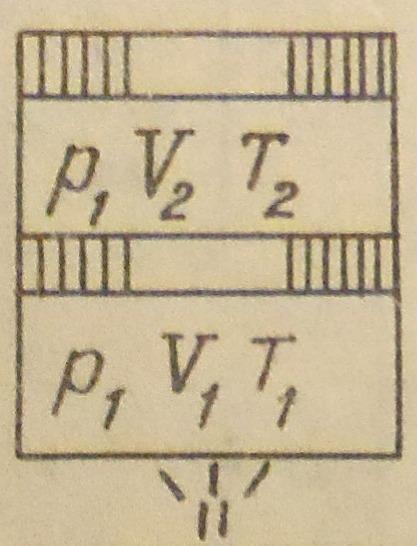 2)
2) 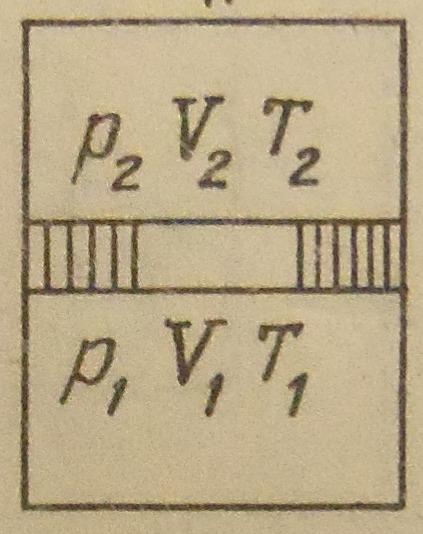 3)
3)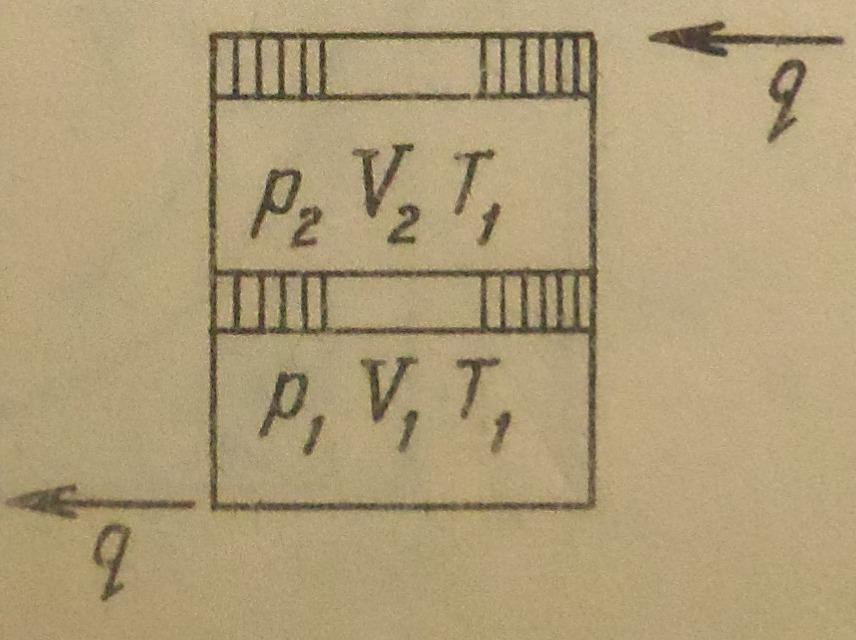 4)
4)
3. Тепловая машина состоит из
1) теплоотдатчика 2) рабочего тела 3) теплоотдатчика и рабочего тела 4)теплоотдатчика, рабочего тела и теплоприемника
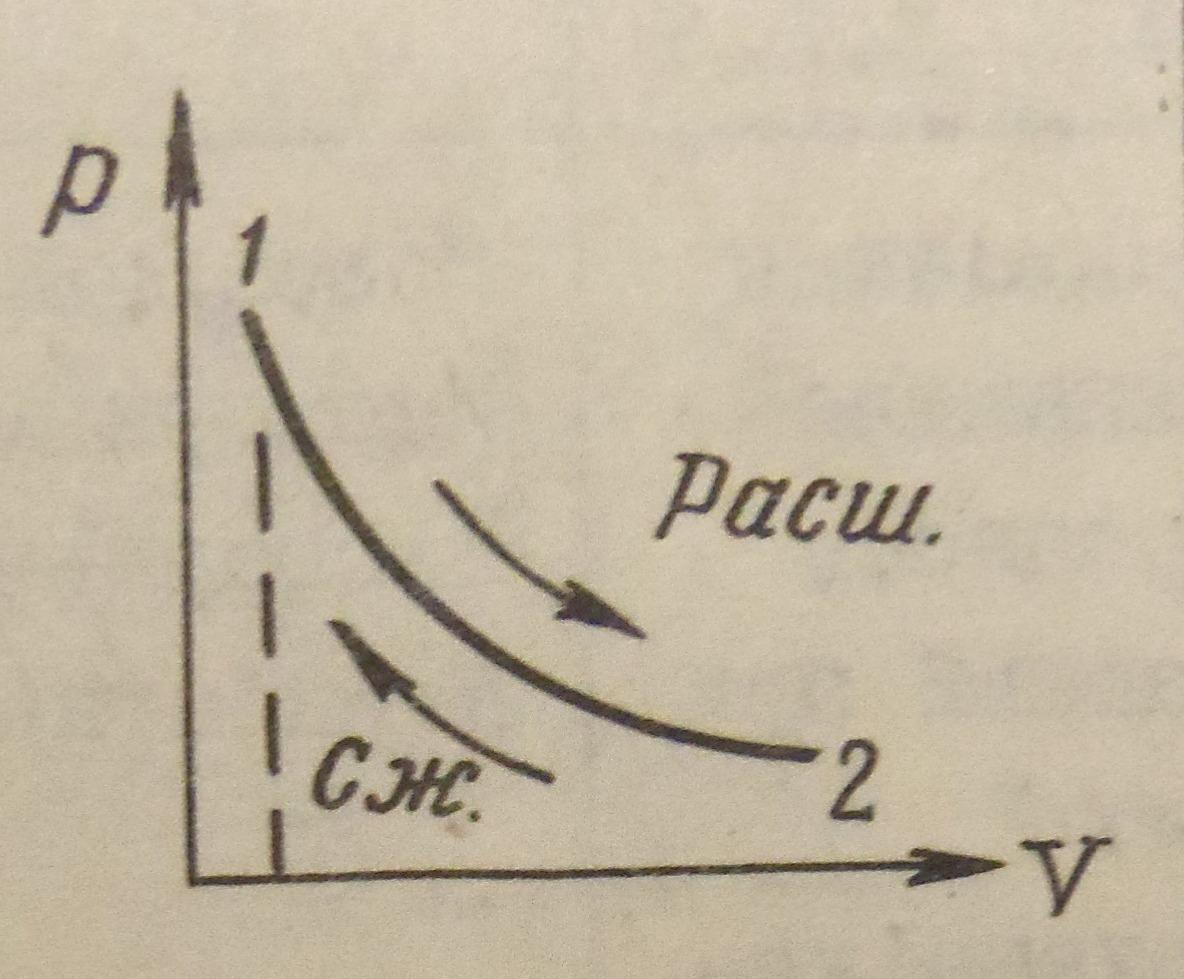
4.Укажите график изохоры в системе p-V координат
1)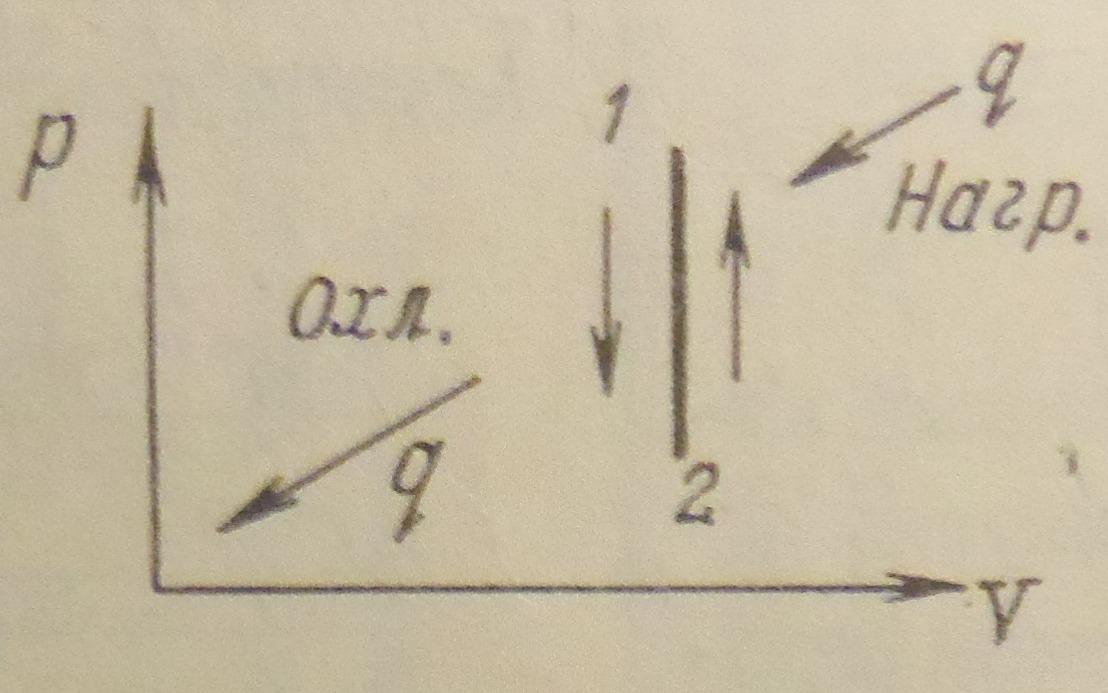 2)
2) 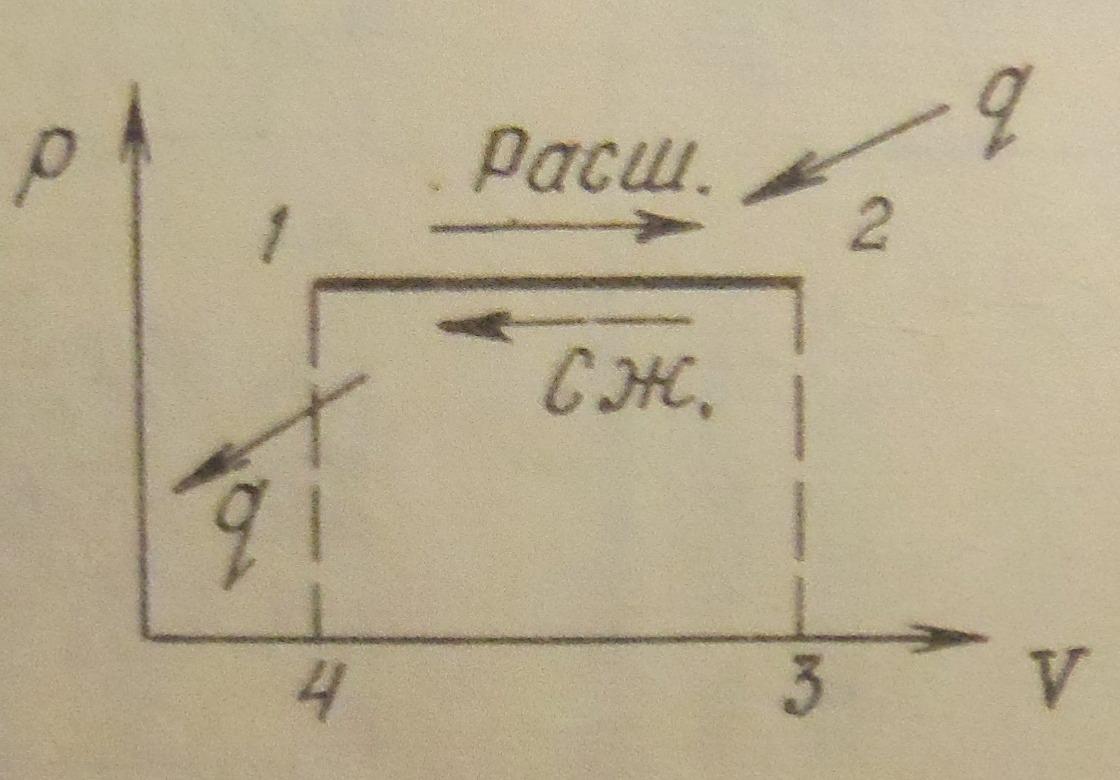 3)
3) 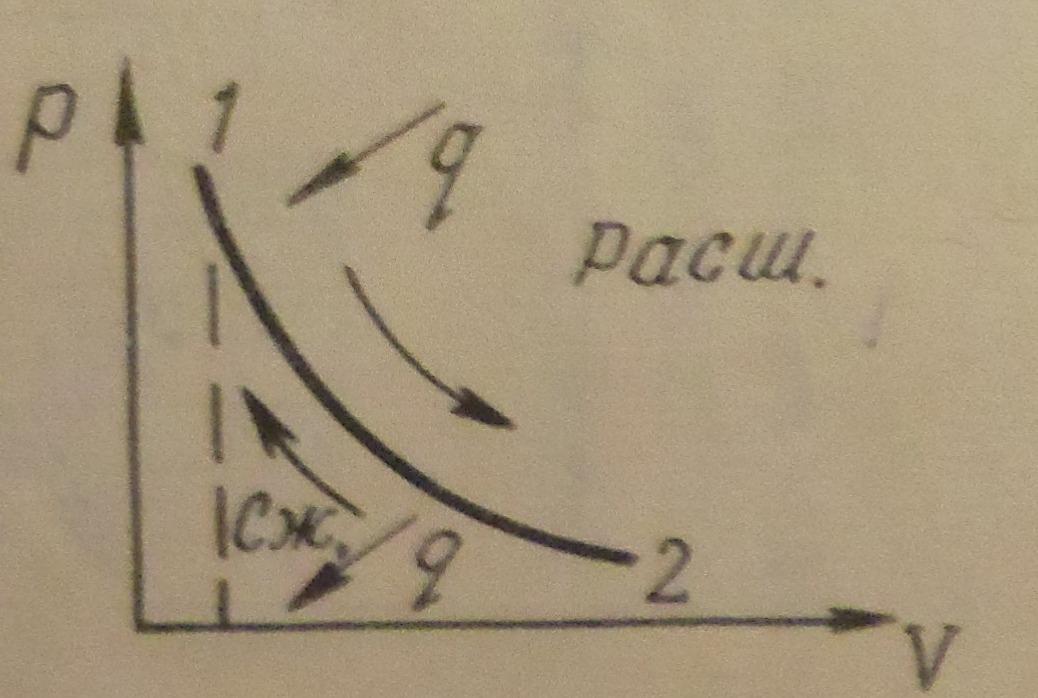 4)
4) 
5. Растворение представляет собой:
1)физический; 2)химический; 3)физико-химический процесс
6. Какая из приведённых реакций эндотермическая?
1.H2+�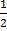 �O2=H2O(ж)∆H=-285КДж 2.�
�O2=H2O(ж)∆H=-285КДж 2.�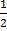 �N2+�
�N2+�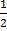 �O2=NO ∆H=90КДж 3.C2H2+2�
�O2=NO ∆H=90КДж 3.C2H2+2�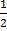 �O2=H2O+2CO2+1298КДж 4.H2+�
�O2=H2O+2CO2+1298КДж 4.H2+�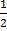 �O2=H2O(пар) ∆H=-242КДж
�O2=H2O(пар) ∆H=-242КДж
7. Теплота нейтрализации равна:
1) 56,98 кДж 2) 57,98 кДж 3)55,98 кДж 4)58,98 кДж
8. Определить разность между Qp и Qv при 25ºС для следующих реакций:
2С(граф)+О2=2СО
1) 4955Дж 2)2477Дж 3)-2477Дж 4)-4955Дж
9. Какое уравнение характеризует тепловой эффект при Р=const
1) Q=∆U 2)Q=A 3)Q=∆H 4) Q=const
10. При окислении 1 г. глюкозы (C6H12O6) выделилось 15,64 Кдж теплоты. Определите тепловой эффект Q реакции:
C6H12O6 + 6O2 = 6CO2 + 6H2O+Q
1)156,4 Кдж 2)1564 Кдж 3)281,5 Кдж 4)2815,2 Кдж
11. Как называется термодинамический процесс, протекающий при V=const
1) изобарный 2) изохорный 3) изотермический 4) адиабатный
12. Какие параметры характеризуют стандартные условия:
1) 0ºC; 101325Па 2) 10ºС; 101325Па 3) 25ºС; 101325Па 4)0ºС; 101325Па
Задача №1.
Сколько теплоты выделится при растворении 200 грамм 38% HCl в 400 см3 воды. (Q(HCl)раст=(50,1n/n+1)+22,5) кДж/моль)
1)284,2кДж 2)142,1 кДж 3)68,25 кДж 4)136,5 кДж
Задача №2.
Определить изменение энтропии ∆S и ∆G при стандартных условиях для реакции
Fe3O4 (кр)+ CO(г) = 3FeO(кр) + CO2(г)
возможно ли протекание реакции при стандартных условиях?
1)возможно 2)не возможно 3)возможно при любых условиях







 2)
2)  3)
3) 4)
4)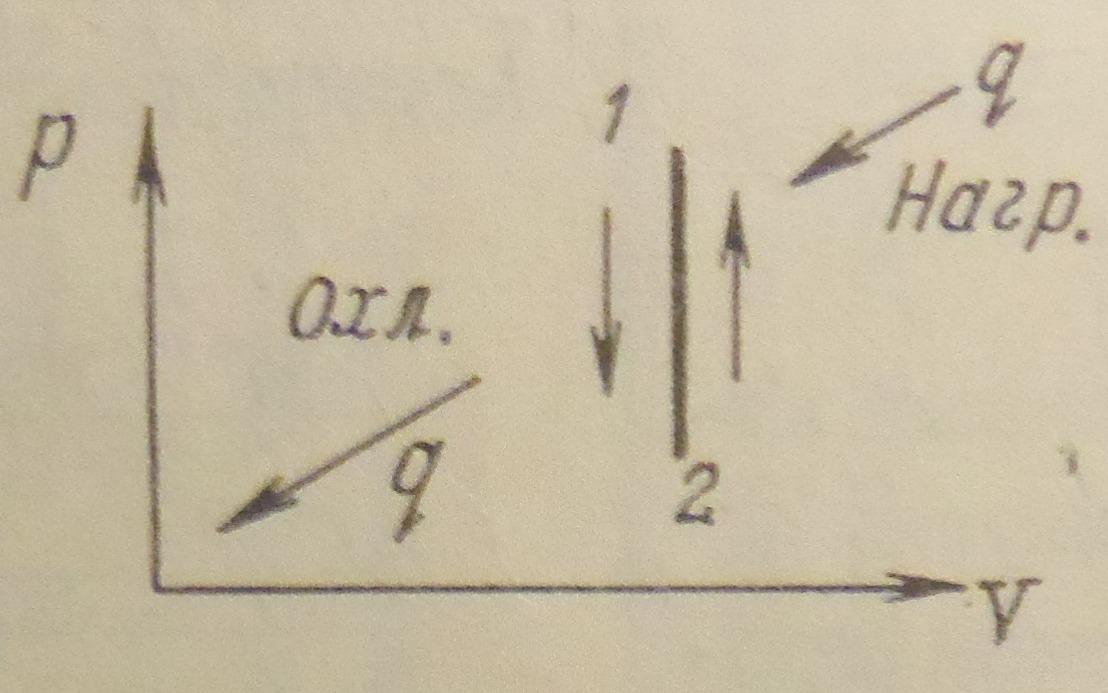 2)
2)  3)
3)  4)
4) 










