
Урок химии в 8 классе
Переведите с химического языка на общепринятый, следующие выражения:
1. Не всё то АУРУМ, что блестит.
2. ФЕРРУМНЫЙ ХАРАКТЕР.
3. Слово- АРГЕНТУМ, а молчание- АУРУМ.
4. За КУПРУМНЫЙ грош удавится.

ЗАДАНИЕ 1.
Дайте название химическому элементу
C
Ag
Mg
Si
Al
S
P
Mn
Cu
Zn
Ca
O
Na
Fe
Cl
K
H
N
Сейчас на экране будут появляться знаки химических элементов. Четко и правильно проговаривай название и произношение химического элемента. Желаю тебе удачи!

ЗАДАНИЕ 2.
Вспомним математику: правила округления
П равила округления:
- если после запятой стоит цифра меньше 5, то число остается без изменения.
- если после запятой стоит цифра 5 или больше 5 , то число увеличивается на единицу.
Примеры:
Рb
Ag
207, 19
107, 868
А r (Pb) = 207
А r (Ag) = 108
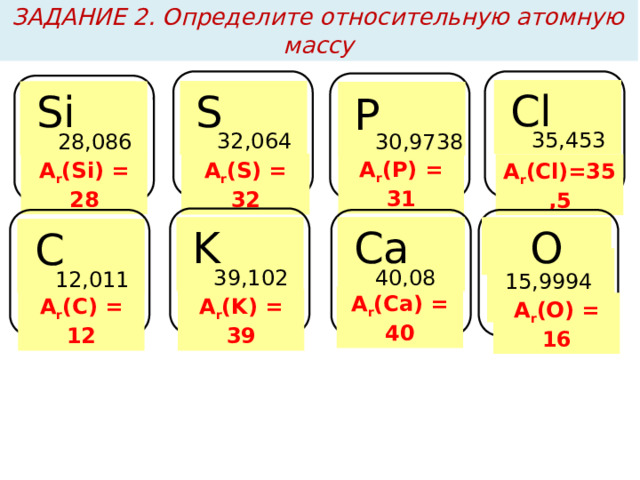
ЗАДАНИЕ 2. Определите относительную атомную массу
Cl
S
Si
P
35,453
32,064
28,086
30,9738
А r (P) = 31
А r (Si) = 28
А r (S) = 32
А r (Cl)=35,5
O
K
Ca
C
40,08
39,102
12,011
15,9994
А r (Ca) = 40
А r (C) = 12
А r (K) = 39
А r (O) = 16

ЗАДАНИЕ 3. Установите соответствие между названием химического элемента, положением в Периодической системе и его символом:
Ответ:
1) В, б;
2) Г, г
3) Б, а
4) А, в
ЗАДАНИЕ 4. Химические элементы расположены в порядке увеличения относительных атомных масс в рядах:
Ответ:
3)
5)
4
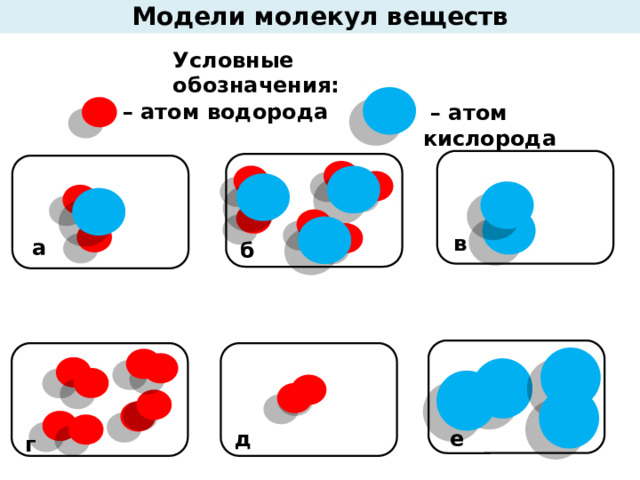
Модели молекул веществ
Условные обозначения:
– атом водорода
– атом кислорода
в
а
б
Водород
д
е
г

Химические формулы. Относительная молекулярная масса.

Цель:
- научиться понимать, записывать и читать химические формулы веществ;
- познакомиться с понятием «относительная молекулярная масса вещества» и научиться рассчитывать ее по химической формуле.
Основные понятия:
1. Химические формулы
2. Индексы и коэффициенты
3. Относительная молекулярная масса ( М r )

ЗАДАНИЕ 5. Переведите текстовую информацию в символическую.
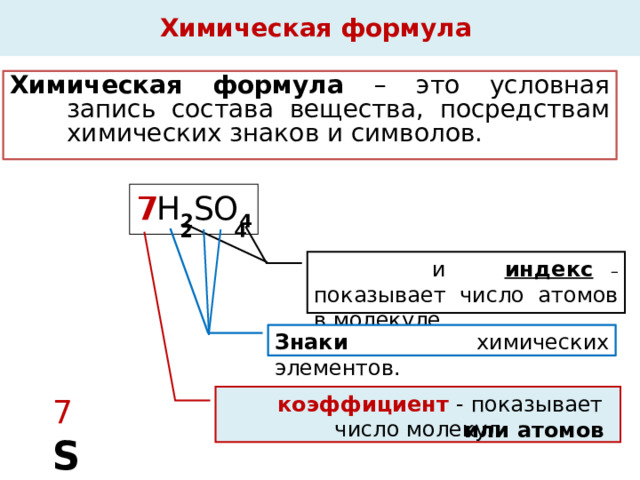
Химическая формула
Химическая формула – это условная запись состава вещества, посредствам химических знаков и символов.
7 H 2 SO 4
7
4
2
и индекс – показывает число атомов в молекуле.
Знаки химических элементов.
коэффициент - показывает число молекул
7 S
или атомов
4

Какую информацию несет формула вещества?
Качественный состав:
в состав молекулы воды входят атомы водорода и кислорода, значит вода – сложное вещество.
H 2 O
Количественный состав:
одна молекула воды содержит два атома водорода и один атом кислорода

ЗАДАНИЕ 5. Переведите текстовую информацию в символическую.
2О 3
7S
5 SО 2
3Fe

Практическое задание 6.
Соберите шаростержневые модели молекул:
- метана , если известно, что в состав его молекулы входят один атом углерода и четыре атома водорода,
- водорода , если известно, что в состав его молекулы входят два атома водорода;
- запишите их формулы и определите молекулярные массы.
Подсказка. Из атомов складываются молекулы, а из относительных атомных масс - относительные молекулярные массы (Mr).

Относительная молекулярная масса М r
Из атомов складываются молекулы, а из относительных атомных масс - относительные молекулярные массы (Mr).
Величина, которая показывает, во сколько раз масса молекулы больше 1/12 массы атома углерода, называют относительной молекулярной массой ( М r )
12 + 1 · 4 = 16
Аr(Н) · 4 =
Аr(C) +
Mr (CН 4 ) =
Mr ( Са(ОН) 2 ) =
40 + 32 + 2 =
74
+ 1 · 2 =
+16 · 2
40
Mr ( СаCО 3 ) =
100
16 · 3 =
12 +
40 +
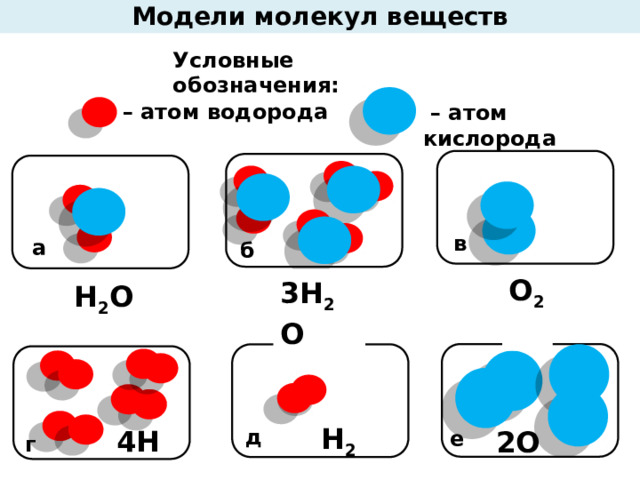
Модели молекул веществ
Условные обозначения:
– атом водорода
– атом кислорода
в
а
б
О 2
3Н 2 O
Н 2 O
Водород
Н 2
4Н 2
2О 2
д
е
г

Составляем формулы
Составьте формулу сахара , если известно, что в состав его молекулы входят (по порядку) двенадцать атомов углерода, двадцать два атома водорода и одиннадцать атомов кислорода
Составьте формулу поваренной соли , если известно, что в ее состав входят один атом натрия и один атом хлора
Составьте формулу пищевой соды , если известно, что в ее состав входят один атом натрия, один атом водорода, один атом углерода и три атома кислорода
С 12 Н 22 O 11
NaНСO 3
NaCl
сахар
соль
сода

Самостоятельная работа «Построй фигуру»
17
16
36
36,5
37
16
32
4
55
34
44
48
18
20
2
22
21
10
28
30
6-я точка
7-я точка
М r (HCl) =
8-я точка
М r (CH 4 ) =
9-я точка
М r (O 3 ) =
10-я точка
М r (CO 2 ) =
11-я точка
М r (CO) =
12-я точка
М r (N 2 ) =
М r (H 2 O) =
1-я точка
2-я точка
М r (H 2 S) =
3-я точка
М r (H 2 ) =
4-я точка
М r (O 2 ) =
5-я точка
М r (NH 3 )
М r (HF) =
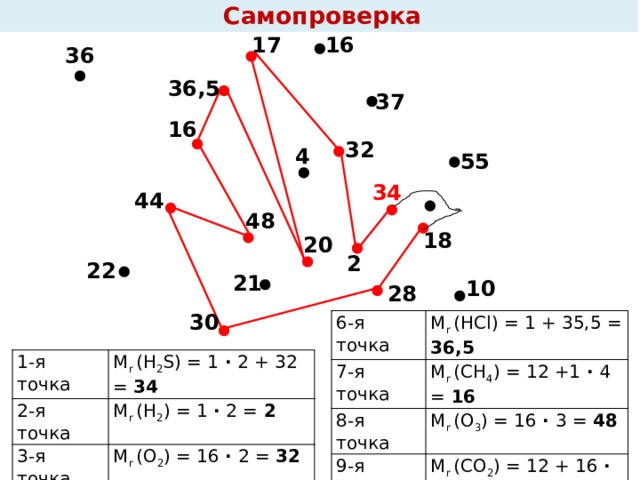
Самопроверка
17
16
36
36,5
37
16
32
4
55
34
44
48
18
20
2
22
21
10
28
30
6-я точка
7-я точка
М r (HCl) = 1 + 35,5 = 36,5
8-я точка
М r (CH 4 ) = 12 +1 ∙ 4 = 16
9-я точка
М r (O 3 ) = 16 ∙ 3 = 48
10-я точка
М r (CO 2 ) = 12 + 16 ∙ 2 = 44
11-я точка
М r (CO) = 14 + 16 = 30
12-я точка
М r (N 2 ) = 14 ∙ 2 = 28
М r (H 2 O) = 1 ∙ 2 + 16 = 18
1-я точка
2-я точка
М r (H 2 S) = 1 ∙ 2 + 32 = 34
3-я точка
М r (H 2 ) = 1 ∙ 2 = 2
4-я точка
М r (O 2 ) = 16 ∙ 2 = 32
5-я точка
М r (NH 3 ) = 14 + 1 ∙ 3 = 17
М r (HF) = 1 + 19 = 20

Домашнее задание:
Все: §14 прочитать, упр.1,4 (устно), упр. 3 (п);
На выбор: упр. 5 (п)

Оцените свою работу на уроке

Чтение химических формул (если останется время)
Примеры:
- NH 3 – молекула эн аш три состоит из одного атома азота и трех атомов водорода.
2. Al(OH) 3 – молекула алюминий о аш трижды состоит из одного атома алюминия , трех атомов кислорода и трех атомов водорода .
Аl 2 ( SO 4 ) 3
P 2 O 5
Ca(OH) 2
(NH 4 ) 3 PO 4
AgNO 3
Fe 2 O 3
C 8 H 18
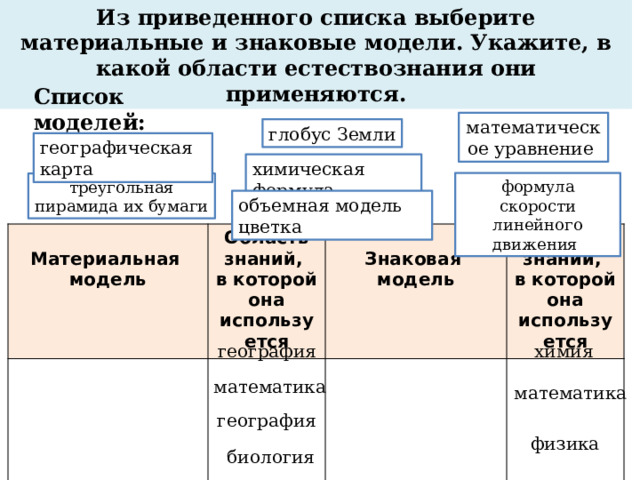
Из приведенного списка выберите материальные и знаковые модели. Укажите, в какой области естествознания они применяются.
Список моделей:
математическое уравнение
глобус Земли
географическая карта
химическая формула
формула скорости линейного движения
треугольная пирамида их бумаги
объемная модель цветка
Материальная
Область знаний,
модель
в которой она используется
Область знаний,
Знаковая
модель
в которой она используется
география
химия
математика
математика
география
физика
биология













































