ХИМИЯ
ПЛАН УРОКА 13
Тема урока: Фенолы. Состав, строение, свойства, получение и применение
Обучающая цель: изучить состав, строение, свойства фенола, рассмотреть зависимость взаимного влияния атомов в молекуле фенола на его свойства, познакомить учащихся с физическими и химическими свойствами фенола, изучить качественную реакцию на фенол, рассмотреть применение фенола и его соединений, их биологическую роль
Воспитательная цель: формирование коммуникативных качеств, культуры общения; формирование интереса к изучаемому предмету; стимулирование любознательности, активности на уроке; развитие работоспособности
Развивающая цель: продолжать развивать умение наблюдать, анализировать, делать выводы при выполнении химического эксперимента
Методическая цель: повышение интереса учащихся к изучению химии через применение интерактивной доски
Междисциплинарные связи: биология
Внутридисциплинарные связи: тема «Углеводороды», тема «Спирты»
Тип урока: урок - изучения новых знаний
Оснащение урока: компьютер, проектор, учебный модуль по теме занятия, растворы С6Н5ОН, чая, парацетамола, FeCl3, пробирки, резиновые пробки.
ХОД УРОКА
I ОРГАНИЗАЦИОННЫЙ МОМЕНТ – проверка присутствующих, вопросы о готовности группы к уроку, постановка целей урока
Здравствуйте, ребята!
Сегодня у нас необычный урок. Настройтесь на волну успеха и у нас с вами всё получится.
II АКТУАЛИЗАЦИЯ ЗУН И ПРОВЕРКА ДОМАШНЕГО ЗАДАНИЯ
Ребята, скажите, пожалуйста, состав, строение и свойства каких веществ мы изучали на предыдущих занятиях?
1. Блиц – опрос:
Насыщенные одноатомные спирты –это …
Общая формула насыщенных одноатомных спиртов …
Название спирта образуют от …
Спиртам характерна изомерия …
Число изомерных спиртов состава С3Н8О равно … и их формулы …
При межмолекулярной дегидратации спиртов образуются …
При внутримолекулярной дегидратации спиртов образуются …
Древесный спирт –
Винный спирт –
Чрезвычайно ядовитое вещество, 5 -10 мл вызывает слепоту …
Ядовитое наркотическое вещество, систематическое употребление его напитков приводит к циррозу печени –
Многоатомные спирты –
1,2,3 пропантриол (формула) –
Этиленгликоль(формула) –
Качественной реакцией для многоатомных спиртов является …
2. Сообщения о применении многоатомных спиртов ксилита и сорбита.
III ИЗЛОЖЕНИЕ НОВОГО МАТЕРИАЛА
План:
Строение фенола
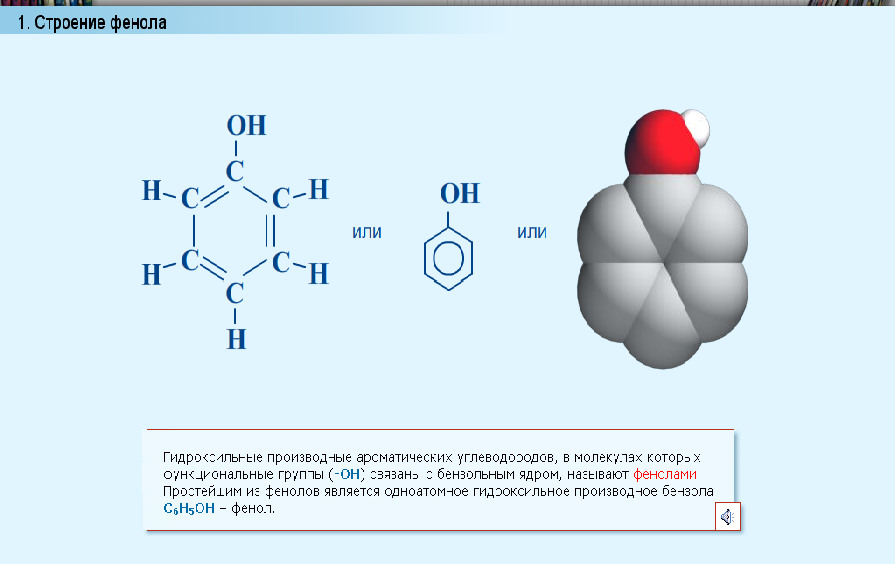
Физические свойства

Химические свойства
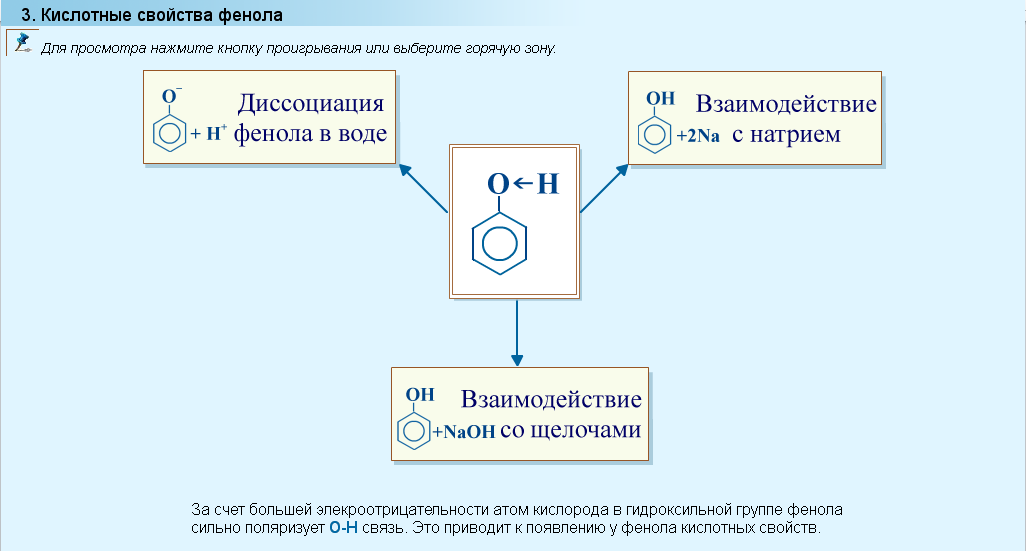
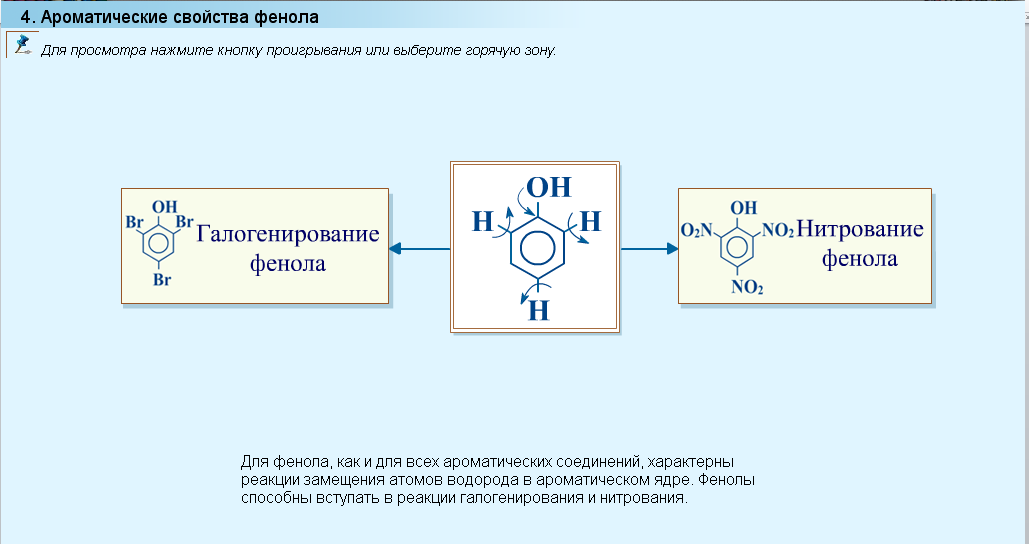
Реакция с бромной водой используется как качественная реакция на фенол.
Но кроме этой реакции качественной реакцией на фенол является реакция с раствором хлорида железа (III).
Опыт № 1 «Взаимодействие фенола с раствором хлорида железа (III)»
В чистую пробирку налить 2 – 3 мл раствора фенола и добавить 2 – 3 капли FeCI3.
Что произошло? Почему изменилась окраска? Сделайте вывод.
Опыт № 2 « Определение танина в холодной заварке чая»
В чистую пробирку налить 2 – 3 мл холодной заварки чая и добавить 2 – 3 капли FeCI3.
Что произошло? Почему изменилась окраска? Сделайте вывод.
Опыт № 3 «Определение фенола в парацетамоле».
В чистую пробирку налить 2 – 3 мл воды и поместить полтаблетки парацетамола .
Встряхнуть пробирку, чтоб таблетка растворилась. Добавить 2-3 капли FeCI3.
Что произошло? Почему изменилась окраска? Сделайте вывод.
Способы получения (работа с учебником)
Применение фенола
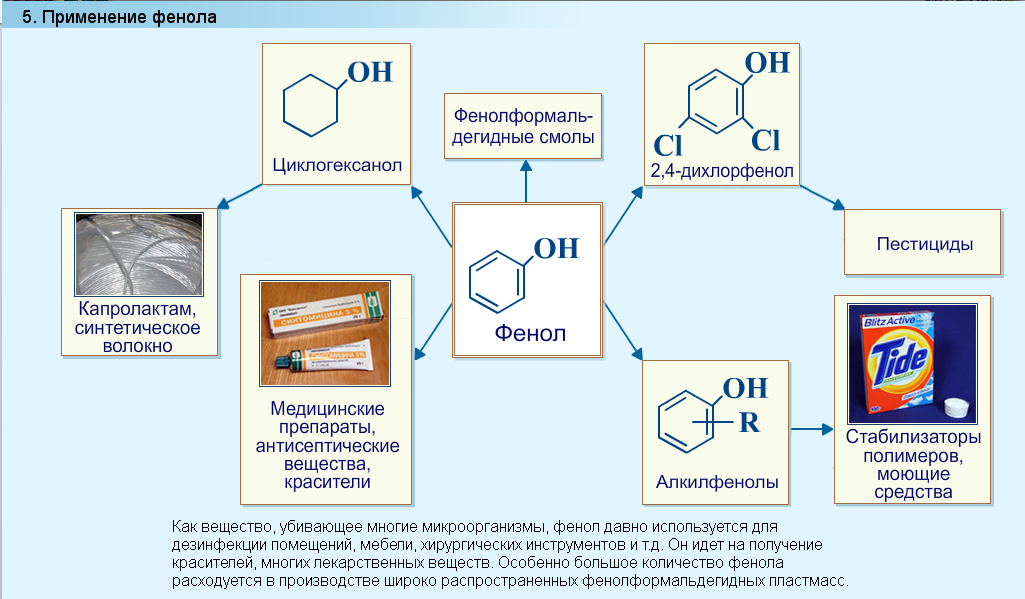
Биологическая роль
Фенол обладает и другими свойствами. Вот как их описывает А.П. Чехов в произведении “Враги”:
“… По случаю дифтерита вся прислуга еще с утра была выслана из дому. Кирилов, как был, без сюртука, в расстегнутой жилетке, не вытирая мокрого лица и рук, обожженных карболкой, пошел сам отворять дверь…”
О каких свойствах идет речь? (Фенол способен вызывать ожоги и является антисептиком).
В рассказе “Письмо” А.Чехов пишет такие строки:
“ … Вчера я так увлекся книгой, что даже не обрадовался приезду Травникова, которого я люблю. Он приехал ко мне с головной болью и не в духе. После больших операций у него всегда болит голова — отравляется парами карболовой кислоты….”
О каких свойствах идет речь? ( Фенол – токсичное вещество).
Фенол - ядовит!!! При попадании на кожу вызывает ожоги, при этом он всасывается даже через неповрежденную кожу и вызывает отравление. Но вместе с тем, раствор фенола используют в качестве дезинфицирующего средства (карболовая кислота). Двухатомные фенолы применяют как антисептики (антибактериальные обеззараживающие вещества).
Биологическая роль соединений фенола:
| Положительная | Отрицательная (токсическое действие) |
лекарственные препараты (пурген, парацетамол) антисептики (3-5 % раствор – карболовая к-та) эфирные масла (обладают сильными бакте-рицидными и противовирусными свойствами, стимулируют иммунную систему, повышают артериальное давление: - анетол в укропе, фенхеле, анисе - карвакрол и тимол в чабреце - эвгенол в гвоздике, базилике | пестициды, гербициды, инсектициды загрязнение вод фенольными отходами |
IV ЗАКРЕПЛЕНИЕ
1. Фронтальный опрос в виде игры «Да-нет»
Если утверждение правильное, то учащиеся говорят «да», если неправильное, то «нет».
Фенолы – это производные спиртов, в молекулах которых есть гидроксильная группа (нет)
Фенол является тугоплавким веществом (нет)
Формула фенола – С6Н5NH2 (нет)
Фенол при доступе воздуха розовеет (да)
При взаимодействии фенола со щелочами, получаются феноляты (да)
Фенол – газообразное вещество, с резким запахом (нет)
Фенолы – производные аренов (да)
Фенол является сильной кислотой (нет)
Фенол называют карболовой кислотой (да)
Из фенолов можно получить лекарства (да)
Фенол получают только из каменноугольной смолы
Из фенола получают пикриновую кислоту (да)
Фенол представляет собой бесцветные кристаллы (да)
При взаимодействии фенола с натрием, получают этилаты (нет)
Фенол не является антисептиком (нет)
Растворимость фенола в воде хорошая (нет)
Фенолы с одной гидроксогруппой называются одноатомными (да)
Все фенолы имеют бензольное ядро (да)
2. Осуществите следующие превращения:
а) СН4 С2Н2 С6Н6 С6Н5CI C6H5OH 2,4,6-трибромфенол
б) СН4 CH3CI C2H6 C2H5CI C3H8 C3H7CI C6H14 C6H6 C6H5CI C6H5OH пикриновая кислота
3. Тестовое задание по теме «Спирты. Фенолы»
1. Вещество, формула которого СН3СН2ОН, относится к
а) одноатомным спиртам б) фенолам
в) альдегидам г) многоатомным спиртам.
2. Гомологами являются
а) метанол и глицерин б) метанол и бутанол-1
в) уксусный альдегид и ацетон г) фенол и этанол.
3. Изомерами являются:
а) метанол и этанол б) фенол и гексанол-1
в) ацетон и уксусный альдегид г) бутанол и 2-метилпропанол-2.
4. Водородная связь отсутствует между молекулами:
а) одноатомных спиртов б) углеводородов в) гликолей
г) трехатомных спиртов.
5. Реакцией Кучерова можно получить:
а) этаналь б) этанол в) глицерин г) фенол.
6. С чем взаимодействует фенол в отличие от этанола:
а) с металлическим натрием б) с гидроксидом натрия
в) с азотной кислотой г) с карбоновыми кислотами
7. Образование белого осадка с бромной водой является качественной реакцией на:
а) фенол б) глицерин в) метанол г) этиленгликоль.
8. Образование ярко- синего комплексного соединения с гидроксидом меди (II) является качественной реакций на:
а) альдегиды б) многоатомные спирты в) фенолы г) кетоны.
9. Что общего в строении молекул одноатомных и многоатомных спиртов?
10. Для этилового спирта характерны:
А) хорошая растворимость в воде
Б) наличие π - связи в молекуле
В) пагубное действие на организм человека
Г) горение на воздухе
Д) реакция гидрирования
Е) реакция полимеризации.
(Проверка ответов Теста – КЛЮЧ на доске.)
КЛЮЧ 1- а; 2 – б; 3 – г; 4 – б; 5 – а; 6 – б; 7 – а; 8 – б.
9- функциональная группа –ОН; 10 – А, В, Г.
V ПОДВЕДЕНИЕ ИТОГОВ РАБОТЫ
Комментирование и выставление отметок
VI ВЫДАЧА ДОМАШНЕГО ЗАДАНИЯ
[2] §27-28, стр. 141 в. 4,5






















