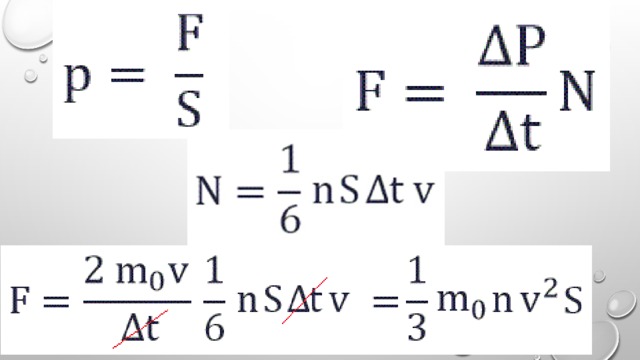Просмотр содержимого документа
«Идеальный газ в МКТ. Основное уравнение МКТ»

ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ ПОВТОРИМ
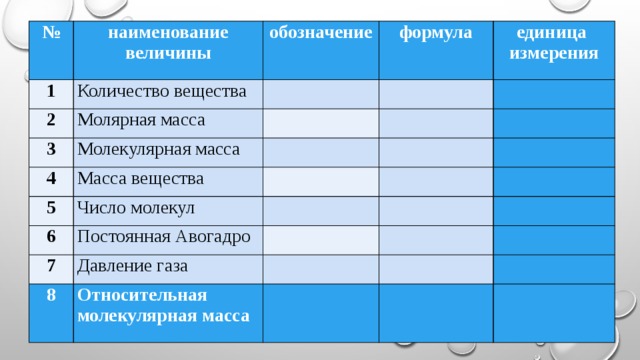
№
1
наименование величины
Количество вещества
2
обозначение
формула
Молярная масса
3
Молекулярная масса
4
единица
измерения
5
Масса вещества
Число молекул
6
7
Постоянная Авогадро
8
Давление газа
Относительная молекулярная масса

- Что такое молекулярно-кинетическая теория? Сформулируйте ее основные положения.
- Какие наблюдения и эксперименты подтверждают основные положения молекулярно-кинетической теории?
- Что называют броуновским движением? Каковы его особенности?
- Что называют диффузией? Приведите примеры диффузии в газах, жидкостях и твердых телах.
От чего зависит скорость диффузии? О чем свидетельствует явление диффузии?

- Что называют количеством вещества? Какая формула выражает смысл этого понятия? Какова единица количества вещества? Сформулируйте определение этой единицы.
- Что называют постоянной Авогадро? Чему она равна?
- Что такое молярная масса вещества? Какая формула выражает связь молярной массы вещества с числом Авогадро? Какова единица молярной массы?

Решите задачи
Вариант №1.
Вариант №2.
- 1.Сколько молекул содержится в 1 г углекислого газа?
- 2.Определите молярную массу и массу одной молекулы кислорода?
- 1.Определите молярную массу и массу одной молекулы поваренной соли?
- 2.Сколько молекул содержится в 1 кг водорода ?

Идеальный газ в МКТ. Основное уравнение МКТ газа
10 класс
Базовый уровень

Как понять слово ИДЕАЛЬНЫЙ?
- нереальный , не существующий в действительности
нереальный ,
воображаемый
безупречный , совершенный
реальный ,
существующий ,
действительный

Идеализация – метод научного познания, прокладывает путь к решению трудных задач.
- Идеальный газ – это простейшая физическая модель настоящего газа.
- Идеальный газ состоит из огромного числа частиц, которые уподобляют шарикам (материальным точкам), имеющим конечную массу, и у которых отсутствует объем.

Модель идеального газа
- Расстояние между молекулами больше размеров молекул
- Молекулы – упругие шары
- Силы притяжения стремятся к нулю.
- Отталкивание – только при ударах
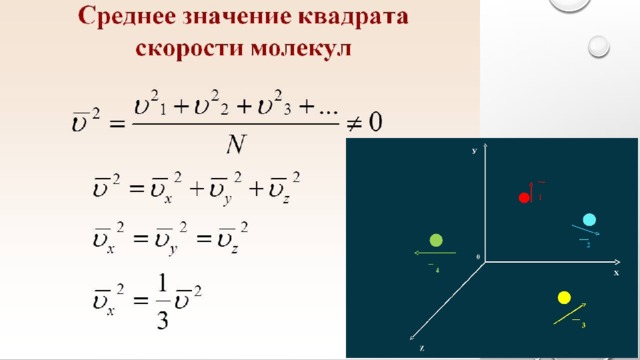
- Движение отдельно взятой молекулы
– по законам Ньютона.
- Движения в разные стороны равноправны.
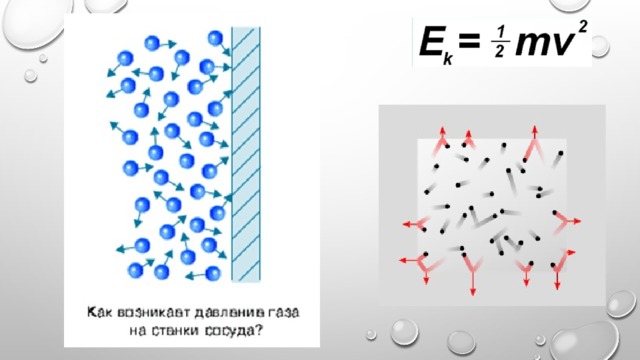

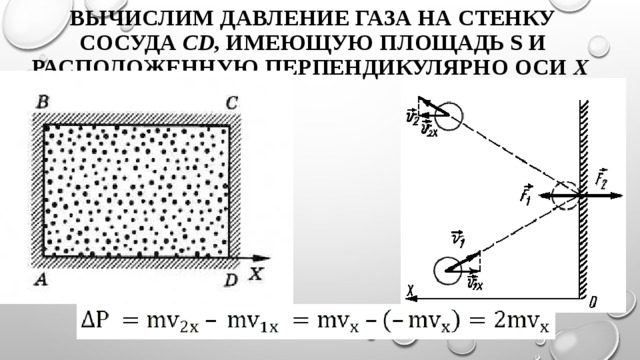
Вычислим давление газа на стенку сосуда CD, имеющую площадь S и расположенную перпендикулярно оси X

- Поскольку в каждом из шести основных направлений декартовой системы координат (вверх, вниз, вперед, назад, вправо, влево) движется одна шестая часть частиц N/6. Тогда число частиц, которые сталкиваются с каждой стенкой за время Δt равно:
S – площадь этой стенки
n - концентрация частиц
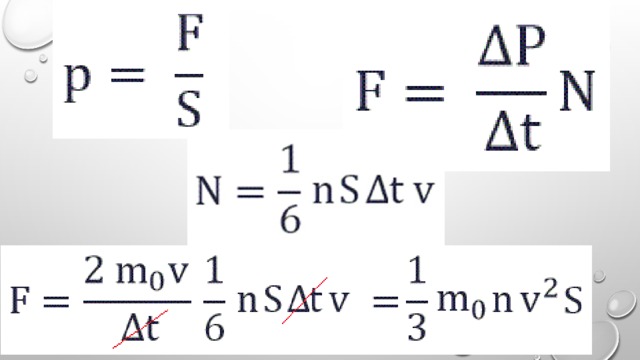

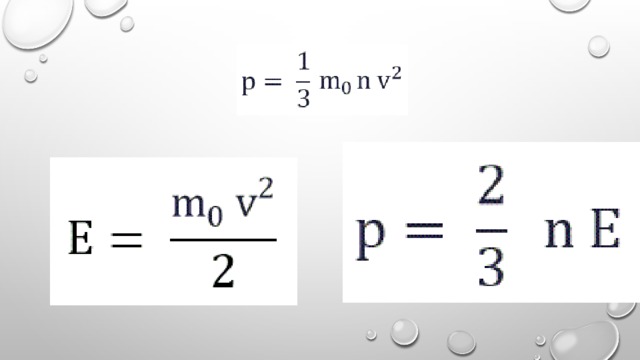

ПРОВЕРИМ СЕБЯ


ТЕСТ
1. Давление газа на стенку сосуда обусловлено
А. притяжением молекул друг к другу
Б. столкновениями молекул со стенками сосудов
В. столкновением молекул газа между собой
Г. проникновением молекул сквозь стенки сосуда
2. Как изменилось давление идеального газа, если в данном объеме скорость каждой молекулы газа увеличилась в 2 раза, а концентрация молекул осталась без изменения?
А. увеличилось в 2 раза
Б. увеличилось в 4 раза
В. уменьшилось в 2 раза
Г. уменьшилось в 4 раза

3. При повышении температуры идеального газа в запаянном сосуде его давление увеличивается. Это объясняется тем, что с ростом температуры...
А. увеличиваются размеры молекул газа
Б. увеличивается энергия движения молекул газа
В. увеличивается потенциальная энергия молекул газа
Г. увеличивается хаотичность движения молекул газа
4. Как изменится концентрация молекул газа при уменьшении объема сосуда в 2 раза?
А. увеличится в 2 раза
Б. уменьшится в 2 раза
В. не изменится
Г. уменьшится в 4 раза
5. При уменьшении температуры средняя кинетическая энергия молекул
А. увеличится
Б. уменьшится
В. не изменится
Г. иногда увеличится, иногда уменьшится

ОТВЕТЫ
1 - Б, 2 – Б, 3 – Б, 4 – А, 5 – Б
ДОМАШНЕЕ ЗАДАНИЕ В ЭЛЕКТРОННОМ ДНЕВНИКЕ
УДАЧИ!