
МОУ «Степанщинская средняя общеобразовательная школа»
Презентация к интегрированному уроку
для 8-9 классов
«Удивительные свойства воды»

Цель:
- Расширение и углубление знаний учащихся о воде, влиянии человека на гидросферу, о глобальных экологических проблемах, расширение кругозора учащихся, развитие познавательного интереса к предметам естественнонаучного цикла .
Задачи:
- Показать учащимся, что вода – уникальное природное соединение, активная среда жизни;
- Обобщение знаний о физических, химических и аномальных свойствах воды;
- Раскрыть роль воды в природе и в жизни человека, пути рационального использования водных ресурсов;
- формирование деятельностных компетенций экономного водопользования на основе интеграции предметных знаний в учебной и внеклассной работе;
- Активизация познавательной деятельности учащихся, самостоятельного мышления, умения применять полученные знания на практике;
- Формирование коммуникативных компетенций и культуры общения.

Вода, у тебя нет ни вкуса, ни цвета, ни запаха, тебя невозможно описать, тобой наслаждаются, не ведая, что ты такое! Нельзя сказать, что ты необходима для жизни! Ты сама жизнь! Ты наполняешь нас радостью, которую не объяснить нашими чувствами… Ты самое большое богатство на свете…»
Антуан де Сент- Экзюпери

Самое уникальное и удивительное вещество в природе
… Все хорошо в природе, но вода – красота всей природы!
С.Т.Аксаков

Вода – самое распространенное неорганическое соединение на нашей планете
Океан, покрывающий почти всю нашу планету, на котором миллион лет назад зародилась жизнь – это вода. Тучи, облака, туманы, роса, несущие влагу всему живому на земной поверхности, -- это тоже вода. Бескрайние ледяные пустыни полярных областей, снеговые покровы, застилающие почти половину планеты, -- и это вода.

Открытие состава воды
состоящее из 11% водорода
и 89% кислорода.
принимали воду за простое вещество.
- В 1783 году Г. Кавендиш обнаружил, что горючий воздух (водород)и 1,5 часть обыкновенного воздуха при
сгорании дают воду;
- Опыты по синтезу и разложению
воды провел французский химик
А.Лавуазье.

Общий запас воды на Земле составляет 1359000 м 3 . Около 70% поверхности планеты покрыто морями и океанами, но эта вода – соленая. На долю пресной воды приходится 2,8%, причем 2,2% из них недоступно людям, так как это ледники северного Ледовитого океана, Гренландии, Антарктиды.
Почему же одно из бесчисленных химических соединений с простой и ничем не примечательной формулой Н 2 О, состоящее их двух обычных для мироздания химических элементов – кислорода и водорода, самая обычная, всем известная вода занимает столь особое место в жизни природы? Чем объясняется такая исключительная роль воды?

На первый взгляд, вода кажется очень простым соединением, состоящим из атомов водорода и кислорода. На самом деле это самое аномальное вещество в мире.
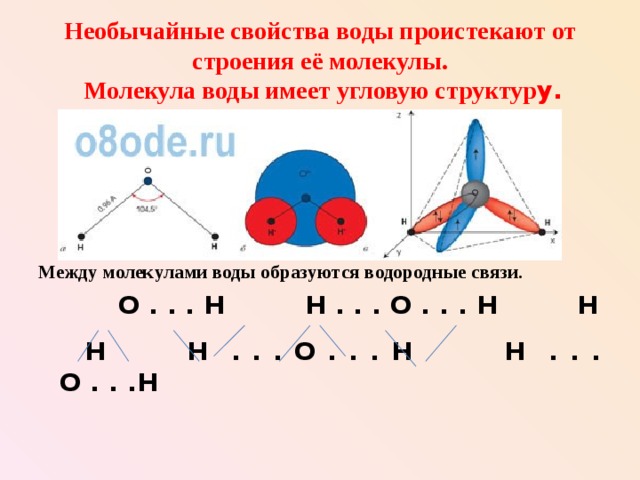
Необычайные свойства воды проистекают от строения её молекулы. Молекула воды имеет угловую структур у.
Между молекулами воды образуются водородные связи.
О . . . Н Н . . . О . . . Н Н
Н Н . . . О . . . Н Н . . . О . . .Н

Аномальные свойства воды
Вода имеет высокие температуры плавления и кипения. Вода кипит при 100 ⁰ С.Температуры кипения различных веществ не случайны. Сравним между собой одинаковые по составу химические соединения различных элементов, принадлежащих к одной и той же группе Периодической системы химических элементов Менделеева. Легко заметить, что чем меньше атомная масса элемента, тем ниже температура кипения его соединений .
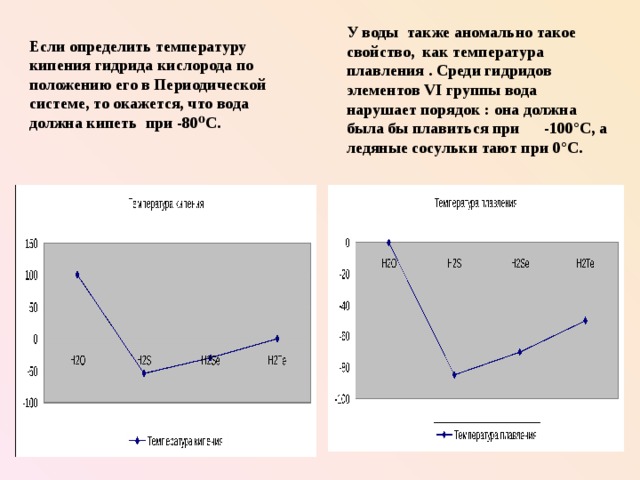
У воды также аномально такое свойство, как температура плавления . Среди гидридов элементов VI группы вода нарушает порядок : она должна была бы плавиться при -100°С, а ледяные сосульки тают при 0°С.
Если определить температуру кипения гидрида кислорода по положению его в Периодической системе, то окажется, что вода должна кипеть при -80 ⁰ С.
2 O
2 O
2 S
2 S
2 Se
2 Se
2 Te
2 Te

- Следовательно, вода кипит приблизительно на 180 ⁰ С выше, чем должна кипеть. Температура воды – это наиболее обычное её свойство оказывается необычайным .
- Если бы температура кипения воды была -80 ⁰ С, чтобы тогда случилось на нашей Земле?
- Океаны внезапно закипели бы. На Земле не осталось бы ни одной капли, и на небе никогда не смогло бы появиться ни одного облачка.

- Жидкая вода имеет самую высокую теплоёмкость среди всех жидкостей – 4,19 кДж / кг*град.
- При нагревании теплоемкость веществ, как правило, возрастает, но от 0 до 37 С теплоемкость воды падает, достигая минимального значения около 37 С, а от 37 до 100 С начинает подниматься.
- В организме человека при температуре 36,6 -37 С наиболее интенсивно идут важнейшие биохимические реакции.
- Благодаря высокой теплоемкости воды Мировой океан не дает Земле летом перегреваться, а зимой – переохлаждаться.

Вода и аномальное поверхностное натяжение 0,073 Н/м2 при 20°С .
- Меч из воды Струя химически чистой воды сечением 1 см2 по прочности на разрыв не уступает стали того же сечения. Водную струю как бы цементирует сила поверхностного натяжения. Поведение воды в капиллярах подчиняется и более сложным физическим закономерностям. Ходить по воде... Благодаря пленке некоторые предметы, будучи тяжелее воды, не погружаются в воду. Многие насекомые (водомерки, ногохвостки и др.) не только передвигаются по поверхности воды, но взлетают с нее и садятся, как на твердую опору. Более того, живые существа приспособились использовать даже внутреннюю сторону водной поверхности. Личинки комаров повисают на ней с помощью несмачиваемых щетинок, а маленькие улитки – прудовики и катушки – ползают по ней в поисках добычи.

Аномальная плотность воды
- Плотность воды достигает максимального значения при 4 С. Охлаждаясь до этой температуры, вода уменьшается в объеме, а при дальнейшем понижении температуры от 4 С до 0 С расширяется. Так не ведет себя ни одно другое вещество. Причина этого – все те же водородные связи.
- .

Попробуем вообразить, как выглядел бы мир, если бы вода обладала нормальными свойствами
- Зимой, незамерзающий сверху более плотный лед тонул бы в воде, непрерывно опускаясь на дно водоема. Летом лед, защищенный толщей холодной воды, не мог бы растаять.
- Постепенно все озера, пруды, реки промерзли бы нацело, превратившись в гигантские ледяные глыбы. Наконец, промерзли бы моря, а за ними и океаны. Наш прекрасный цветущий мир стал бы сплошной ледяной пустыней, кое-где покрытый тонким слоем талой воды.

Вода, как первоначальный источник жизни и ее непременный атрибут, поскольку именно в ней появились и эволюционировали все живые существа



Загрязнение воды

Последствия кислотных дождей

Вода – ключ к жизни.

Литература
- « Я познаю мир» Детская энциклопедия, Химия / Автор-составитель Л. А. Савина, Москва, АСТ,1996
- О. В. Недогибченко «Химические стихи и сказки», НГПУ, НИПКиПРО, Новосибирск,2002
- В. В. Синюков «Вода известная и неизвестная», Москва, Знание, 1987
- К. С. Лосев «Вода», Ленинград, 1989
5. Резников К.М. Вода жизни //Прикладные информационные аспекты медицины. – 2001. – Т.4. - №2. С.3-10.
6. Вилле Герман Гайнц «Чудесный мир воды»
Ссылки
- http://kleman.chat.ru
- http://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%B0
- http://att-vesti.narod.ru/J30-0.HTM














































