Спецификация
контрольных измерительных материалов
для проведения контрольной работы по Химии в 10 классе (общий уровень)
по теме «Ненасыщенные углеводороды»
Назначение КИМ – оценить уровень общеобразовательной подготовки по химии учащихся 10 класса. КИМ предназначены для промежуточного контроля достижения планируемых предметных и метапредметных результатов.
Промежуточная работа содержит задания с выбором ответа, с кратким ответом и развернутым ответом.
К каждому заданию части 1 с выбором ответа предлагается четыре варианта ответа, из которых один правильный.
В части 2 работы представлены задания с кратким ответом: задания на установление соответствия. Ответ на задания части 2 записывается в виде последовательности цифр.
В части 3 работы представлены задания, ответы на которые записываются учащимися самостоятельно в развернутом виде.
Количество заданий части 1 – 12 заданий, части 2 – 3 задания, части 3 – 2 задания
Время выполнения работы 45 минут
Правильно выполненная работа оценивается 27 баллами.
Каждое задание части 1 с выбором ответа оценивается 1 баллом.
Каждое задание части 2 оценивается 2 баллами.
Первое задание части 3 оценивается 5 баллами, задание 2 – 4 баллами.
Таблица перевода баллов в отметки по пятибалльной шкале
| Отметка | «2» | «3» | «4» | «5» |
| Первичный балл | 0-7 | 8-15 | 16-23 | 24-27 |
Продолжительность работы 45 минут
| № | Проверяемый элемент | Тип задания | Балл |
| Часть 1 |
| 1 | Классификация углеводородов | ВО | 1 |
| 2 | Изомерия углеводородов | ВО | 1 |
| 3 | Строение молекул углеводородов | ВО | 1 |
| 4 | Изомерия углеводородов | ВО | 1 |
| 5 | Свойства алкинов | ВО | 1 |
| 6 | Получение аренов | ВО | 1 |
| 7 | Свойства алкадиенов | ВО | 1 |
| 8 | Свойства углеводородов | ВО | 1 |
| 9 | Свойства алкенов | ВО | 1 |
| 10 | Взаимосвязь между углеводородами | ВО | 1 |
| 11 | Свойства алкадиенов | ВО | 1 |
| 12 | Получение алкинов | ВО | 1 |
| Часть 2 |
| 13 | Классификация углеводородов | КО | 2 |
| 14 | Химические свойства углеводородов | КО | 2 |
| 15 | Характеристика способов получения углеводородов | КО | 2 |
| Часть 3 |
| 16 | Реакции, подтверждающие взаимосвязь органических веществ | РО | 5 |
| 17 | Нахождение молекулярной формулы вещества | РО | 4 |
Контрольная работа по химии
10 класс
Ненасыщенные углеводороды
Часть 1
| При выполнении заданий 1–12 обведите кружком номер выбранного ответа в работе. |
Общая формула алкадиенов
1)CnH2n 2) CnH2n+2 3) CnH2n-2 4) CnH2n-4
Этилен и пропен являются
1) изомерами 3) одним и тем же веществом
2) гомологами 4) разными веществами
Валентный угол и длина связи в молекуле этилена соответственно равны
1) 120° и 0,120нм 3) 180° и 0,134нм
2) 109°28´и 0,154нм 4) 120° и 0,134нм
Изомером углеводорода, формула которого
СН≡С ─ СН ─ СН3,
│
СН3,
является
1) бутин-2 3) 2-метилбутен-2
2) 3-метилбутен-1 4)2-метилбутадиен-1,3
Бутин-2 может взаимодействовать с
1) HNO3 2)Br2 3) Ag2O(аммиач.р) 4) С2Н5ОН
Бензол может быть получен в реакции
1) Лебедева 2) Зелинского 3) Вюрца 4) Кучерова
Какие из приведенных утверждений об алкадиенах и их свойствах верны?
А. Для алкадиенов характерны реакции присоединения, полимеризации и окисления
Б. Бутадиен-1,2 используют для получения каучуков
1)верно только А 3)верны оба утверждения
2)верно только Б 4) оба утверждения неверны
Бромную воду обесцвечивают оба вещества в ряду
бутин-1 и бутан 3) изопрен и пропан
гексан и полиэтилен 4) бутин-2 и бутен-2
Какие вещества Х1 и Х2 надо взять, чтобы осуществить следующие превращения
С2Н5Cl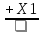 →C2H4
→C2H4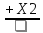 →C2H4Cl2
→C2H4Cl2
1) NaOH, HCl 2) Na, HCl 3) NaOH, Cl2 4) Na, Cl2
В схеме превращений
1-хлорпропан  Х1
Х1 Х2
Х2
веществами Х1 и Х2 соответственно являются
1) пропен и 2-бромпропан 3) пропан и 1-бромпропан
2) пропин и 1-бропрмпропан 4) пропен и 2-бромпропан
Мономером для производства каучука является
1)бутадиен-1,2 3) 2-метилбутадиен-1,3
2) бутен-2 4) 2 -метилпентадиен-1,4
Ацетилен может быть получен гидролизом
1) карбида кальция 3) карбида алюминия
2) карбоната кальция 4) метана
Часть 2
| При выполнении заданий 13–15 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы. Цифры в ответе могут повторяться. |
Соотнесите формулу вещества и класс углеводородов
Формула
А. С2Н2
Б. С2Н4
В. С4Н6
Г. С2Н6
Класс
Алканы
Алкены
Алкадиены
Алкины
Циклоалканы
Соотнесите исходные вещества и продукты реакции
Исходные вещества
А. СН3-СН=СН2+HCl
Б. СН3-С≡СН+H2O
В. СН3-СН=СН2+Cl2
Г. СН3-С≡СН+2НCl
-
-
Продукты реакции
СН3-СН2- СН2Cl
СН3-СН Cl – СН3
СН3-СН2- СOH
СН3-СO- СН3
СН3-СНCl- СН2Cl
СН3-СCl2- СН3
Соотнесите способ получения и углеводород
Способ получения
А. С3Н7ОН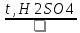 →
→
Б. СН3-СНCl-СН2Cl +2KOH→
В. C3H8→2H2+
Г. СН3-СНCl-СН2Cl+Zn
Углеводород
Пропен
Циклопропан
Пропин
Пропадиен
Часть 3
Составьте уравнения, необходимые для следующего превращения
-
CaC2→C2H2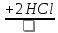 →X1
→X1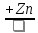 →X2
→X2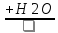 →X3
→X3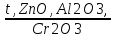 →X4
→X4
-
-
Алкадиен массой 2,04г может полностью обесцветить 384г раствора бромной воды с массовой долей 2,5%. Установите молекулярную формулу алкадиена. Приведите возможную структурную формулу алкадиена, если известно, что он является мономером для получения каучука.
Ответы:
Часть 1
1 | 3 |
2 | 2 |
3 | 4 |
4 | 4 |
5 | 3 |
6 | 2 |
7 | 1 |
8 | 4 |
9 | 3 |
10 | 1 |
11 | 3 |
12 | 1 |
Часть 2
13 | 4,2,3,1 |
14 | 2,4,5,6 |
15 | 1,3,3,1 |
Часть 3
16 | Ответ содержит пять уравнений реакций: СаС2+2Н2О→С2Н2+Са(ОН)2 С2Н2+2HCl→Cl-CH2-CH2-Cl Cl-CH2-CH2-Cl+Zn→CH2=CH2+ZnCl2 CH2=CH2+Н2О→CH3CH2OH 2 CH3CH2OH→CH2=CH-CH=CH2+2H2O+H2 За каждое правильно составленное уравнение – 1 балл -
|
17 | Составить уравнение: CnH2n-2+2Br2→CnH2n-2Br4 Найти массу брома в растворе и его количество вещества: m(Br2)=m(p-p)*ω=384*0,025=9,6(г) n(Br2)=m/M M(Br2)=160г/моль n(Br2)=9,6/160=0,06(моль) по уравнению n(CnH2n-2)= ½ n(Br2)=0,03(моль) Найти молярную массу алкадиена М=m/n=2,04/0,03=68(г/моль) Выразить молярную массу алкадиена по формуле М=12n+2n-2 12n+2n-2=68 14n=70 n=5 значит, молекулярная формула алкадиена С5Н8 т.к. по условию алкадиен при полимеризации образует каучук, то алкадиен имеет сопряженные двойные связи. Структурная формула, которая может соответствовать алкадиену составом С5Н8 может быть изопрен (2-метилбутадиен-1,3) СН2=С(СН3)-СН=СН2 |
-






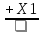 →C2H4
→C2H4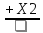 →C2H4Cl2
→C2H4Cl2 Х1
Х1 Х2
Х2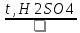 →
→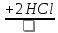 →X1
→X1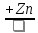 →X2
→X2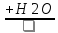 →X3
→X3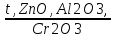 →X4
→X4









