Просмотр содержимого документа
«"Качественное определение катионов и анионов", ресурс для 9, 11 классов»

Качественные реакции.
Качественные реакции – это реакции обнаружения катионов, анионов, отдельных веществ в различных образцах.
Они составляют основу химического анализа.

Обнаружение хлорид-аниона
Реактив - бесцветный раствор соли нитрата серебра - AgNO 3
NaCl + AgNO 3 = AgCl ↓ + NaNO 3
Ag + + Cl - = AgCl ↓
Выпадает
белый осадок
Хлорида серебра.

Обнаружение Молекулярного йода
Реактив - раствор, содержащий крахмал 0
J 2 + крахмал → тёмно-синий
раствор
Тёмно-синее
окрашивание
раствора.
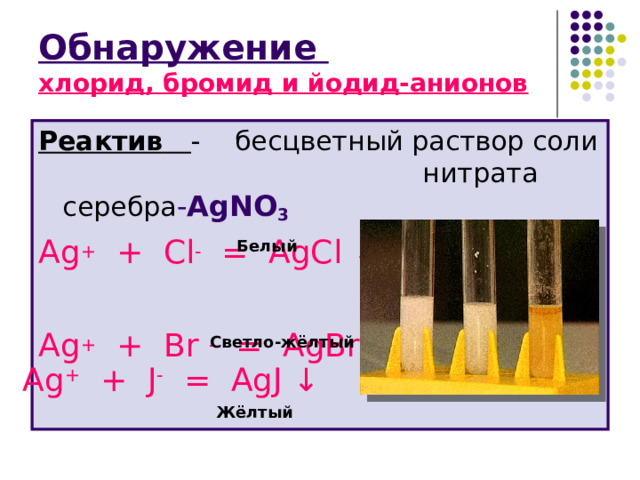
Обнаружение хлорид, бромид и йодид-анионов
Реактив - бесцветный раствор соли нитрата серебра - AgNO 3
Ag + + Cl - = AgCl ↓
Ag + + Br - = AgBr ↓
Белый
Светло-жёлтый
Ag + + J - = AgJ ↓
Жёлтый

Обнаружение фосфат-аниона
Реактив - бесцветный раствор соли нитрата серебра - AgNO 3
Na 3 PO 4 + 3 AgNO 3 = Ag 3 PO 4 ↓ +3 NaNO 3
3 Ag + + РО 4 3 - = Ag 3 РО 4 ↓
Выпадает
жёлтый осадок
Фосфата серебра.

Обнаружение сульфат-аниона:
Реактив - бесцветный раствор соли бария, например хлорида - BaCl 2
BaCl 2 + Na 2 SO 4 = BaSO 4 ↓ + 2NaCl
Ba 2+ + SO 4 2- =BaSO 4 ↓
Выпадает
белый осадок
Сульфата бария.

Обнаружение карбонат-аниона
Реактив - бесцветный раствор любой сильной кислоты
N а 2 CO 3 + 2HCl = 2NaCl + CO2 ↑ + H 2 O
СО 3 2- + 2Н + = СО 2 ↑ + Н 2 О
Происходит выделение
углекислого газа.

Обнаружение катиона железа (2+)
Реактив - бесцветный раствор щелочи
Fe SO 4 +2NaOH = Fe(OH) 2 ↓ + Na 2 SO 4
Fe 2+ + 2ОН - = Fe (ОН) 2 ↓
Происходит выпадение
темно-зелёного
осадка
гидроксида железа( II) .

Обнаружение катиона железа (3+)
Реактив - бесцветный раствор щелочи
FeCl 3 + 3 KOH = Fe ( OH ) 3 ↓+ 3 KCl
Fe 3+ + 3ОН - = Fe (ОН) 3 ↓
Происходит выпадение
бурого осадка
гидроксида железа( III) .

Ещё способ обнаружения катиона железа (3+)
Реактив - бесцветный раствор роданида калия - KSCN
Fe 3+ + 3 SCN - = Fe ( SCN ) 3
Раствор окрашивается
в тёмно-красный
цвет,
образуется
роданид железа( III) .
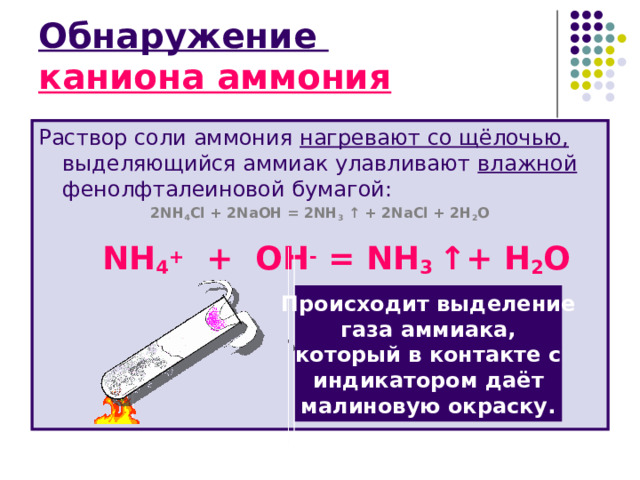
Обнаружение каниона аммония
Раствор соли аммония нагревают со щёлочью, выделяющийся аммиак улавливают влажной фенолфталеиновой бумагой:
2NH 4 Cl + 2NaOH = 2NH 3 ↑ + 2NaCl + 2H 2 O
NH 4 + + O Н - = NH 3 ↑+ Н 2 О
Происходит выделение
газа аммиака,
который в контакте с
индикатором даёт
малиновую окраску.


































