Химический состав клетки
В состав клетки входят неорганические, органические вещества и химические элементы.
Химические элементы делятся на 3 группы:
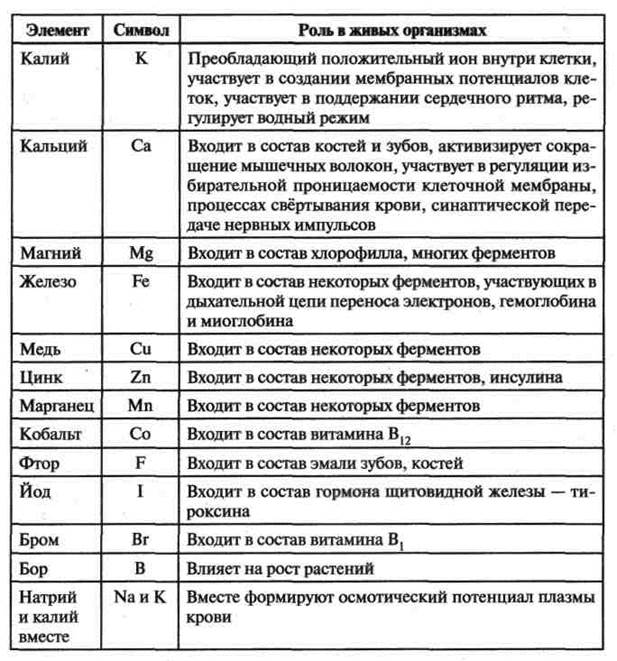
Макроэлементы (кислород, азот, углерод, водород, калий, натрий, кальций железо, сера, фосфор, магний)
Микроэлементы (бор, кобальт, медь, цинк, бром, йод, молибден)
Ультрамикроэлементы (уран, цезий, радий, золото, цезий, селен, бериллий, ртуть).
Неорганические вещества: вода и минеральные соли (анионы и катионы).
Органические вещества: белки, углеводы, жиры, ферменты, АТФ, нуклеиновые и органические кислоты.

Из всех веществ, входящих в состав клетки, наибольшее количество приходится на воду и белки.

Из химических элементов более 98% приходятся на кислород, водород, азот, углерод.

Среди веществ клетки на первом месте стоит вода (75-85%). Высокое содержание воды - важнейшее условие деятельности клетки. При потере воды клетки и организмы гибнут. Молекула воды электронейтральна, дипольна. Атомы водорода имеют положительный заряд, атом кислорода – отрицательный. Дипольность молекулы воды способствует присоединению к различным молекулам и участкам молекул, в результате образуются гидраты. Способностью образовывать гидраты обусловлены ее универсальные растворяющие свойства.
В зависимости от притяжения молекул воды к молекулам других веществ они делятся на 2 группы: гидрофильные и гидрофобные. Гидрофильными называются вещества, хорошо растворимые в воде (соли, щелочи, спирты, кислоты). Гидробными называются вещества, плохо растворимые или нерастворимые в воде (древесина, жиры, металл, пластмассы, каучук, бензин, масла).
Роль воды в клетке: Является растворителем веществ, непременным участником всех химических реакций. Вода обладает высокой теплоемкостью и теплопроводностью, что важно для поддержания теплового равновесия в клетке. Вода – среда для протекания реакций, служит источником кислорода, выделяемого при фотосинтезе и водорода, необходимого для восстановления продуктов ассимиляции углекислого газа. Вода – средство передвижения веществ в организме (ток крови, лимфы, токи растворов по сосудам у растений. С ее помощью удаляются вредные вещества из клетки. Участвует в образовании смазывающих жидкостей и слизей, соков в организме, создает влажную среду слизистых оболочек и органов.
Минеральные соли обеспечивают буферные свойства клетки. Буферность – это способность клетки сохранять опредеренную концентрацию водородных ионов (рН). В клетке поддерживается слабощелочная реакция – ( рН 7,2).
Катионы калия и натрия участвуют в деятельности кальциево-натриевого насоса, обеспечивающего буферность клетки. Фосфат кальция входит в состав костной ткани, в раковины моллюсков, обеспечивая прочность этих образований.
Значение химических элементов заключается в том, что они участвуют в построении организма и участвуют в химических реакциях.
Органические вещества клетки. Белки
Белки - это высокомолекулярные органические соединения, в состав которых входят атомы углерода, кислорода, водорода, азота, серы, фосфора. Белки иначе называются протеинами или пептидами. От сырой массы клетки они составляют 10-20%.остав которых входят атомы углерода, кислорода. енияя. .ислоты. 000000000000000000000000000000000000000000000000000000000000000
Белки - это нерегулярные полимеры, мономерами которых являются аминокислоты. В состав белков входят 20 природных альфа – аминокислот. Разнообразие белков зависит от количества и состава аминокислот, входящих в молекулу и порядком их чередования в полипептидной цепи.
Каждая аминокислота состоит из аминогруппы NH2 и карбоксильной группы CООН, которые одинаковы у всех аминокислот. Третьей составной частью является радикал, лежащий вне этих групп. Именно радикалом отличаются аминокислоты друг от друга. Синтез новых белков идет непрерывно из аминокислот, образующихся за счет расщепления белков пищи пищеварительными ферментами. Соединение аминокислот происходит через группировки, аминогруппа одной аминокислоты соединяется с карбоксильной группой другой аминокислоты. При их соединении выделяется молекула воды. Между аминокислотами возникает связь, называемая пептидной (ковалентной). Это самая прочная связь между аминокислотами. Соединение нескольких аминокислот называется пептидом, а соединение из большого числа аминокислот называется полипептидом. Аминокислоты бывают заменимые и незаменимые. Заменимые аминокислоты синтезируются в организме, незаменимые не образуются (лизин, триптофан, валин, тирозин, метионин, лейцин, изолейцин)
Существует 4 уровня организации белковой молекулы: первичная, вторичная, третичная, четвертичная.
Первичная структура – самая простая структура, полипептидная цепь, те нить аминокислот, расположенных в линейном порядке, связанных между собой пептидными связями.остав которых входят атомы углерода, кислорода. енияя. .ислоты. 000000000000000000000000000000000000000000000000000000000000000
Вторичная структура имеет более высокий уровень организации, когда белковая нить закручена в виде спирали, между аминогруппой одной аминокислоты и карбоксильной группой другой, образуются водородные связи. Они достаточно прочные за счет их большого количества.
Третичная структура – специфичная, сложная конфигурация, возникающая при сворачивании нити аминокислот в клубок, или фибриллу. Водородные связи, поддерживающую эту структуру слабые, образующиеся за счет гидрофобных взаимодействий между неполярными участками молекул в водной среде. Кроме гидрофобных сил, в поддержании структуры большую роль играют электростатические связи между радикалами аминокислот. Кроме того, образуются дисульфидные –S-S-связи между атомами серы.
Четвертичная структура соединение нескольких молекул белков между собой, образование глобулы. Связи слабые водородные, дисульфидные. Самая нестойкая структура.
Под влиянием различных факторов (температуры, солевого состава, радиации, давления, действия гормонов) происходит разрыв связей, структура белка его свойства изменяются, наступает денатурация.
Денатурация – процесс разрушения природной белковой структуры. Ренатурация – это процесс восстановления нарушенной структуры белка. Возможна только тогда, когда не нарушена первичная структура белка.

Большое разнообразие белков обеспечивает им выполнение множества функций.
Функции белков
Каталитическая функция: белки являются ферментами, т.е. катализаторами (ускорителями) химических реакций. Почти все ферменты являются белками, но не все белки – ферменты! ( Д.Самнер, 1926 год, выделил ферменты белков в кристаллической форме). Примеры: фермент уреаза катализирует расщепление мочевины, липаза катализирует расщепление жиров, амилаза – углеводов, пепсин, трипсин – белков)
Регуляторная (гормоны). Белки – регуляторы физиологических процессов, многие гормоны - белки (гормоны гипоталамуса и гипофиза: адренокортикотропный, тиреотропный гормоны, гормон роста, либерины, статины, инсулин, глюкагон регулируют все процессы организма. Отдельные гормоны не являются белками, это производные аминокислот (адреналин, мелатонин, триодтиронин).
Транспортная функция – Белки транспортируют вещества в организме, в крови, мембранах, цитоплазме клеток узнают и переносят гормоны, переносят ионы, аминокислоты, сахара. Гемоглобин переносит кислород в крови ко всем клеткам и углекислый газ от клеток.
Защитная функция – белки защищают организм от бактерий и вирусов, обеспечивают иммунную защиту. В лимфоидных тканях образуются антитела – защитные белки (иммуноглобулины). Антитела распознают антигены и уничтожают их. При ранении сосудов образуется тромб, в его образовании участвуют белки фибрин и фибриноген, их действия защищают организм от кровопотери.
Двигательная функция обеспечивается сократительными белками, участвующих в мерцании ресничек, биении жгутиков, движении листьев у растений. Белки актин и миозин участвуют в движениях всех мышц животных.
Строительная (структурная) функция – белки участвуют в образовании всех клеточных мембран, органоидов клетки, внеклеточных структур (волокна, волосы, сухожилия). Белки – это «кирпичик» организма.
Энергетическая функция – Белки служат источником энергии в клетке. Распад 1 грамма белков дает 17,6 кдж энергии.
Рецепторная (узнавание). Белки клеточных мембран воспринимают действие разных факторов, отличают свои белки от чужеродных.
Адгезивная функция (слипание). Образование межклеточных контактов в эпителиальной ткани, межклеточного вещества, склеивание чужеродных частиц и обезвреживание (пектин)
Органические вещества. Углеводы.
Углеводы – органические вещества, в состав которых входят атомы углерода, водорода и кислорода. Соотношение кислорода и водорода такое же, как в молекуле воды. Общая формула углеводов Сп (Н2О)п, где п – не меньше трех. Термин «углеводы» ввел в 1844 году отечественный ученый К.Шмид.
В животных клетках углеводов содержится 2 - 5%, в растительных клетках их много (клубни картофеля, семена, фрукты, ягоды). Все углеводы делятся на 2 группы: монозы или моносахариды, и полиозы (полисахариды). Полисахариды являются биополимерами. Ди-, три-, тетрасахариды составляют группу полисахаридов первого порядка (олигосахариды). Сложные сахара, в которых сахаров много называются полисахариды второго порядка. Это сложные вещества с большой молекулярной массой.
Моносахариды – это простые сахара, состоящие из одной молекулы, представляющие собой твердые кристаллические вещества, хорошо растворимые в воде, сладкие на вкус (глюкоза, фруктоза, галактоза, рибоза, дезоксирибоза, эритроза, молочная и пировиноградная кислота). Глюкоза – виноградный сахар, мономер полисахаридов, первичный источник энергии, распространенный в природе. Глюкоза регулирует осмотическое давление в клетке. Фруктоза – плодовый сахар, мономер полисахаридов, распадается быстрее, чем глюкоза. Галактоза – изомер глюкозы, входит в состав лактозы и других полисахаридов.
Олигосахариды, из них больше интересуют дисахариды: сахароза, лактоза, мальтоза.
Сахароза (глюкоза+фруктоза) - тростниковый (свекловичный) сахар), содержится в семенах, ягодах, корнях, плодах, клубнях). Формула - С12Н22О11. Важна в питании животных и человека.
Лактоза (глюкоза+галактоза) – молочный сахар, источник энергии для детенышей млекопитающих, используется в микробиологии для получения питательных сред.
Мальтоза( глюкоза+глюкоза) – основной структурный элемент крахмала и гликогена – животного крахмала.
Полисахариды второго порядка: амилоза, амилопектин, крахмал, гликоген, клетчатка (целлюлоза).
Это высокомолекулярные углеводы, состоящие из большого количества моносахаридов, не растворимы в воде, не имеют сладкого вкуса. Бывают резервного (крахмал, гликоген) и структурного назначения (клетчатка). Могут образовывать комплексы с белками (гликопротеиды) и с жирами (гликолипиды).
Крахмал – резервный полисахарид растений, имеет вид зернышек неслоистого строения, нерастворим в холодной воде, в горячей образует коллоидный раствор (клейстер). Состоит из амилозы и амилопектина. Формула (С6Н10О5)п.
Гликоген – полисахарид, содержащийся в тканях животных, грибах, дрожжах. Накапливается в печени, мышцах, сердце, является поставщиком глюкозы в кровь, участвует в превращениях углеводов в животном организме. Состоит из 30 тысяч остатков глюкозы.
Клетчатка – главный структурный компонент клеточных оболочек растений. Она нерастворима в воде, лишь набухает в ней. По своей структуре линейный полимер, поэтому определяет свойства растительных волокон.
Функции углеводов
Энергетическая – углеводы служат основным источником энергии для организма. При расщеплении 1 грамма углеводов выделяется 17,6 кдж энергии.
Структурная – углеводы входят в состав всех тканей и органов, оболочек, органоидов (межклеточное вещество соединительной ткани, клеточная стенка растений, хитин животных), принимают участие в синтезе веществ, у растений выполняют опорную функцию.
Защитная – вязкие секреты (слизи), выделяемые разными железами, богаты углеводами, которые предохраняют слизистые стенки внутренних органов от механических повреждений, от проникновения бактерий и вирусов.
Запасающая – в организме и клетках углеводы могут накапливаться в виде крахмала у растений и гликогена у животных., которые расходуются по мере потребности в энергии (гликоген печени, крахмал в клубнях и плодах).
Рецепторная – Узнавание и взаимодействие клеток одного типа (рецепторы клеток печени)
Регуляторная – фитогормоны регулируют рост и развитие растений.
Органические вещества. Липиды (жиры)
Липиды - сложные эфиры 3-х высокомолекулярных жирных кислот и трехатомного спирта – глицерина Глицерин иначе называется глицерол.
Липиды – органические соединения с различной структурой, но общими свойствами. Они нерастворимы в воде, но растворимы в органических растворителях: бензине, хлороформе, эфире. Присутствуют во всех клетках, их содержание составляет 5-15% от сухой массы. Но, жировая ткань содержит до 90% жира. Липиды состоят из атомов водорода, кислорода и углерода. Виды липидов: жиры, масла, воска, фосфолипиды. К жирным кислотам относятся олеиновая, пальмитиновая, стеариновая. Они делятся на насыщенные и ненасыщенные. Насыщенные не содержат двойные связи (пальмитиновая и стеариновая), а ненасыщенные содержат двойные связи (олеиновая). Свойства жиров определяются качественным составом и количественным соотношением жирных кислот.
Растительные жиры содержат ненасыщенные кислоты, поэтому они легкоплавкие и становятся жидкими при комнатной температуре.
Животные жиры твердые, так как состоят из насыщенных кислот. Молекула жира содержит остаток глицерина, хорошо растворимого в воде, с другой стороны содержит остатки жирных кислот, которые нерастворимы в воде. Такая особенность расположения жиров в мембранах препятствует смешиванию содержимого клетки с окружающей средой. Липиды могут образовывать соединения с фосфорной кислотой, образуются фосфолипиды, они и являются основными компонентами мембран клеток. Стероиды - это желчные кислоты, холестерол, половые гормоны, витамин Д, гиббереллины (ростовые вещества), каротиноиды (пигменты), ментол и камфора (эфирные масла растений).
Соединения липидов и углеводов называются гликолипидами, они входят в состав ткани мозга и волокон. Липопротеиды представляют соединения белков и жиров. Функции жиров:
Структурная – принимают участие в построении мембран клеток, органов, тканей, важных соединений.
Энергетическая – липиды обеспечивают 25-30% всей энергии, необходимой организму, при расщеплении 1 грамма жира выделяется 38,9 кдж энергии.
Запасающая – жиры являются «энергетическими консервами», накапливаются в подкожной клетчатке у человека, в виде капель жира внутри клетки, в составе «жирового тела» у насекомых, в горбу верблюдов, в околопочечной капсуле, жировой подушке около глаз..
Терморегуляционная - жиры плохо проводят тепло, они откладываются под кожей толстым слоем, что позволяет многим животным жить в холодной воде.
Являются источником «эндогенной (внутренней воды). При окислении 100 граммов бурого жира выделяется 107 мл воды, за счет которой могут жить пустынные обитатели (песчанки, тушканчики, верблюды).
Гормональная (регуляторная) – Многие липиды участвуют в синтезе гормонов, сами являются гормонами (эстрадиол – женский гормон, тестостерон – мужской). Простогландины регулируют сокращение мускулатуры, поддерживают тонус сосудов, регулируют центр терморегуляции.
Ферменты
Ферменты – биологические катализаторы, ускоряющие течение биохимических реакций. Почти все ферменты имеют белковую природу, но могут быть и производными аминокислот и стероидами (фосфолипидами). Делятся на группы: оксиредуктазы, трансферазы, гидролазы, лиазы, изомеразы, лигазы.
В их состав входят: апофермент – белковая часть, кофактор – компоненты молекул ферментов неорганической природы (ионы цинка и магния) и кофермент (коэнзим) - низкомолекулярные органические соединения – витамины. Витамины активируют действие ферментов.
Активный центр фермента содержит 3-12 аминокислот, расположенных в строго определенном порядке. Фермент имеет один или несколько активных центров, в которых происходит тесный контакт между молекулой фермента и специфического вещества (субстрата), на которое он действует. Пространственная конфигурация активного центра соответствует конфигурации тех веществ, с которыми фермент взаимодействует. Узнав свой субстрат, фермент взаимодействует с ним и ускоряет его превращение.
Все ферменты обладают специфичностью, каждый из них катализирует только одну определенную реакцию, действует при определенной температуре (36-38 градусов) и рН – среды (щелочной, нейтральной или кислой). Зависит от концентрации реагирующих веществ и концентрации фермента. Повышение температуры приводит к увеличению активности ферментов, но при очень высоких температурах происходит денатурация ферментов и потеря каталитической активности.
Примеры: Каталаза, расщепляет пероксид водорода на воду и кислород. Пепсин, трипсин расщепляют белки, и пептиды до аминокислот. Амилаза расщепляет крахмал до глюкозы. Синтетаза участвует в сборке белковой молекулы. Дезоксикарбоксилаза отщепляет карбоксильные группы аминокислот.
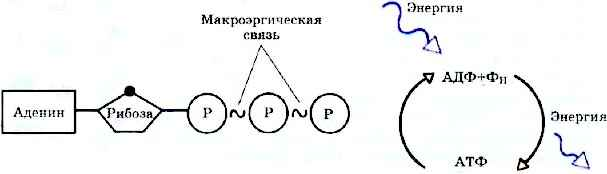
АТФ – аденозинтрифосфорная кислота
АТФ – сложное органическое соединение, содержащее две макроэргические связи (богатые энергией).
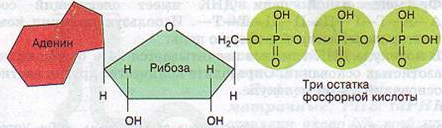
По свой структуре АТФ – нуклеотид. Она представлена одним нуклеотидом, состоящим из азотистого основания – аденина, углевода – рибозы и трех остатков фосфорной кислоты. Очень нестойкое соединение, при отделении одного остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту). Если отделяется еще один остаток, то АДФ переходит в АМФ (аденозинмонофосфорную кислоту), что бывает крайне редко. АТФ – АДФ - АМФ
Место отделившегося остатка занимает вода. Отделение каждого остатка идет с помощью ферментов, при этом выделяется 40 Кдж энергии (419кдж/моль). Именно поэтому эти связи являются макроэргическими. При синтезе АТФ энергия наоборот поглощается в большом количестве. Синтез АТФ происходит на внутренней мембране митохондрий в процессе кислородного этапа диссимиляции, поэтому их называют «энергетическими станциями клетки». Молекулы АТФ, покидая митохондрии, поступают в цитоплазму, участвуют во всех процессах и возвращаются в виде АДФ и Ф. У растений АТФ синтезируются в хлоропластах в процессе световой фазы фотосинтеза (фосфорилирование). Во всех клетках АТФ аккумулирует энергию, которая расходуется по мере надобности там, где происходят процессы с большими затратами энергии. Наибольшее количество АТФ потребляет мышечная ткань.
Энергия АТФ используется на все виды деятельности организма. Это универсальный источник энергии в клетки и организме.
Структурная формула АТФ
Аденин (азотистое основание) – Рибоза (углевод) – Фосфорная кислота (3 остатка)
А –Р- 3Н3РО4
Нуклеиновые кислоты: ДНК и РНК
Нуклеиновые кислоты – природные высокомолекулярные органические соединения, обеспечивающие хранение и передачу наследственной информации. Впервые описаны в 1869 году швейцарским ученым Ф.Мишером.. Он назвал выделенное вещество нуклеином, думая, что оно содержится только в ядрах клеток. Существует 2 вида: РНК и ДНК, которые различаются по составу, строению и функциям.
ДНК (дезоксирибонуклеиновая кислота) - молекула, обладающая большой молекулярной массой, длиной несколько тысяч нанометров. По структуре это линейный неразветвленный полимер, имеющий вид двойной правозакрученной спирали, образованной парой антипараллельных, комплементарных друг другу цепей. Пространственная структура ДНК была создана в 1953 году американскими учеными Д.Уотсоном и Ф. Криком.
Встречается в ядрах, митохондриях, хлоропластах. В ядре локализуется в хромосомах. Мономерами ДНК являются дезоксирибонуклеотиды. Каждый нуклеотид состоит из азотистого основания: пуринового (А - аденин, Г – гуанин) или пиримидинового (Т - тимин, Ц – цитозин), пятиуглеродного сахара – дезоксирибозы и фосфатной группы (фосфорной кислоты).
Примеры структурных формул ДНК:
А – Д - Ф(Н3РО4); 2) Т – Д - Ф; 3) Г – Д - Ф; 4) Ц – Д – Ф
Нуклеотиды обращены друг к другу азотистыми основаниями и объединены парами в соответствии с правилом комплементарности: напротив А (аденина) расположен Т (тимин), напротив Г (гуанина) расположен Ц (цитозин). Пара А-Т соединена двумя водородными связями, пара Г-Ц – тремя водородными связями. При репликации (удвоении) молекулы ДНК водородные связи рвутся и цепи расходятся и на каждой из них синтезируется новая цепь ДНК. Основу цепей образуют сахарофосфатные остатки. Последовательность нуклеотидов в молекуле ДНК определяет ее специфичность и специфичность белков, которые кодируются этой последовательностью. Эти последовательности индивидуальны для каждого вида организмов и отдельных особей.
Пример: дана последовательность нуклеотидов ДНК: ЦГА-ТТА-ЦАА. На информационной РНК будет синтезирована цепь: ГЦУ-УУТ-ГУУ, в результате чего выстроится цепочка аминокислот: аланин-аспарагин – валин. При замене нуклеотидов в одном из триплетов или их перестановке триплет будет кодировать другую аминокислоту, следовательно, изменится и белок, кодируемый этим геном. Изменения в составе нуклеотидов или их последовательности называется мутацией.
ДНК обладает способностью к репликации (самоудвоению) и стабильностью.
Функция: Является химической основой хромосомного генетического материала (гена), синтез ДНК и РНК, хранит информацию о структуре белков.
РНК (рибонуклеиновая кислота) - линейная одинарная полинуклеотидная цепочка. Содержится в ядре, рибосомах, цитоплазме, митохондриях, хлоропластах. Мономерами РНК являются рибонуклеотиды. Каждый нуклеотид состоит из азотистого основания: пуринового (А - аденин, Г – гуанин) или пиримидинового (У - урацил, Ц – цитозин), пятиуглеродного сахара – рибозы и фосфатной группы (фосфорной кислоты). Примеры структурных формул РНК:
А – Р - Ф (Н3РО4); 2) У – Р - Ф; 3) Г – Р - Ф; 4) Ц – Р– Ф
Свойства молекулы РНК: не способна к самоудвоению. Лабильна (изменчива). Существует несколько видов: информационная, транспортная, рибосомная, митохондриальная и пластидная, каждая из которых выполняет свою функцию:
Информационная (иРНК) – переписывает информацию с ДНК и передает генетическую информацию о первичной структуре белка к месту синтеза белка (к рибосомам). Синтезируется в ядре при участии фермента РНК- полимеразы.
Транспортная (тРНК) – транспортирует аминокислоты из цитоплазмы к месту синтеза белка. Самая маленькая молекула, состоящая из 70-90 нуклеотидов, имеющая форму клеверного листа.
Рибосомная (рРНК)- синтезируется в ядрышке и входит в состав рибосом.
Митохондриальная и пластидная (мРНК и пРНК) – входят в состав этих органоидов.
Правило ЧАРГАФФА (американский биохимик, в 1905 и 1951 годах проанализировал нуклеотидный состав ДНК и сформулировал правило комплементарности (соответствия):
Число пуриновых оснований (Аденин и Гуанин) в ДНК всегда равно числу пиримидиновых( Тимин и Цитозин), количество аденина равно количеству тимина, а количество гуанина равно количеству цитозина.
Витамины
Витамины - (от лат. vita — «жизнь») — группа низкомолекулярных органических соединений простого строения и разнообразной химической природы, необходимых для нормальной жизнедеятельности организмов, поступающие в организм в основном с пищей. Открыты в 1880 году русским ученым Н.И Луниным.
Все витамины делят на жирорастворимые — A, D, E, K, и водорастворимые — C, РР и витамины группы B. Жирорастворимые витамины накапливаются в организме (жировая ткань и печень) Водорастворимые витамины в существенных количествах не запасаются и при избытке выводятся с мочой.
Большинство витаминов не синтезируются в организме человека и полностью должны поступать с пищей. Синтезируются в организме: витамин D, который образуется в коже человека под действием ультрафиолетового света; витамин A, который может синтезироваться из предшественников, поступающих в организм с пищей; витамин B3 — ниацин, предшественником которого является аминокислота триптофан, витамины K и В7 синтезируются симбиотической бактериальной микрофлорой толстой кишки человека.
Концентрация витаминов в тканях и суточная потребность невелики, но при недостаточном поступлении витаминов в организме появляются заболевания, например цинга, бери – бери и пеллагра.
С нарушением поступления витаминов в организм связаны 3 принципиальных патологических состояния: отсутствие витамина — авитаминоз, недостаток витамина — гиповитаминоз, избыток витамина — гипервитаминоз.
Витамины являются коферментами, они выполняют каталитическую функцию в составе активных центров разнообразных ферментов. Витамины могут участвовать в гуморальной регуляции в качестве прогормонов и гормонов, участвуют в различных видах обмена веществ, но они не являются источником энергии для организма (не обладают калорийностью), не являются структурными компонентами тканей, т.е. не выполняют строительную функцию.
| Название витамина | Где содержится | На что влияет | Авитаминозы (заболевания) |
| А (ретинол) | Мясо, яйца, печень, масло, животные жиры морковь, шпинат, абрикос | Влияет на рост, развитие, зрение. Входит в пигмент родопсин | Куриная слепота – нарушение сумеречного зрения, задержка роста, сухость кожи |
| Д (кальциферол) | Рыбий жир, треска, печень, яйца. Синтезируется в коже. | Регулирует обмен кальция ми фосфора. Нужен для образования зубов и костей. | Рахит – деформация (искривление и размягчение костей) |
| Е (токоферол) | Облепиха, перец, зеленые овощи, зародыши пшеницы | Регулирует репродуктивную функцию, работу мышц | Дистрофия скелетных мышц, ослабление половой функции, импотенция, фригидность |
| К (филлохинон) | Салат, капуста, крапива, шпинат, синтезируется в кишечнике. | На процесс свертываемости крови | Снижение свертываемости крови |
| В1 | Кожура семян, отруби, бобовые, изделия из муки грубого помола | Участвует в обмене белков, жиров, углеводов, в проведении нервных импульсов | Понижение двигательной активности, «бери – бери» - железные оковы, паралич мышц |
| В2 (рибофлавин) | Яйца, сыр, молоко, мясо, дрожжи, горох, соя, фасоль, зерновые | Участвует в клеточном дыхании, влияет на ЦНС, обмен веществ, цветовое зрение | Помутнение хрусталика (катаракта), поражение слизистой оболочки рта, шелушение кожи, снижение зрения |
| В6 (пиридоксин) | Дрожжи, отруби, овощи, печень, яйца, молоко | Участвует в обмене веществ | Заболевания кожи, анемия, судороги, расстройство пищеварения |
| В9 (фолиевая кислота) | Печень, почки, салат. Синтезируется в кишечнике | Влияет на состояние сосудов | Ломкость капилляров, кровотечения |
| В12 (цианокобаламид) | Печень, продукты животного происхождения | Участвует в белковом обмене | Анемия, дегенеративные изменения нервной ткани |
| РР (никотиновая кислота) | Мясо, печень, дрожжи, отруби, зародыши пшеницы | Участвует в клеточном дыхании, работе пищеварительной системы | Пеллагра – поражение кожи, диарея, бессонница, депрессия |
| С (аскорбиновая кислота) | Цитрусовые, капуста, перец, шиповник, фрукты, ягоды | Участвует в окислительно - восстановительных реакциях, повышает устойчивость к инфекциям, укрепляет сосуды | Цинга- поражение стенок кровеносных сосудов, кровоточивость и набухание десен, вялость, ОРЗ |