Метод электронного баланса для уравнивания окислительно-восстановительных реакций

Вспомним!
Степень окисления – это условный заряд, который приобрел бы атом в молекуле, если бы все электронные пары его химических связей сместились в сторону более электроотрицательных атомов.

1. Степень окисления атомов в простых веществах равна нулю:
0 0 0
H 2 , Cl 2 , Na .
2. В сложных веществах О -2 .
3. В сложных веществах Н +1 .
4. С.О. металлов всегда положительна, максимальное значение С.О. металлов главных подгрупп обычно совпадает с номером группы, в которой расположен металл.

Алгебраическая сумма степеней окисления всех атомов в соединении всегда равна нулю:
+1 -2
H 2 SO 4
(+1)·2 + (+6)·1 + (–2)·4 = 0

В реакциях ионного обмена составные части веществ переходили в состав других веществ без изменений, степени окисления элементов и заряды ионов не менялись :
+1 +5 -2 +1 -1 +1 -1 +1 +5 -2 AgNO 3 + HCl = AgCl + HNO 3

Однако существует огромное множество реакций, в ходе которых меняются степени окисления элементов:
0 0 +2 -2
Fe + S = FeS

Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества, называют окислительно-восстановительными реакциями (ОВР) .

Элемент, отдающий электроны, называется восстановителем , а принимающий электроны - окислителем .
Процесс отдачи электронов называется окислением , а принятия - восстановлением .
В процессе окисления степень окисления повышается, в процессе восстановления - понижается.

Эти процессы неразрывно связаны между собой, число принятых окислителем электронов должно быть равно числу отданных восстановителем электронов. На этом основании составляется электронный баланс и расставляются коэффициенты.

Чтобы составить схему о-в процесса, необходимо:
1. Определить степень окисления элементов.
2. Определить элементы, изменившие степень окисления.
3. Составить схему: определить элемент, теряющий, и элемент, принимающий электроны.
4. Составить электронный баланс (число отданных электронов всегда должно равняться числу электронов, принятых).
5. Расставить коэффициенты в уравнении по электронному балансу, определить окислитель и восстановитель.
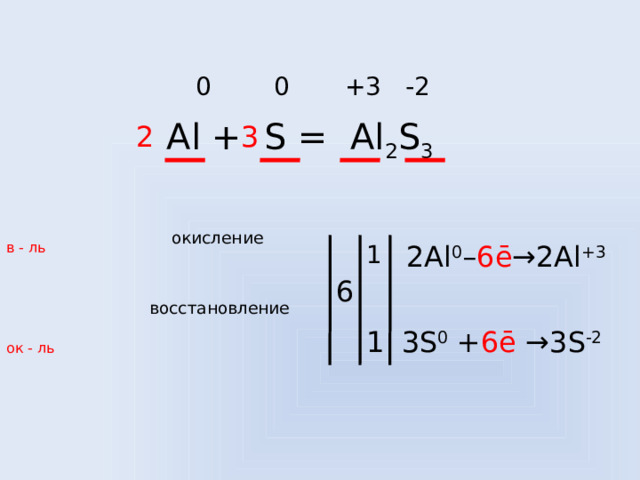
0 0 +3 -2
Al + S = Al 2 S 3
2
3
окисление
в - ль
1
2Al 0 – 6ē →2Al +3
6
восстановление
1
3S 0 + 6ē →3S -2
ок - ль
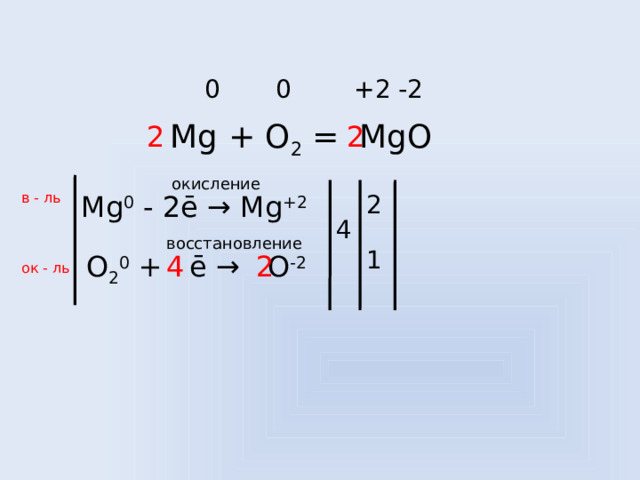
0 0 +2 -2
Mg + O 2 = MgO
2
2
окисление
2
в - ль
Mg 0 - 2ē → Mg +2
4
восстановление
1
4
2
O 2 0 + ē → O -2
ок - ль
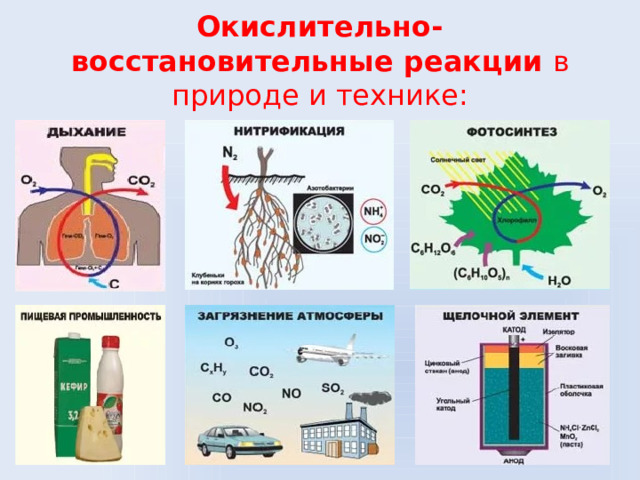
Окислительно-восстановительные реакции в природе и технике:

Задание 1.
Определите степени окисления всех химических элементов, входящих в состав веществ:
NaOH, MgCl 2 , K 2 CO 3 , AlCl 3 , H 3 PO 4 ,
K 2 SO 4 , HNO 3 , CuSO 4 , Fe, Zn(NO 3 ) 2 .

Задание 2.
Расставьте коэффициенты методом электронного баланса в следующих уравнениях реакций:
1) HgO = Hg + O 2
2) H 2 S + O 2 = SO 2 + H 2 O
3) KClO 3 = KCl + O 2
4) CuS + O 2 = CuO + SO 2
5) N 2 + H 2 = NH 3
Домашнее задание:
Расставьте коэффициенты в уравнениях методом электронного баланса:
1) Fe + Cl 2 → FeCl 3
2) Zn + HCl → ZnCl 2
3) HBr + O 2 → H 2 O + Br 2
4) NH 3 + O 2 → NO + H 2 O
5) Zn + HNO 3 → Zn(NO 3 ) 2 + N 2 + H 2 O