Просмотр содержимого документа
«Химиялык байланыш жана анын түрлөрү»

Терс электрдүүлүк
Химиялык байланыш жана анын түрлөрү

Химиялык элементтердин терс электрдүүлүгү
Эгерде элемент электронду тартып алса,анда ал элемент бир аз терс зарядга ээ болот.Анткени металл эместер бири-бири менен аракететнишкенде электрондордун биринен экинчисине жылышат(металл менеен металл эмес аракеттенишкенде электрондор бир атомдон экинчи атомго өтөт.Элемент оң жана терс заряддалат
Терс электрдүүлүк төмөн,элемент + заряддалат дельта + болуп белгиленет ∂+
Терс электрдүүлүк жогору элмент – заряддалат да “дельта -” болуп белгиленет.δ+δ-
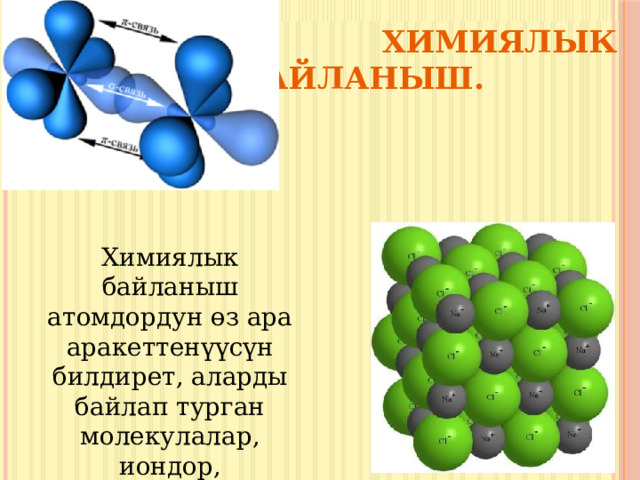
Химиялык байланыш.
Химиялык байланыш атомдордун өз ара аракеттенүүсүн билдирет, аларды байлап турган молекулалар, иондор, радикалдар,кристаллдар.
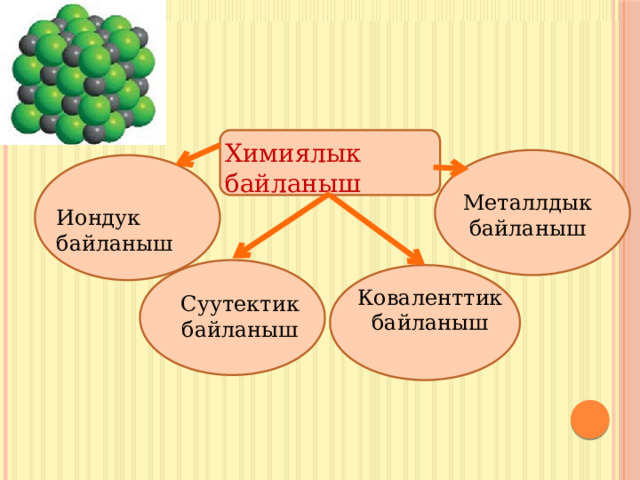
Химиялык байланыш
Иондук байланыш
Металлдык байланыш
Коваленттик байланыш
Суутектик байланыш

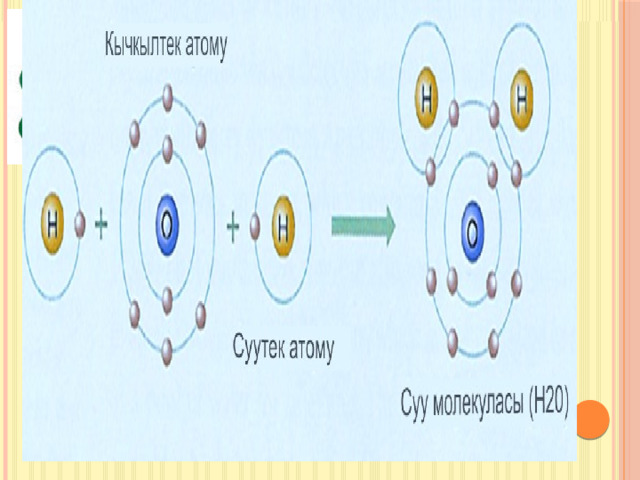
Коваленттик байланыш.
Жалпы электрондук жуптарын эсебинен келип чыккан байланыш коваленттик байланыш деп аталат.

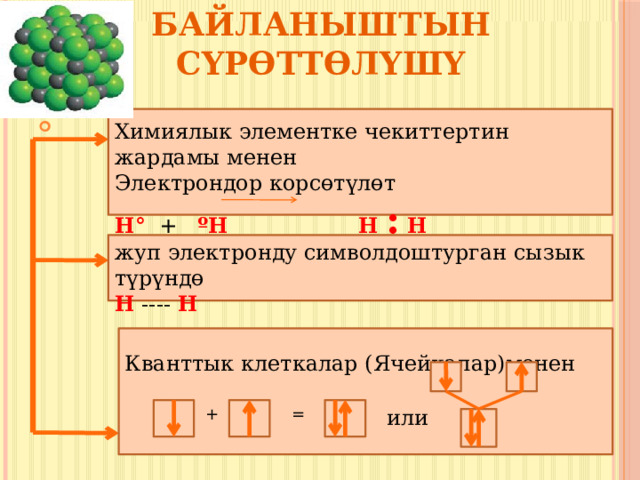
Химиялык байланыштын сүрөттөлүшү
Химиялык элементке чекиттертин жардамы менен
Электрондор корсөтүлөт
Н° + ºН Н : Н
жуп электронду символдоштурган сызык түрүндө
Н ---- Н
Кванттык клеткалар (Ячейкалар)менен
=
или
+
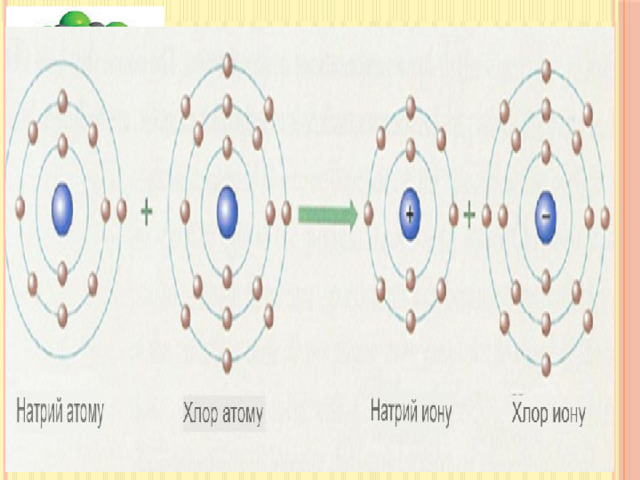
Иондук химиялык байланыш.
Иондук байланыш
Иондордун арасында электростатикалык тартылуу күчүнүн натыйжасында пайда болгон байланыш иондук байланыш деп аталат.
Иондордон пайда болгон бирикмелер иондук бирикмелер деп аталат.
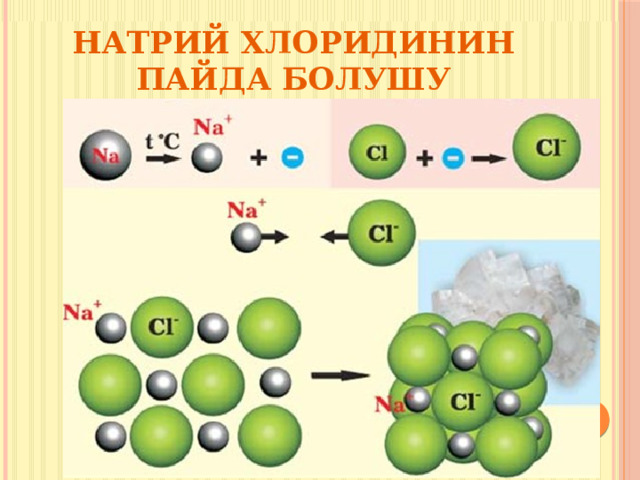
Натрий хлоридинин пайда болушу
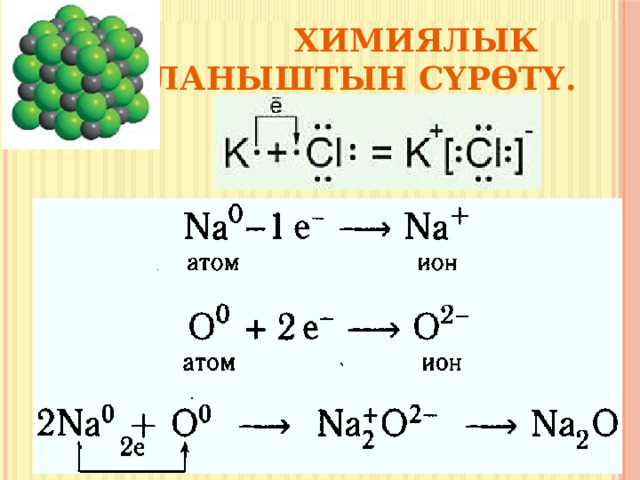
Химиялык байланыштын сүрөтү.
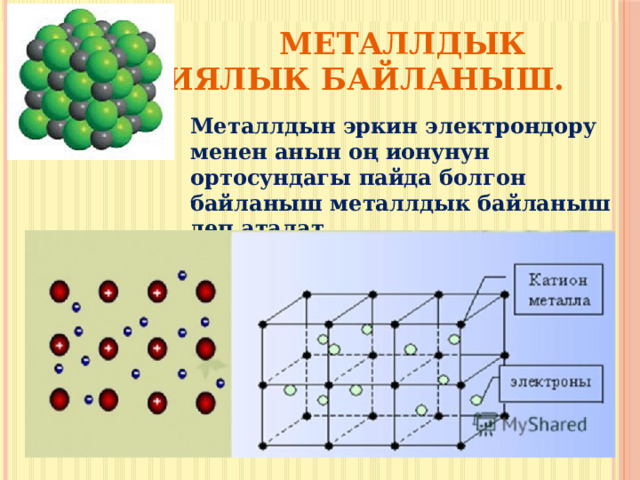
Металлдык химиялык байланыш.
Металлдын эркин электрондору менен анын оң ионунун ортосундагы пайда болгон байланыш металлдык байланыш деп аталат
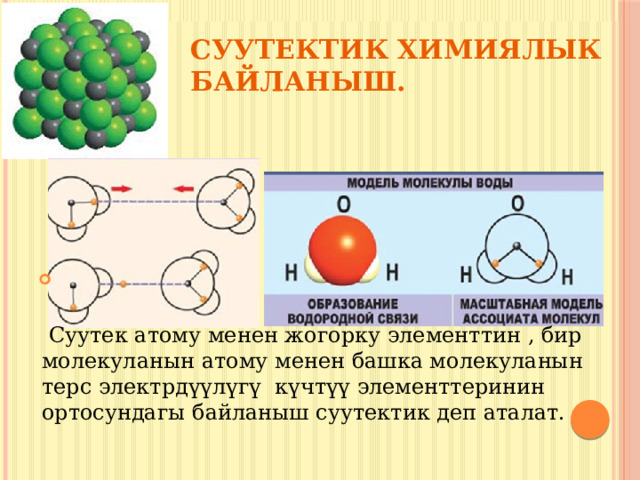
Суутектик химиялык байланыш.
Суутек атому менен жогорку элементтин , бир молекуланын атому менен башка молекуланын терс электрдүүлүгү күчтүү элементтеринин ортосундагы байланыш суутектик деп аталат.
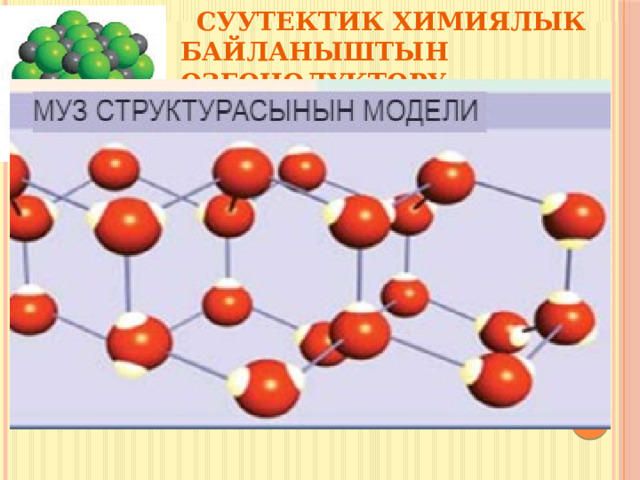
Суутектик химиялык байланыштын өзгөчөлүктөрү.
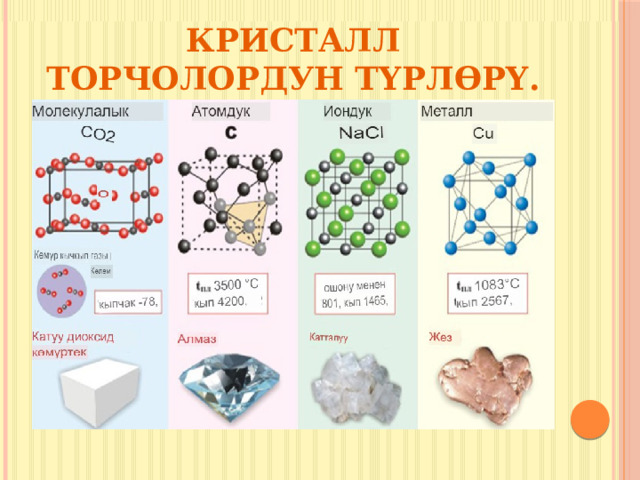
Кристалл торчолордун түрлөрү.







































