Просмотр содержимого документа
«Кейс по теме "Ковалентная связь"»
Ковалентная химическая связь
Ковалентную химическую связь образуют атомы химических элементов-неметаллов, которые имеют сравнительно небольшой радиус атома и, как правило, большое число электронов (4–7) на внешнем электронном слое. Укажите число электронов на внешнем электронном слое в атомах фтора, кислорода, азота, хлора, серы, фосфора.
Атомы элементов-неметаллов устойчивую электронную конфигурации внешнего электронного слоя (8 электронов) приобретают:
1) присоединение электронов – в случае взаимодействия с химическим элементом-металлом;
2) обобществление электронов – при взаимодействии с элементом-неметаллом.
Обратил внимание на возможность образования октета не только путем передачи электронов от одного атома другому, но и путем обобществления неспаренных электронов атомов американский химик Г. Льюис в 1916 г.
Обменный механизм возникновения ковалентной связи можно рассмотреть на примере, схемы образования химической связи меду атомами:
а) водорода и водорода
Н• + •Н → Н : Н;
б) водорода и хлора •• ••
Н • + • Cl : → Н : Cl :
•• ••
Ковалентная химическая связь – это связь, возникающая между атомами за счет образования общих электронных пар.
Общую пару электронов можно изобразить не только, используя точки, но и черточкой. Структурная формула молекулы водорода и хлороводорода будет выглядеть так:
а) H—H; б) H—Cl.
Такую формулу, в которой общая электронная пара обозначена чертой, называют структурной формулой.
Схемы взаимодействия электронных облаков атомов, образующих химическую связь:
а) 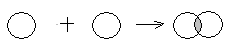

б)
Таким образом, с точки зрения современных теорий химической связи, ковалентную химическую связь следует рассматривать как результат действия сил электростатического притяжения положительно заряженных атомных ядер к электронному облаку, сконцентрированному в межъядерном пространстве.
 Донорно-акцепторном механизме образования ковалентной связи на примере образования катиона аммония: Н Н
Донорно-акцепторном механизме образования ковалентной связи на примере образования катиона аммония: Н Н
•• •• +

 H : N : + H+ H: N : H ,
H : N : + H+ H: N : H ,
• • • •
Н Н
Электроотрицательность – это способность атомов химического элемента оттягивать к себе общие электронные пары.
Схема 1 Классификация ковалентной связи по полярности
|
| Ковалентная связь |
|
| 
|
| 
|
| Ковалентная полярная связь Связь, возникающая между атомами разных элементов-неметаллов. При ее образовании происходит смещение общих электронных пар к более электроотрицательному элементу. В молекуле по линии ковалентной связи возникает два полюса – положительный и отрицательный
|
| Ковалентная неполярная связь Связь, возникающая между атомами одного и того же элемента-неметалла. При ее образовании не происходит смещение общих электронных пар. |
Ковалентная связь осуществляется не только в бинарных соединениях, но и в соединениях, образованных большим числом химических элементов.
Задания к кейсу:
I. Составьте опорный конспект по плану:
1. Природа связанных химических элементов.
2. Способ образования химической связи.
3. Механизмы образования химической связи.
4. Разновидности ковалентной связи (полярная и неполярная).
5. Примеры веществ
II. Запишите схемы образования молекул хлора, азота, метана, аммиака, углекислого газа.
Классификация ковалентной связи по полярности
|
| Ковалентная связь |
|
| 
| 
|
|
| Ковалентная полярная связь Связь, возникающая между атомами разных элементов-неметаллов. При ее образовании происходит смещение общих электронных пар к более электроотрицательному элементу. В молекуле по линии ковалентной связи возникает два полюса – положительный и отрицательный |
| Ковалентная неполярная связь Связь, возникающая между атомами одного и того же элемента-неметалла. При ее образовании не происходит смещение общих электронных пар.
|






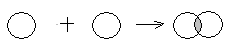

 Донорно-акцепторном механизме образования ковалентной связи на примере образования катиона аммония: Н Н
Донорно-акцепторном механизме образования ковалентной связи на примере образования катиона аммония: Н Н
 H : N : + H+ H: N : H ,
H : N : + H+ H: N : H ,