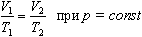Урок № 9-10
Тема: Уравнение состояния идеального газа. Газовые законы. Изопроцессы.
Цель: Организовать деятельность учащихся по анализу уравнения состояния идеального газа, применение уравнения к изопроцессам.
| задачи | Способы достижения задач |
| Организовать деятельность учащихся по анализу уравнения состояния идеального газа, применение уравнения к изопроцессам. | Составление ОК. |
| Способствовать развитию умения анализировать, обобщать полученные знания , применяя их к решению задач | Активное участие в доработке ОК. Работа с обучающей программой. |
| Способствовать развитию познавательного интереса | Восприятие материала. |
Структура урока.
| Этап урока | Деятельность учителя | Деятельность ученика |
| 1 | Физический диктант по основам МКТ. | Самостоятельная запись |
| 1 | Изложение нового материала: 1.Вывод уравнения Менделеева-Клапейрона. 2.Универсальная газовая постоянная. 3.Уравнение Клапейрона. 4.Изотермический процесс. 5.Изобарный процесс. 6.Изохорный процесс. 7.Закон Авогадро. 8. Закон Дальтона. | Составление опорного конспекта.
|
| 2 | Дом. Задание: Конспект учить. | Запись в тетрадь |
| 3. | Рефлексия изученного материала. Решение задач
| Запись в тетрадь |
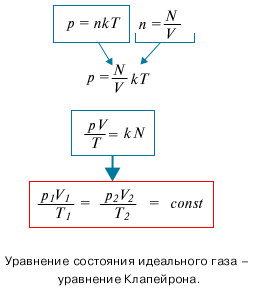
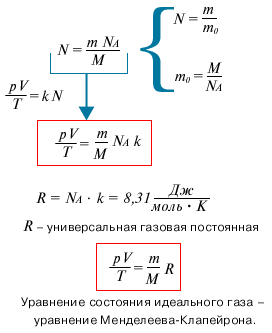
Уравнение Менделеева-Клапейрона.
1.Вывод уравнения Менделеева-Клапейрона.
2.Универсальная газовая постоянная.
3.Уравнение Клапейрона.
4.Изотермический процесс.
5.изобарный процесс.
6.Изохорный процесс.
7.Закон Авогадро.
8. Закон Дальтона.
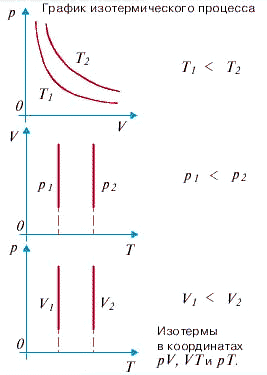
1. Изотермический процесс - процесс изменения состояния термодинамической системы при постоянной температуре .
Если Т =const, то
Закон Бойля-Мариотта
Для данной массы газа произведение давления газа на его объем постоянно, если температура газа не меняется: p1V1=p2V2 при Т = const
Изотермы в разных осях координат
p1V1=p2V2 при Т = const
2. Изохорный процесс-процесс изменения состояния термодинамической системы при постоянном объеме.
Закон Шарля
m= сonst
Давление данной массы газа при постоянном объеме прямо пропорционально абсолютной температуре:
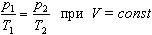
Изохоры в разных осях координат
3. Изобарный процесс - процесс изменения состояния термодинамической системы при постоянном давлении .
m= сonst
Закон Гей-Люссака
Объем данной массы газа при постоянном давлении прямо пропорционален абсолютной температуре
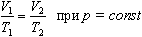
Изобары в разных осях координат
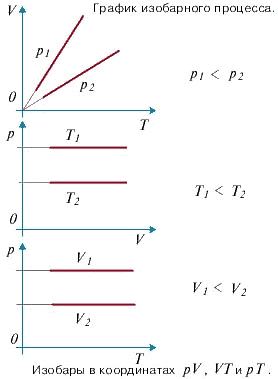
Закон Дальтона
-
Если идеальный газ является смесью нескольких газов, то согласно закону Дальтона, давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов.
-
Парциальное давление - это такое давление, которое производил бы газ, если бы он один занимал весь объем, равный объему смеси.
Дом. Задание:
Учить конспект.
Рефлексия изученного материала.
820. Газ находится в цилиндре с подвижным поршнем и при температуре 300 К занимает объем 250 см3. Какой объем (в см3) займет газ, если температура понизится до 270 К? Давление постоянно. (225)
821. На сколько градусов необходимо нагреть газ при постоянном давлении, чтобы его объем увеличился вдвое по сравнению с объемом при 0°С? (273)
830. В цилиндре под поршнем находится газ. Чтобы поршень оставался в неизменном положении при увеличении абсолютной температуры газа в 2 раза, на него следует положить груз массой 10 кг. Площадь поршня 10 см2. Найдите первоначальное давление (в кПа) газа. g = 10 м/с2.(100)
855. Два сосуда соединены тонкой трубкой с краном. Один из сосудов объемом 3 л заполнен газом при давлении 10 кПа, в другом сосуде объемом 6 л давление пренебрежимо мало. Температура газа в первом сосуде 27°С. Какое давление (в кПа) установится в сосудах, если открыть кран, а температуру газа повысить до 177°С? (5)
856. При каждом ходе поршневой насос захватывает 10 дм3 воздуха из атмосферы при нормальных условиях (Т0 = 273 К) и нагнетает его в резервуар объемом 10 м3. Температура в резервуаре постоянна и равна 364 К. Сколько ходов должен сделать поршень насоса, чтобы повысить давление в резервуаре от нормального (pо = 1 атм) до 10 атм? (6750)
857. Воздух в цилиндре под поршнем сначала изотермически сжали, увеличив давление в 2 раза, а затем нагрели при постоянном давлении. В результате объем воздуха увеличился в 3 раза по сравнению с начальным. До какой температуры (в кельвинах) нагрели воздух, если его начальная температура была 300 К? (1800)
868. Какую массу (в г) водорода содержал баллон, если он взорвался при температуре 1172 К и был рассчитан на хранение азота массой 7 кг при температуре 293 К при десятикратном запасе прочности? Молярная масса водорода 2 кг/кмоль, азота — 28 кг/кмоль.
874. В цилиндре под невесомым поршнем находится 1 моль газа, объем которого 0,02 м3, а температура 250 К. С какой силой надо действовать на поршень перпендикулярно к его поверхности, чтобы он оставался неподвижным? Атмосферное давление 100 кПа, площадь поршня 0,02 м2, универсальная газовая постоянная 8300 Дж/(кмоль*К). (75)
881. Какова разница в массе воздуха, заполняющего зал объемом в 249 м3 зимой и летом, если летом температура в зале достигает 27°С, а зимой падает до 17°С? Давление зимой и летом 105 Па. Универсальная газовая постоянная 8300 Дж/(кмоль*К), молярная масса воздуха 29 кг/кмоль. (10)