Ход урока
1. Организационный момент урока.
№ 1. В какой группе все вещества являются оксидами?
А) NaOH, P2O5, H2CO3
Б) CO2, Na2O, FeO
В) Na2SO4,CaO, SO2
Г) Li2O, SiO2, H2SO3
№ 2. В какой группе все вещества являются основными оксидами?
А) KOH, Ca(OH)2, CaO
В) Na2O, Fe2O3,CrO
Г) Na2O, CaO, MnO
Д) P2O5,NaOH, HNO3
2. Степень электролитической диссоциации
Поскольку электролитическая диссоциация - процесс обратимый, то в растворах электролитов наряду с их ионами присутствуют и молекулы. Другими словами, различные электролиты, согласно теории С. Аррениуса, диссоциируют на ионы в различной степени. Полнота распада (сила электролита) характеризуется количественной величиной – степенью диссоциации.
Степень диссоциации (α – греческая буква альфа) - это отношение числа молекул, распавшихся на ионы (n), к общему числу растворенных молекул (N):
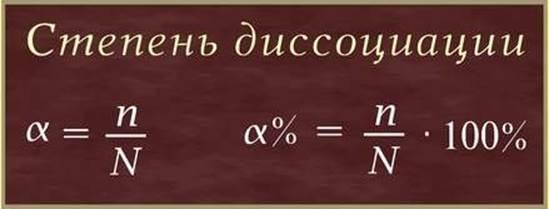
Степень диссоциации электролита определяется опытным путем и выражается в долях единицы или в процентах. Если α = 0, то диссоциация отсутствует, а если α = 1 или 100%, то электролит полностью распадается на ионы. Если же α = 20%, то это означает, что из 100 молекул данного электролита 20 распалось на ионы.
3. Степень диссоциации зависит от природы электролита и растворителя, от концентрации электролита, температуры.
1. Зависимость степени диссоциации от природы: чем полярнее химическая связь в молекуле электролита и растворителя, тем сильнее выражен процесс диссоциации электролита на ионы и тем выше значение степени диссоциации.
2. Зависимость степени диссоциации от концентрации электролита: с уменьшением концентрации электролита, т.е. при разбавлении его водой, степень диссоциации всегда увеличивается.
3. Зависимость степени диссоциации от температуры: степень диссоциации возрастает при повышении температуры (повышение температуры приводит к увеличению кинетической энергии растворённых частиц, что способствует распаду молекул на ионы).
4. Сильные и слабые электролиты
Учитель: Вещества, растворы которых проводят электрический ток назвали электролитами, а вещества, которые не проводят ток – неэлектролитами
– А какие вещества проводят электрический ток? (Растворы кислот, щелочей, солей.)
– С каким видом химической связи растворы веществ проводят электрический ток? (Ионной, ковалентной сильно полярной)
– Какие вещества не проводят электрический ток? (Все кристаллические вещества, оксиды, газы)
– С каким видом химической связи вещества не проводят электрический ток? (С ковалентной неполярной и слабо полярной)
– Сформулируйте определения электролитов и неэлектролитов. (Запись в тетрадь)
– Какой тип химической связи характерен электролитам и неэлектролитам?
– Классы каких веществ относятся к электролитам и неэлектролитам?
– Где Вы в жизни встречались с электролитами? (Аккумуляторы в автомобилях)
| Классификация электролитов | Сильные электролиты | Средние электролиты | Слабые электролиты |
| Значение степени диссоциации (α) | α30% | 3%≤α≤30% | α |
| Примеры | 1. Растворимые соли; 2. Сильные кислоты (НСl, HBr, HI, НNО3, НсlO4, Н2SO4(разб.)); 3. Сильные основания – щёлочи. | H3PO4 H2SO3 | 1. Почти все органические кислоты (CH3COOH, C2H5COOH и др.); 2. Некоторые неорганические кислоты (H2CO3, H2S и др.); 3. Почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH); 4. Вода. |
2 этап: Механизм электролитической диссоциации.
Продолжение беседы:
– Какие частицы могут создавать электрический ток в растворе? (Движущие заряженные частицы)
– Почему и при каких условиях вещества проводят электрический ток?
(Они распадаются на ионы при растворении или расплавлении, являются проводниками второго рода. Прохождение тока происходит за счёт переноса ионов, а не электронов. Металлы – проводники первого рода (ток создается за счет свободных электронов).
– А какие заряженные частицы могут быть в растворах, например, у веществ с ионной связью – растворе NaCl? (Свободные ионы)
Внимание: В кристаллах ионы не свободные, а находятся в узлах кристаллической решетки.
– Что же происходит с кристаллом при растворении его в воде?
– Какова роль воды в этом процессе?
(Вода взаимодействует с электролитом и он под действием воды распадается на ионы).
Рассмотрим механизм этого процесса.
Сначала рассмотрим строение молекулы воды
Вода (диполь) 104,50
Сообщение: Интересное о воде… (Приложение 3)