

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока


КОс по химии для проведения итоговой аттестации 1 курс
КОС по химии для проведения итоговой аттестации студентов 1 курса медицинских специальностей с добавлением рассчетных задач с профессиональной направленностью
Просмотр содержимого документа
«КОс по химии для проведения итоговой аттестации 1 курс»
| Министерство образования и науки Самарской области |
| государственное бюджетное профессиональное образовательное учреждение Самарской области «Сызранский медико-гуманитарный колледж» |
| |
| | УТВЕРЖДАЮ |
|
| Зам. директора по учебной работе |
| | _________________Н.А. Куликова |
| | «_____»____________2024_____ |
| КОМПЛЕКТ |
| КОНТРОЛЬНО-ОЦЕНОЧНЫХ СРЕДСТВ |
| по учебному предмету |
| ОУП. 07. Химия |
| программы подготовки специалистов среднего звена |
| 34.02.01 Сестринское дело 31.02.03 Лабораторная диагностика 31.02.02 Акушерское дело 31.02.01 Лечебное дело |
| базовая подготовка |
| |
| |
г. Сызрань, 2024
Комплект контрольно-оценочных средств разработан в соответствии с требованиями
Федерального государственного образовательного стандарта среднего общего образования, Федерального государственного образовательного стандарта среднего профессионального образования по специальностям 34.02.01 Сестринское дело, 31.02.03 Лабораторная диагностика,
31.02.02 Акушерское дело, 31.02.01 Лечебное дело (базовая подготовка)
с учетом:
- Рабочей программы воспитания ГБПОУ СМГК
- Методических материалов по обязательным общеобразовательным дисциплинам ФГБОУ ДПО ИРПО, 29.09.2022 г., (https://firpo.ru/activities/projects/razrabotka-i- vnedreniye-metodik-prepodavaniya/ )
Составитель:
преподаватель ГБПОУ «СМГК» Захарова С.Г.
Комплект контрольно-оценочных средств рассмотрен и одобрен на заседании
методического объединения преподавателей общеобразовательного блока по специальностям
34.02.01 Сестринское дело 31.02.03 Лабораторная диагностика 31.02.02 Акушерское дело
31.02.01 Лечебное дело (базовая подготовка).
протокол № от « ___» _____________ 2024___
| Руководитель МО ООБ | _________________________ подпись | ___С.Г.Захарова_ |
СОДЕРЖАНИЕ
| 1. | Пояснительная записка | 4 | |
| 2. | ПАСПОРТ КОМПЛЕКТА КОНТРОЛЬНО-ОЦЕНОЧНЫХ СРЕДСТВ | | |
| | 2.1. | Наименование УД, МДК | 4 |
| | 2.2. | Предметы оценивания | 4 |
| | 2.3. | Требования к деятельности обучающегося и соответствующих форм и методов оценивания | 6 |
| | 2.4. | Требования к кадровому обеспечению оценки | 9 |
| 3. | ПРОЦЕДУРЫ ОЦЕНКИ | 9-14 | |
| | 3.1. | Инструментарий оценки освоения УД, МДК | 9 |
| | 3.2. | Кодификация тестовых и практических заданий | 9 |
| | 3.3. | Итоги сформированности | 11 |
| | 3.4. | Критерии оценки знаний обучающихся | 12 |
| 4. | ПРИЛОЖЕНИЯ | 13-23 | |
| | 4.1. | Контрольные вопросы по дисциплине | 13-15 |
| | 4.2. | Инструкции по выполнению работы, тесты | 16-21 |
| | 4.3. | Эталон ответов | 22 |
| | 4.4. | Литература | 23 |
1. ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
Контрольно-оценочные средства (КОС) предназначены для контроля и оценки образовательных достижений обучающихся, освоивших программу учебной дисциплины
«ОУП 07 Химия».
Оценка осуществляется с использованием письменного опроса в форме дифференцированного зачета, и предусматривает использование 5-балльной системы оценивания.
2. Паспорт комплекта оценочных средств
2.1. Учебная дисциплина
ОУП. 07 Химия
2.2. Предметы оценивания
В результате освоения учебной дисциплины обучающийся должен обладать предусмотренными ФГОС СПО, ФГОС среднего общего образования следующими результатами:
| Наименование и код компетенции | Планируемые результаты | |
| Общие (Личностные и метапредметные) | Дисциплинарные (Предметные) | |
| ОК 01. Выбирать способы решения задач профессиональной деятельности применительно к различным контекстам; ОК 02. Использовать современные средства поиска, анализа и интерпретации информации и информационные технологии для выполнения задач профессиональной деятельности; ОК 03. Планировать и реализовывать собственное профессиональное и личностное развитие, предпринимательскую деятельность в профессиональной сфере, использовать знания по финансовой грамотности в различных жизненных ситуациях; ОК 05. Осуществлять устную и письменную коммуникацию на государственном языке Российской Федерации с учетом особенностей социального и культурного контекста; ОК 07. Содействовать сохранению окружающей среды, ресурсосбережению, применять знания об изменении климата, принципы бережливого производства, эффективно действовать в чрезвычайных ситуациях; | гражданское воспитание: -сформированность гражданской позиции обучающегося как активного и ответственного члена российского общества; патриотическое воспитание: -сформированность российской гражданской идентичности, патриотизма, уважения к своему народу, чувства ответственности перед Родиной, гордости за свой край, свою Родину, свой язык и культуру, прошлое и настоящее многонационального народа России; трудовое воспитание: -готовность к труду, осознание ценности мастерства, трудолюбие; -готовность и способность к образованию и самообразованию на протяжении всей жизни; экологическое воспитание: -сформированность экологической культуры, понимание влияния социально-экономических процессов на состояние природной и социальной среды, осознание глобального характера экологических проблем; -умение прогнозировать неблагоприятные экологические последствия предпринимаемых действий, предотвращать их; ценности научного познания: -сформированность мировоззрения, соответствующего современному уровню развития науки и общественной практики, основанного на диалоге культур, способствующего осознанию своего места в поликультурном мире; -совершенствование языковой и читательской культуры как средства взаимодействия между людьми и познания мира; -осознание ценности научной деятельности, готовность осуществлять проектную и исследовательскую деятельность индивидуально и в группе. МР: Овладение универсальными учебными познавательными действиями: а) базовые логические действия: самостоятельно формулировать и актуализировать проблему, рассматривать ее всесторонне; устанавливать существенный признак или основания для сравнения, классификации и обобщения; выявлять закономерности и противоречия в рассматриваемых явлениях; вносить коррективы в деятельность, оценивать соответствие результатов целям, оценивать риски последствий деятельности; развивать креативное мышление при решении жизненных проблем б) базовые исследовательские действия: владеть навыками учебно- исследовательской и проектной деятельности, навыками разрешения проблем; выявлять причинно- следственные связи и актуализировать задачу, выдвигать гипотезу ее решения, находить аргументы для доказательства своих утверждений, задавать параметры и критерии решения; анализировать полученные в ходе решения задачи результаты, критически оценивать их достоверность, прогнозировать изменение в новых условиях; - уметь переносить знания в познавательную и практическую области жизнедеятельности уметь интегрировать знания из разных предметных областей; | 1) иметь представления: о химической составляюще естественнонаучной картины мира, роли химии в познании явлений природы, в формировании мышления и культуры личности, ее функциональной грамотности, необходимой для решения практических задач и экологически обоснованного отношения к своему здоровью и природной среде; 2) владеть системой химических знаний, которая включает: основополагающие понятия (химический элемент, атом, электронная оболочка атома, электронные орбитали атомов, ион, молекула, валентность,электроотрицательность, степень окисления, химическая связь, моль, молярная масса, молярный объем, углеродный скелет, функциональная группа, радикал,изомерия, изомеры, гомологический — ряд, гомологи, углеводороды, кислород- и азотсодержащие соединения, биологически активные вещества (углеводы, жиры, белки), мономер, полимер, структурное звено,высокомолекулярные соединения, кристаллическая решетка, типы химических реакций (окислительно-восстановительные, экзо-и эндотермические, реакцииионного обмена), раствор, электролиты, неэлектролиты, электролитическая диссоциация, окислитель, восстановитель, скорость химической — реакции, химическое равновесие), теории изаконы (теория химического строения органических веществ А.М. Бутлерова, теория электролитической диссоциации, периодический закон Д.И. Менделеева, закон сохранения массы), закономерности, символический язык химии, фактологические сведения о свойствах, составе, получении и безопасном использовании важнейших неорганических и органических веществ в быту и практической деятельности человека; 3) выявлять характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов; 4) использовать наименования химических соединений международного союза теоретической и прикладной | химии и тривиальные названия важнейших веществ (этилен, ацетилен, глицерин, фенол, формальдегид, уксусная кислота, глицин, угарный газ, углекислый газ, аммиак, гашеная известь, негашеная известь, питьевая сода и других), составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснятьих смысл; подтверждать характерные химические свойства веществ соответствующими экспериментами и записями уравнений химических реакций; 5) устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства; определять виды химических связей (ковалентная, ионная, металлическая, водородная), типы кристаллических решеток веществ; классифицировать химические реакции; 6) проводить расчеты по химическим формулам и уравнениям химических реакций с использованием физических — величин, характеризующих вещества с количественной стороны: массы, объема (нормальные условия) газов, количества вещества; использовать системные химические знания для принятия решений в конкретных жизненных ситуациях, связанных с веществами и их применением; 7) соблюдать правила экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; учитывать опасность воздействия на живые организмы определенных веществ, понимая смысл показателя предельной допустимой концентрации; |
Личностные результаты из рабочей программы воспитания по специальности:
| Личностные результаты воспитания (ЛР ВР) | |
| ЛР ВР 1 | Осознающий себя гражданином и защитником великой страны |
| ЛР ВР 9.1 | Соблюдающий и пропагандирующий правила здорового и безопасного образа жизни, спорта; предупреждающий либо преодолевающий зависимости от алкоголя, табака, психоактивных веществ, азартных игр и т.д. |
| ЛР ВР 10.1 | Заботящийся о защите окружающей среды |
| ЛР ВР 15 | Стремящийся к саморазвитию и самосовершенствованию, мотивированный к обучению, к социальной и профессиональной мобильности на основе выстраивания жизненной и профессиональной траектории. Демонстрирующий интерес и стремление к профессиональной деятельности в соответствии с требованиями социально-экономического развития Самарской области. |
2.3. Требования к деятельности обучающегося и соответствующих форм и методов оценивания
| Предмет оценивания (перечень ОР: знания, умения, опыт практической деятельности с ФГОС) | Объект (ы) оценивания | Показатели оценки сформированности ОР | Тип задания/ Методы оценки |
| У11 иметь представления: о химической составляюще естественнонаучной картины мира, роли химии в познании явлений природы, в формировании мышления и культуры личности, ее функциональной грамотности, необходимой для решения практических задач и экологически обоснованного отношения к своему здоровью и природной среде; | Представления о химической составляюще естественнонаучной картины мира | Владение информацией о химической составляюще естественнонаучной картины мира, роли химии в познании явлений природы, в формировании мышления и культуры личности, ее функциональной грамотности, необходимой для решения практических задач и экологически обоснованного отношения к своему здоровью и природной среде; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 2 владеть системой химических знаний, которая включает: основополагающие понятия, теории и законы, символический язык химии, фактологические сведения о свойствах, составе, получении и безопасном использовании важнейших неорганических и органических веществ в быту и практической деятельности человека; | Система химических знаний | Умение владеть системой химических знаний, которая включает: основополагающие понятия, теории и законы, символический язык химии, фактологические сведения о свойствах, составе, получении и безопасном использовании важнейших неорганических и органических веществ в быту и практической деятельности человека; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 3 выявлять характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов; | Умение идентифицировать изучаемые объекты | Владение логическим мышлением и способностью объяснять: характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 4 использовать наименования химических соединений международного союза теоретической и прикладной | химии и тривиальные названия важнейших веществ, составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснять их смысл; подтверждать характерные химические свойства веществ соответствующими экспериментами и записями уравнений химических реакций; | Умение называть химические вещества | Владение навыком называть вещества по разным видам номенклатур, составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснять их смысл; подтверждать характерные химические свойства веществ соответствующими экспериментами и записями уравнений химических реакций; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 5 устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства; определять виды химических связей (ковалентная, ионная, металлическая, водородная), типы кристаллических решеток веществ; классифицировать химические реакции; | Умение различать и описывать химические вещества | Владение навыком устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства; определять виды химических связей (ковалентная, ионная, металлическая, водородная), типы кристаллических решеток веществ; классифицировать химические реакции; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 6 проводить расчеты по химическим формулам и уравнениям химических реакций с использованием физических — величин, характеризующих вещества с количественной стороны: массы, объема (нормальные условия) газов, количества вещества; использовать системные химические знания для принятия решений в конкретных жизненных ситуациях, связанных с веществами и их применением; | Умение применять методы познания для описания химических явлений | Владение навыком математических вычислений, умение проводит расчеты по химическим формулам и химическим уравнениям | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| У 7 соблюдать правила экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; учитывать опасность воздействия на живые организмы определенных веществ, понимая смысл показателя предельной допустимой концентрации; | Умение соблюдать правила экологической безопасности при обращении с химическими веществами | Умение соблюдать правила экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; учитывать опасность воздействия на живые организмы определенных веществ, понимая смысл показателя предельной допустимой концентрации; | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| З.1. важнейшие химические понятия | Умение идентифицировать изучаемые объекты | Знают и понимают смысл важнейших химических понятий | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| З.2. основные законы химии: закон сохранения массы веществ, закон постоянства состава веществ, периодический закон Д.И. Менделеева, закон Гесса, закон Авогадро | Умение применять методы познания для описания химических явлений | Знают и понимают смысл важнейших химических законов | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| З.3. основные теории химии: строение атома, химической связи, электролитической диссоциации кислот и оснований, строения органических и неорганических соединений, химическую кинетику и химическую термодинамику; | Умение применять методы познания для описания химических явлений | Знают и понимают смысл важнейших химических теорий | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| З.4. классификацию и номенклатуру неорганических и органических соединений; | Умение идентифицировать изучаемые объекты | Знают классификацию и номенклатуру неорганических и органических соединений | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
| З.5. вещества и материалы, широко используемые в практике | Умение применять методы познания для описания химических явлений | Знают вещества и материалы, широко используемые в практике | Теоретическое задание/письменный ответ Оценка результатовдиффеиинцированного зачета |
2.4. Требования к кадровому обеспечению оценки
| Кадровое обеспечение | Характеристика |
| Эксперт-экзаменатор | Преподаватель дисциплин общеобразовательного цикла, осуществляющий подготовку по данному учебной дисциплине |
| Ассистент | Преподаватель дисциплин профессионального цикла, не осуществляющий подготовку по учебной дисциплине |
3. Процедуры оценки.
3.1. Задания для оценки освоения учебной дисциплины
Задания для оценки освоения учебного предмета представлены в 2 равнозначных вариантах.Варианты содержат вопросы по неорганической и органической химии, разделеных на 3 блока
Блок "А" состоит из 25 вопросов на выбор единственно верного ответа и задания.
Правильный ответ оценивается 1 баллом
Блок "Б" состоит из 2 заданий на соответствие заданных параметров.
Правильный ответ оценивается 2 баллами
Блок «С» содержит 3 задачи с профессиональной направленностью (1 задача на составление формул веществ, используемых в медицинской практике, 2 расчетные задачи: вывод формулы вещества, расчет массы вещества в растворе).
Правильный ответ в задачах оценивается 3 баллами
Время выполнения теста – 90 минут. Максимальное количество баллов - 38
3.2. Кодификация тестовых заданий
| № п/п | Показатели оценки сформированности ОР | Номер вариант | |
| 1 | 2 | ||
| Номер вопросов | |||
|
| У1. иметь представления: о химической составляюще естественнонаучной картины мира, роли химии в познании явлений природы, в формировании мышления и культуры личности, ее функциональной грамотности, необходимой для решения практических задач и экологически обоснованного отношения к своему здоровью и природной среде | Часть А Часть В Часть С | Часть А Часть В Часть С |
|
| У 2. владеть системой химических знаний, которая включает: основополагающие понятия, теории и законы, символический язык химии, фактологические сведения о свойствах, составе, получении и безопасном использовании важнейших неорганических и органических веществ в быту и практической деятельности человека | А1, А2, А9, А10, А12, А13 | А1, А2, А9, А10, А12, А13 |
|
| У 3. выявлять характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов | А3, А7, А8, А11, А14, А 19, А25 | А3, А7, А8, А11, А14, А 19, А25 |
|
| У 4. использовать наименования химических соединений международного союза теоретической и прикладной | химии и тривиальные названия важнейших веществ, составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснять их смысл; подтверждать характерные химические свойства веществ соответствующими экспериментами и записями уравнений химических реакций | А4, А6, А 18, А 20, А21 | А4, А6, А 18, А 20, А21 |
|
| У 5. устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства; определять виды химических связей (ковалентная, ионная, металлическая, водородная), типы кристаллических решеток веществ; классифицировать химические реакции | А5, А15, А16, А17, А22, А23 В1, В2, С1 | А5, А15, А16, А17, А22, А23 В1, В2, С1 |
|
| У 6. проводить расчеты по химическим формулам и уравнениям химических реакций с использованием физических — величин, характеризующих вещества с количественной стороны: массы, объема (нормальные условия) газов, количества вещества; использовать системные химические знания для принятия решений в конкретных жизненных ситуациях, связанных с веществами и их применением | С2, С3 | С2, С3 |
|
| У7. соблюдать правила экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; учитывать опасность воздействия на живые организмы определенных веществ, понимая смысл показателя предельной допустимой концентрации | С1 | С1 |
|
| З.1. важнейшие химические понятия | А 4, А 9. А 13 А 22а 24 | А 4, А 9. А 13 А 22а 24 |
| 7. | З.2. основные законы химии: закон сохранения массы веществ, закон постоянства состава веществ, периодический закон Д.И. Менделеева, закон Гесса, закон Авогадро | С1, А2. | С1, А2. |
| 8. | З.3. основные теории химии: строение атома, химической связи, электролитической диссоциации кислот и оснований, строения органических и неорганических соединений, химическую кинетику и химическую термодинамику | А 1, А2. А9 | А 1, А2. А9 |
| 9. | З.4. классификацию и номенклатуру неорганических и органических соединений | А 5, А6, А 15. А16. А 17. А18. А 21 В1,В2 | А 5, А6, А 15. А16. А 17. А18. А 21 В1,В2 |
| 10. | З.5. вещества и материалы, широко используемые в практике | А 5, А 6, А 9, А11, А14, А24, А25 | А 5, А 6, А 9, А11, А14, А24, А25 |
3.3. Итоги сформированности
| Предмет оценивания (перечень ОР:Знания,Умения, Опыт практической деятельности в соответствии с ФГОС) | Показатели оценки сформированности ОР | Номер задания |
| У1. иметь представления: о химической составляюще естественнонаучной картины мира, роли химии в познании явлений природы, в формировании мышления и культуры личности, ее функциональной грамотности, необходимой для решения практических задач и экологически обоснованного отношения к своему здоровью и природной среде | Владение информацией о химической составляющей естественнонаучной картины мира, роли химии в познании явлений природы, | см п 3.2 |
| У 2. владеть системой химических знаний, которая включает: основополагающие понятия, теории и законы, символический язык химии, фактологические сведения о свойствах, составе, получении и безопасном использовании важнейших неорганических и органических веществ в быту и практической деятельности человека | Владеет системой химических знаний об основных химических понятиях, законах, свойствах и применении веществ | |
| У 3. выявлять характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов | Умеет выявлять характерные признаки и взаимосвязь изученных понятий, применять соответствующие понятия при описании строения и свойств неорганических и органических веществ и их превращений; выявлять взаимосвязь химических знаний с понятиями и представлениями — других естественнонаучных предметов | |
| У 4. использовать наименования химических соединений международного союза теоретической и прикладной | химии и тривиальные названия важнейших веществ, составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснять их смысл; подтверждать характерные химические свойства веществ соответствующими записями уравнений химических реакций | Умеет использовать правила международной и тривиальной номенклатуры к химическим веществам и составлять формулы неорганических и органических веществ, уравнения химических реакций, объяснять их смысл; подтверждать характерные химические свойства веществ соответствующими записями уравнений химических реакций | |
| У 5. устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства; определять виды химических связей (ковалентная, ионная, металлическая, водородная), типы кристаллических решеток веществ; классифицировать химические реакции | Умеет устанавливать принадлежность изученных неорганических и органических веществ к определенным классам и группам соединений, характеризовать их состав и важнейшие свойства | |
| У 6. проводить расчеты по химическим формулам и уравнениям химических реакций с использованием физических — величин, характеризующих вещества с количественной стороны: массы, объема (нормальные условия) газов, количества вещества; использовать системные химические знания для принятия решений в конкретных жизненных ситуациях, связанных с веществами и их применением | Умеет проводить математические расчеты и применять их для описания химических явлений | |
| У7. соблюдать правила экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; учитывать опасность воздействия на живые организмы определенных веществ, понимая смысл показателя предельной допустимой концентрации; | Владеет информацией о правилах экологически целесообразного поведения в быту и трудовой деятельности в целях сохранения своего здоровья и окружающей природной среды; с учитом опасности воздействия на живые организмы определенных веществ | |
| З.1. важнейшие химические понятия | Знает важнейшие химические понятия | |
| З.2. основные законы химии: закон сохранения массы веществ, закон постоянства состава веществ, периодический закон Д.И. Менделеева, закон Гесса, закон Авогадро | Знает основные химические законы и использует их для конкренных химических задач | |
| З.3. основные теории химии: строение атома, химической связи, электролитической диссоциации кислот и оснований, строения органических и неорганических соединений, химическую кинетику и химическую термодинамику | Знает основные химические теориии и применяет их для конкрентных химических задач | |
| З.4. классификацию и номенклатуру неорганических и органических соединений | Знает различные виды номенклатур | |
| З.5. вещества и материалы, широко используемые в практике | Знает области применения различных химических веществ |
3.4. Критерии оценки знаний
Задания блока «А» оцениваются 1 баллом. Максимальное количество баллов по блоку 25
Задания блока «В» оцениваются 2 баллами. Максимальное количество баллов по блоку 4
Задания блока «С» оцениваются 3 баллами. Максимальное количество баллов по блоку 9
Общее количество баллов по работе – 38 баллов
| Процент правильных ответов, % | Количество правильных ответов | Оценка знаний |
| 90-100 | 38-35 | 5 «отлично» |
| 76-89 | 34-29 | 4 «хорошо» |
| 60-75 | 28-23 | 3 «удовлетворительно» |
| Менее 60 | 22 и менее | 2 «неудовлетворительно» |
ПРИЛОЖЕНИЯ
4.1. Контрольные вопросы для подготовки к дифференцированному зачету
Вопросы по неорганической химии
1. Предмет и задачи химии. Значение неорганической химии в подготовке будущего медика. Основные законы химии.
2.Периодический закон и периодическая система химических элементов Д.И. Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки. Научный и гражданский подвиг Д. И. Менделеева
3.Современные представления о строении атомов химических элементов и закономерности в изменении их свойств на примере: элементов одного периода. Электронные формулы и графические схемы строения электронных слоев атомов этого периода.
4.Современные представления о строении атомов химических элементов и закономерности в изменении их свойств на примере:
5. Элементов одной главной подгруппы. Электронные формулы и графические схемы строения электронных слоев атомов этой подгруппы.
6.Химическая связь, типы химической связи, примеры веществ с разными типами связи
7.Химическое равновесие и условия его смещения: изменение концентрации реагирующих веществ, температуры, давления.
8.Скорость химических реакций. Зависимость скорости от природы реагирующих веществ, температуры, катализатора.
9. Металлы, их положение в периодической системе химических элементов Д.И.Менделеева, строение их атомов, металлическая связь, металлическая кристаллическая решётка и физические свойства металлов. Общие химические свойства металлов.
10. Неметаллы, их положение в периодической системе химических элементов Д.И. Менделеева, строение их атомов. Окислительно-восстановительные свойства неметаллов на примере элементов подгруппы кислорода.
11. Классификация химических реакций в неорганической и органической химии.
12. Растворы. Способы выражения концентрации растворов (массовая доля, молярная концентрация)
13. Теория электролитической диссоциации. Диссоциация веществ с ионной и сильнополярной ковалентной связями.Гидролиз солей, его типы.
14.Окислительно- восстановительные процессы, их значение.
15.Кислоты, их классификация и свойства на основе представлений об электролитической диссоциации.
16.Основания , их классификация и свойства на основе представлений об электролитической диссоциации.
17.Соли, их состав, свойства на основе представлений об электролитической диссоциации.
18.Оксиды, их состав, свойства на основе представлений об электролитической диссоциации.
19.Электрохимический ряд металлов. Вытеснение металлов из растворов солей другими металлами. Коррозия металлов. Способы защиты металлов от коррозии.
20.Электролиз как окислительно-восстановительный процесс. Электролиз расплавов и растворов на примере хлорида натрия.
21.Типы кристаллических решеток веществ. Зависимость свойств веществ от типа кристаллической решетки.
22.Вода. Ее потребление в быту и на производстве. Роль воды в химических реакциях.
23.Общая характеристика элементов YII группы главной подгруппы. Ответ подтвердите уравнениями реакций.
24.Общая характеристика элементов VI группы, главной подгруппы. Кислород и сера как простые вещества. Аллотропия. Наиболее важные соединения кислорода и серы, их значение для человека.
25.Общая характеристика элементов V группы, главной подгруппы на основании их положения в периодической системе Д.И. Менделеева и строения атомов. Азот и фосфор как простые вещества. Аллотропные видоизменения фосфора, их строение и свойства. Наиболее важные соединения азота и фосфора, их применение. Биологическая роль азота и фосфора.
26.Общая характеристика элементов V группы, главной подгруппы на основании их положения в периодической системе Д.И. Менделеева и строения атомов. Азот и фосфор как простые вещества. Аллотропные видоизменения фосфора, их строение и свойства. Наиболее важные соединения азота и фосфора, их применение. Биологическая роль азота и фосфора.
27. Реакции ионного обмена. Признаки реакций ионного обмена
Вопросы по органической химии
Основые положения теории химического строения органических веществ А.М. Бутлерова. Изомерия органических веществ, ее виды.
Предельные углеводороды, общая формула гомологов данного ряда, строение. Химические свойства метана. Практическое применение алканов.
Непредельные углеводороды ряда этилена, общая формула и химическое строение. Свойства и применение этилена.
Алкины, их химическое строение, свойства, нахождение в природе, практическое значение.
Диеновые углеводороды, их химическое строение, свойства, получение и практическое значение.
6.Ароматические углеводороды. Бензол, структурная формула, свойства и получение. Применение бензола и его гомологов.
7.Предельные одноатомные спирты, их строение, физические и химические свойства. Получение и применение этилового спирта.
8.Фенол, его химическое строение, свойства, получение и применение.
9.Альдегиды, их химическое строение и свойства. Получение и применение муравьиного и уксусного альдегидов.
10.Предельные одноосновные карбоновые кислоты, их строение и свойства на примере уксусной кислоты.
11.Жиры, их состав и свойства. Биологическая роль жиров. Переработка жиров.
12.Многоатомные спирты. Глицерин и этиленгликоль как представители многоатомных спиртов.
13.Углеводы. Классификация.Глюкоза, строение, свойства, применение.
16.Углеводы, классификация
17.Аминокислоты, состав, свойства, биологическая роль, применение.
18.Белки как биополимеры. Свойства и биологические функции белков
19.Амины. Анилин, строение, свойства, применение.
20.ВМС. Полимеры, получение и применение
Государственное бюджетное профессиональное образовательное учреждение Самарской области
«Сызранский медико-гуманитарный колледж»
| Рассмотрено и одобрено на заседании МО преподавателей общеобразовательного блока Протокол № ____ от____________20 г. Руководитель МО ООБ ___________С.Г.Захарова | Зачетное задание №1 по учебному предмету «Химия» по специальностям: 34.02.01 Сестринское дело 31.02.03 Лабораторная диагностика 31.02.02 Акушерское дело 31.02.01 Лечебное дело Курс: I | УТВЕРЖДАЮ Зам. директора по учебной работе _________Н. А.Куликова «____»_______20 г. |
Вариант 1 Часть А Выберите один правильный ответ
1. Число электронов, которые содержатся в атоме углерода равно:
1) 6; 2) 12; 3) 8
2. Электронная формула атома 1s 22s 22p 63s 23p2 . Химический знак этого элемента:
1) C; 2) O; 3) Si
3. Радиусы атомов химических элементов в ряду: хлор, фосфор, алюминий, натрий:
1) увеличиваются; 2) уменьшаются; 3) не изменяются.
4. Химическая связь в молекуле воды:
1) ионная; 2) ковалентная полярная; 3) ковалентная неполярная.
5. Формулы кислотных оксидов:
1) CO2 и CaO; 2) CO2 и SO3; 3) K2O и Al2O3
6. Формула сероводородной кислоты: 1) H2S; 2) H2SO4; 3) H2SO3
7. К реакциям обмена относится:
1) CaO + H2O= Ca(OH)2; 2) Сu(OH)2= CuO + H2O; 3) KOH + HNO3= KNO3 + H2O
8. Горение аммиака 4NH3(r) + 3О2(г) = 2N2(r) + 6Н2О(Ж) + Q является реакцией
соединения, каталитической, эндотермической
замещения, каталитической, экзотермической
окислительно-восстановительной, некаталитической, экзотермической
обмена, некаталитической, эндотермической
9. Электролиты, при диссоциации которых образуются катионы металла, и анионы кислотного остатка называются:
1) кислотами; 2) солями; 3) основаниями.
| 10.Сокращенное ионное уравнение Ba2+ + SO42- = BaSO4 соответствует реакции между: | |
| а) раствором Ba(OH)2 и раствором H2SO4; | в) BaCO3 u раствором H2SO4; |
| б) раствором Ba(NO3)2 и раствором H2SO4; | г) BaO и раствором Na2SO4; |
11. Осадок образуется при взаимодействии раствора КОН с
HNO3 2. NH4Cl 3. SO3 4. FeSO4
12. Химическое равновесие в системе СО(г) + 2Н2(г) → СН3ОН(г) + Q сместится в сторону продукта реакции при
1) понижении температуры 2) понижении концентрации СО
3) повышении концентрации СН3ОН 4) повышении температуры
13.. Какая степень окисления хрома в К2Сr2О7?
1) +6; 2) +3; 3) -3; 4) -6.
14. Лакмус становится красным в водном растворе
1) Ca(NO3)2 2) Na2SiO3 3) CrCl3 4) K2S
15. Вещества с общей формулой CnH2n относятся к классу
1) алканов 2) алкенов 3) алкинов 4) аренов
16. Вещество, формула которого С2Н6 относится к классу
1) алканов 2) алкенов 3) алкинов 4) Аренов
17. Вещество, формула которого СН3 – СН2 – СН2 – СН3 является
1) алканом 2) алкеном 3) алкином 4) ареном
18. Вещество, формула которого СН2 = СН – СН – СН3 называется
СН3
1) 2-метилбутен-3 2) 2-метилбутин-3 3) 3-метилбутен-1 4) 3-метилбутин-1
19. Характерной химической реакцией для веществ, имеющих общую формулу СnH2n+2, является реакция
1) замещения 2) гидрирование 3) присоединение 4) дегидрирование
20.Укажите «лишнее» вещество в ряду:
1) 3 -метилбутаналь; 2) изопропанол;
3) метаналь; 4) ацетальдегид.
21. Дайте название соединению
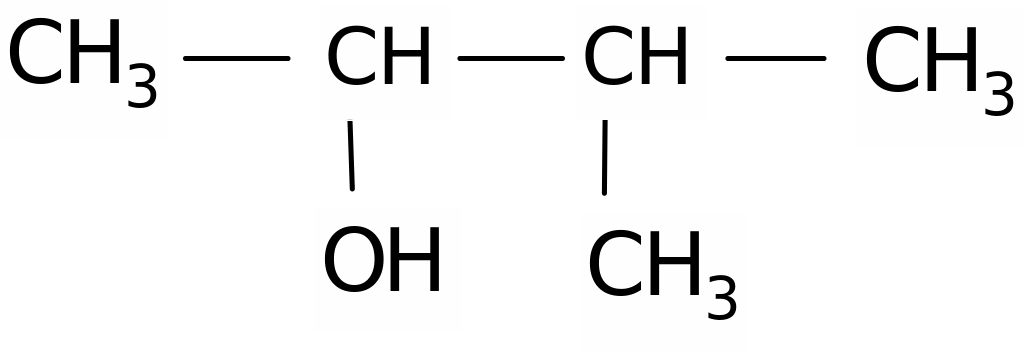
1) 3-метилбутанол-2; 2) 2-метилбутанол-3;
3) 3-метилпропанон-2; 4) 2-метилпропаналь-2.
22. Функциональная группа – СОН характерна для:
1) альдегидов; 2) сложных эфиров;
3) простых эфиров; 4) спиртов.
23. Вещество, относящееся к аминам, имеет формулу
1)С6Н5—NO2 2) С6Н5—NH2
3)С6Н5—СН3 4) С6Н5—OH
24. Мономерами белков выступают:
1) аминокислоты; 2) моносахариды;
3) нуклеотиды; 4) остатки фосфорной кислоты.
25. Какие вещества можно использовать для последовательного осуществления следующих превращений С2H5Cl → С2Н5ОН → С2Н5Оna
1) KOH, NaCl 3) KOH, Na
2) HOH, NaOH 4) O2, Na
Часть В
В1. Установите соответствие между формулой вещества и его принадлежностью к определенному классу (группе), неорганических соединений.
| ХИМИЧЕСКАЯ ФОРМУЛА: А) Н3РО4 Б) Fе(ОН)3 В) LiВr Г) АlОН(NО3)2 F) | КЛАСС (ГРУППА): 1) кислота; 2) основание; 3)амфотерный гидроксид; 4) средняя соль; 5) кислая соль; 6) основная соль. |
В 2. Установите соответствие между формулой вещества и названием.
1) C2H5OH а) уксусная кислота
2) CH3COOH б) глюкоза
3) C12H22O11 в) этиловый спирт
4) C6H5OH г) фенол
д) сахароза
е) глицерин
Часть С
Решите профессионально-ориентированные задачи
С.1 В медицинской практике используют следующие препараты:
1.Порошок Боткина используется как лёгкое слабительное. В его состав входят гидрокарбонат натрия и сульфат натрия. Составьте формулы этих солей.
2.Микстура Бехтерева используется как успокаивающее средство. В её состав входят бромиды натрия, калия, аммония. Составьте формулы этих веществ.
3. Для лечения и профилактики гипертонии ( повышенного артериального давления) используется гиперсол. В его состав входят хлорид натрия, сульфат натрия, ортофосфат натрия, гидрокарбонат натрия, иодид натрия, хлорид калия, вода. Составьте формулы веществ этого средства.
Решите расчетные задачи
С 2. При кислотных ожогах для нейтрализации используют вещество, содержащее 27,38% натрия, 1,19% водорода, 14,29% углерода, 57,14% кислорода. Установите формулу вещества
С 3. В больницу поступил пациент, для поддержания состояния которого, необходимо ввести 250 г 0,9%-ного физиологического раствора. Сколько граммов поваренной соли и воды необходимо взять для приготовления данного раствора.
Государственное бюджетное профессиональное образовательное учреждение Самарской области
«Сызранский медико-гуманитарный колледж»
| Рассмотрено и одобрено на заседании МО преподавателей общеобразовательного блока Протокол № ____ от____________20 г. Руководитель МО ООБ ___________С.Г.Захарова | Зачетное задание №2 по дисциплине «Химия» по специальностям: 34.02.01 Сестринское дело 31.02.03 Лабораторная диагностика 31.02.02 Акушерское дело 31.02.01 Лечебное дело Курс: I | УТВЕРЖДАЮ Зам. директора по учебной работе _________Н. А.Куликова «____»_______20 г. |
Вариант 2 Часть А Выберите один правильный ответ
1. Число нейтронов, которые содержатся в атоме кислорода равно:
1) 6; 2) 12; 3) 8.
2. Формула высшего оксида элемента, электронная формула которого 1s 22s22p 63s 23p3 :
1) N2 O5 ; 2) P2 O5; 3) B2O3 .
3. Наиболее ярко выраженные неметаллические свойства проявляет:
1) фосфор; 2) сера; 3) кремний.
4. Формула вещества с ковалентной полярной связью:
1) H2O; 2) O2; 3) CaCl2
5. Формула основания и кислоты соответственно:
1) Ca(OH)2 и Be(OH)2 ; 2) NaOH и KHSO4; 3) Al(OH)3 и HNO3
6. Формула сульфита натрия:
1) Na2SO4; 2) Na2SO3; 3) Na2S
7. К реакциям замещения относится:
1) Ca + H2SO4= CaSO4 + H2; 2) Сu(OH)2= CuO + H2O; 3) KOH + HNO3= KNO3 + H2O
8. Реакция, уравнение которой 3H2 + N2 ↔ 2NH3 + Q, является
1) обратимой и экзотермической 2) необратимой и экзотермической
3)обратимой и эндотермической 4) необратимой и эндотермической
9. Электролиты, при диссоциации которых образуются катионы металла и гидроксид-ионы называются:
1) солями; 2) кислотами; 3) основаниями
10. Сокращенное ионное уравнение Са2+ + СО32- = СаСО3 соответствует взаимодействию между веществами
Са(ОН)2 и СО2 3. СаО и СО2
СаСl2 и Na2CO3 4. CaSO4 и K2CO3
11. Осадок выпадает при взаимодействии растворов
HCl (р-р) и CuO 2. NaOH (р-р) и H3PO4
H2SO4 (р-р) и Al(OH)3 4. AgNO3 и KCl (р-р)
12. Химическое равновесие в системе 2NО(г) + О2(г) → 2NО2(г) + Q смещается в сторону образования продукта реакции при
1) повышении давления 2) повышении температуры
3) понижении давления 4) применении катализатора
13. Какая степень окисления железа в Fe2(SO4)3 ?
1) +6; 2) +3; 3) -3; 4) -6.
14. Кислую среду имеет водный раствор
1) Na3PO4 2) KCl 3) Na2CO3 4) ZnSO4
15. Для алканов характерна общая формула
1)CnH2n 2)CnH2n+2 3)CnH2n-2 4)CnH2n-6
16. К классу алкенов относится вещество с молекулярной формулой
1) С6Н10 2) С6Н6 3) С6Н12 4) С6Н14
17. Вещество, формула которого СН3 – С ≡ С – СН3 является
1) алканом 2) алкеном 3) алкином 4) ареном
18. Гомологом этана является
1) С2Н4 2) С2Н6 3) С3Н8 4) С3Н6
19. Укажите название соединения СН2 = СН - СН2 - СН2 - СН2 - СН3
1) 3,3-диметилбутин-1; 2) октин-1; 3) 3,3-диметилпентин-1; 4) гексен-1
20. Для алкенов характерна реакция
1) замещения 2) обмен 3) присоединения 4) дегидратации
21. Дайте название соединению:
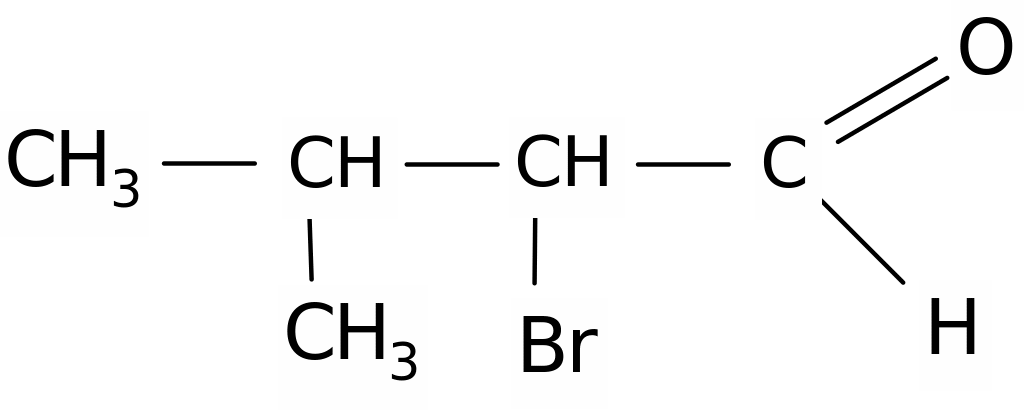
1) 2-метил-3-бромбутанол-1; 2) 2-бром-З-метилбутаналь;
3) 2-бром-З-метилпропаналь; 4) 2-метил-З-бромбутаналь.
22.Укажите «лишнее» вещество в ряду:
1) метанол; 2) этаналь; 3) пентанол; 4) бутиловый спирт.
23. Функциональная группа – СОО- характерна для
1) альдегидов; 2) сложных эфиров; 3) углеводов; 4) спиртов.
24.В состав белков может входить
1)пять аминокислот; 2) двадцать аминокислот;
3)десять аминокислот; 4) тридцать аминокислот
25. Какие вещества можно использовать для последовательного осуществления следующих превращений С2Н5ОН → С2Н5Сl → С4Н10
1)NaCl, Na 3) O2, Na
2) HСl, Na 4) HСl, NaОН
Часть В
В 1. Установите соответствие между формулой вещества и его принадлежностью к определенному классу (группе), неорганических соединений.
| ХИМИЧЕСКАЯ ФОРМУЛА: А) Н2S Б) NаНСО3 В) NН4СI Г) Са(ОН)2 F) | КЛАСС (ГРУППА): 1) кислота; 2) основание; 3)амфотерный гидроксид; 4) средняя соль; 5) кислая соль; 6) основная соль. |
В 2. Установите соответствие между названием вещества и его формулой.
1) уксусная кислота а) C2H5OH
2) сахароза б) CH3COOH
3) этаналь в) C12H22O11
4) этиловый спирт г) C6H5OH
д) CH3COH
е) C6H12O6
Часть С
Решите расчетные профессионально-ориентированные задачи
С.1 В медицинской практике используют следующие препараты:
1. Раствор Липовецкого используется при лечении кожных заболеваний. Он применяется наружно. В его состав входят иодид калия, соляная кислота, вода. Составьте формулы веществ.
2. Смесь Бурже используется при желудочно- кишечных заболеваниях. Составьте формулы веществ этой смеси, если в её состав входят сульфат натрия, сульфат магния, оксид магния, гидрокарбонат натрия.
3. Паста Унна используется при лечении кожных заболеваний. В её состав входят: карбонат кальция, оксид цинка, гидроксид кальция, масло льняное. Составьте формулы неорганических веществ.
Решите расчетные задачи
С 2. Данное вещество применяется для прижигания ранок и удаления бородавок. Установите формулу вещества, если массовая доля серебра равна 63,53%, азота 8,24%, кислорода 28,23%.
С 3. Применяемая в медицине йодная настойка представляет собой 10%-ный раствор йода в спирте. Сколько надо взять йода и спирта, чтобы приготовить 150 г йодной настойки.
4.3. Эталон ответов.
| Варианты | №1 | №2 | | №1 | №2 | | №1 | №2 |
| А1 | 1 | 3 | В1 | А-1 | А-1 | С 1 - 1 | NaHCO3 Na2SO4 | KI HCl H2O |
| А2 | 3 | 2 | | Б-2 | Б-5 | С 1 -2 | NaBr KBr NH4Br | Na2SO4 Mg SO4 MgO NaHCO3 |
| А3 | 1 | 2 | | В-4 | В-4 | С 1- 3 | NaCl Na2SO4 Na3PO4 NaHCO3 NaI KCl, H2O | CaCO3 ZnO Ca(OH)2 |
| А4 | 2 | 1 | | Г-6 | Г-2 | | | |
| А5 | 2 | 3 | | | | С2 | NaHCO3 | AgNO3 |
| А6 | 1 | 2 | В2 | 1-в | 1-б | | | |
| А7 | 3 | 1 | | 2-а | 2-в | C 3 | m (в) =2.25 m(H2O)=245,75 | m (в) =15 m(спирта)=135 |
| А8 | 3 | 1 | | 3-д | 3-д | | | |
| А9 | 2 | 3 | | 4-г | 4-а | | | |
| А10 | 2 | 2 | | | | | | |
| А11 | 4 | 4 | | | | | | |
| А12 | 1 | 1 | | | | | | |
| А13 | 1 | 2 | | | | | | |
| А14 | 3 | 4 | | | | | | |
| А15 | 2 | 2 | | | | | | |
| А16 | 1 | 3 | | | | | | |
| А17 | 1 | 3 | | | | | | |
| А18 | 3 | 3 | | | | | | |
| А19 | 1 | 4 | | | | | | |
| А20 | 2 | 3 | | | | | | |
| А21 | 2 | 2 | | | | | | |
| А22 | 1 | 2 | | | | | | |
| А23 | 2 | 2 | | | | | | |
| А24 | 1 | 2 | | | | | | |
| А25 | 3 | 2 | | | | | | |
4.4. Литература
Основные источники:
1.Габриелян. О.С., Остроумов И.Г., Сладков С.А. Химия. 10, углубленный уровень, М.: Просвещение, 2019.
2.Габриелян. О.С., Остроумов И.Г., Сладков С.А. Химия. 11, углубленный уровень, М.: Просвещение, 2019.
Дополнительные источники:
1.Габриелян О.С. и др. Химия: пособие для подготовки к ЕГЭ: учеб. пособие для студентов профессиональных образовательных организаций, осваивающих профессии и специальности СПО. – М., 2017
2.Габриелян О.С., Лысова Г.Г. Химия. Тесты, задачи и упражнения: учеб. пособие для студентов профессиональных образовательных организаций, осваивающих профессии и специальности СПО. – М., 2017
3.Кузьменко Н.Е., Еремин В.В. Химия. М.: Экзамен: Издательский дом "ОНИКС 21 век", 2020.
2












