

Тема урока:
Электролитическая диссоциация.
Учитель химии:
Шелудянкина Наталья Сергеевна
Ульяновск ,2017
Цели урока:
1) Сформировать понятия об электролитах и неэлектролитах. 2) Рассмотреть механизм диссоциации веществ с ионной и ковалентной полярной связью. 3) Ввести понятие «степень электролитической диссоциации» и рассмотреть классификацию электролитов.
Вещества
Электропроводность
Электролиты
Неэлектролиты

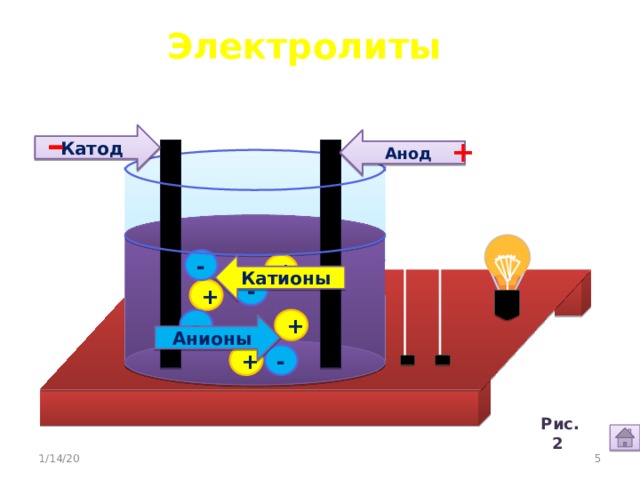
Электролиты
Катод
Анод
-
+
-
+
Катионы
-
+
-
+
Анионы
+
-
Рис.2 .
1/14/20
это вещества, растворы и расплавы которых
проводят электрический ток.
Электролиты -
Кислоты:
HCl; HNO 3 ; H 2 SO 4
NaOH; KOH; Ba(OH) 2
NaCl; CuSO 4 ; Al(NO 3 ) 3
Щелочи:
Соли:
1/14/20

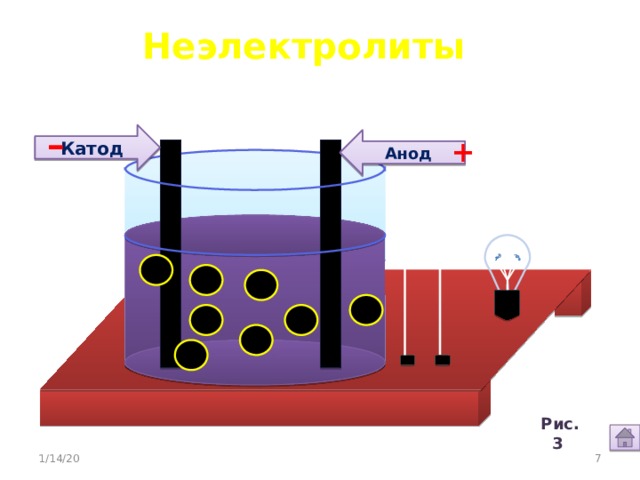
Неэлектролиты
Катод
-
Анод
+
Рис.3 .
1/14/20
6
Неэлектролиты -
это вещества, растворы или расплавы которых не
проводят электрический ток.
Органические вещества:
сахар, ацетон,бензин, керосин, глицерин, этиловый спирт, бензол и др.
Газы: кислород, водород, азот идр.
1/14/20
6
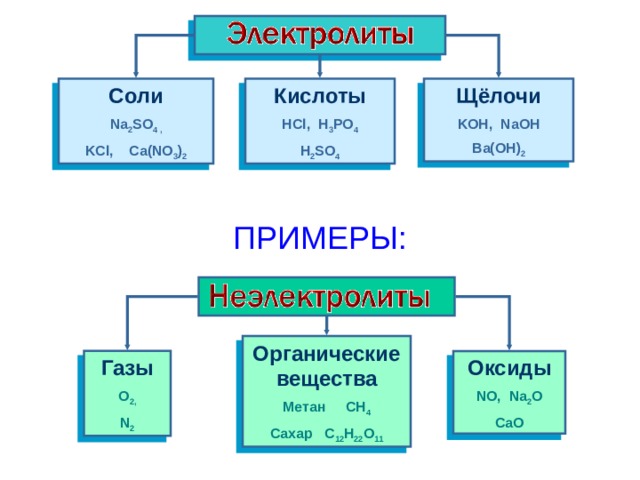
Кислоты
Щёлочи
Cоли
KOH, NaOH
HCl, H 3 PO 4
Na 2 SO 4 ,
H 2 SO 4
Ba(OH) 2
KCl, Ca(NO 3 ) 2
ПРИМЕРЫ:
Органические вещества
Метан CH 4
Сахар C 12 H 22 O 11
Оксиды
Газы
NO, Na 2 O
O 2,
CaO
N 2

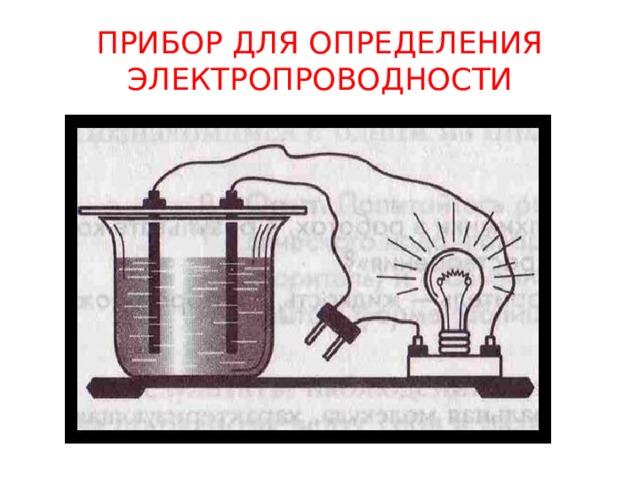
ПРИБОР ДЛЯ ОПРЕДЕЛЕНИЯ ЭЛЕКТРОПРОВОДНОСТИ


сильный электролит
неэлектролит
слабый электролит

Теория электролитической диссоциации
Процесс растворения или плавления электролитов сопровождается образованием заряженных частиц , способных проводить электрический ток
процесс растворения электролитов сопровождается образованием заряженных частиц, способных проводить электрический ток
С. А. Аррениус (1859-1927)

Современная теория
электролитической диссоциации
(ТЭД)
Первое положение ТЭД
- Все вещества по их способности проводить электрический ток в растворах или расплавах делятся на электролиты и неэлектролиты .
Второе положение ТЭД
- В растворах электролиты диссоциируют ( распадаются) на положительные и отрицательные ионы.
Процесс распада электролита на ионы в растворе или расплаве называется электролитической диссоциацией.

За 1 минуту выписать из перечня веществ электролиты и неэлектроиты:
1 ряд.
Ba(OH) 2 , H 2 SO 4 , ZnCL 2 , HCL, CaO, KNO 3 , NaOH, O 2 , спирт, AL(OH) 3 .
2-3 ряд
AgCL, CuSO 4 , H 2 SiO 3 , HNO 3 , RbOH, FeO, CuO, KOH,сахар, K 2 SO 4.
Электролиты
Неэлектролиты
CH 3 COOH
+
+
+
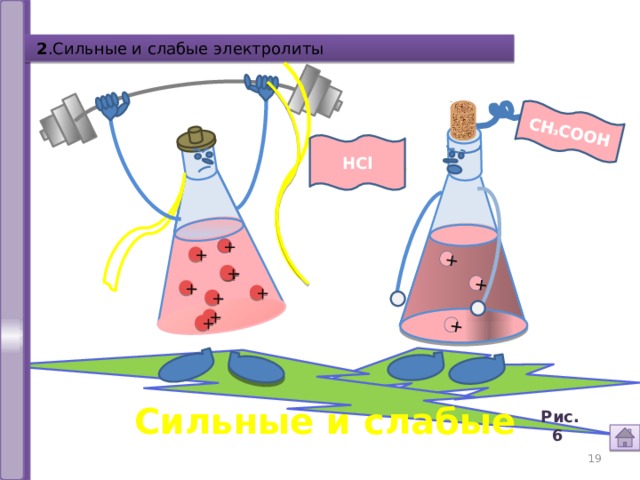
2 .Сильные и слабые электролиты
HCl
+
+
+
+
+
+
+
+
+
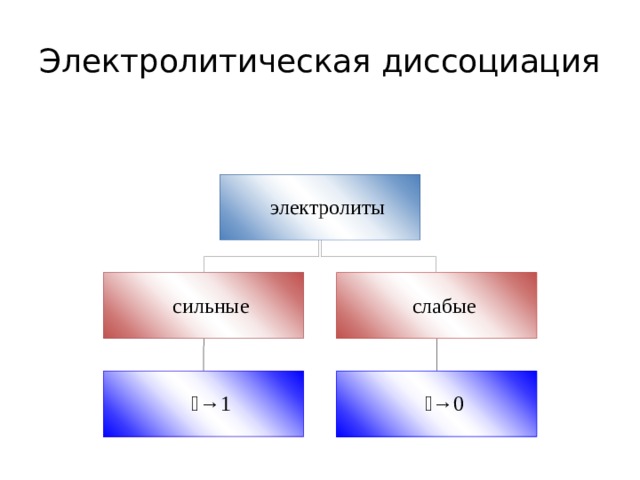
Сильные и слабые
Рис.6 .
 30% Слабые электролиты n α = N α 30% 19 1/14/20 " width="640"
30% Слабые электролиты n α = N α 30% 19 1/14/20 " width="640"
Степень электролитической
диссоциации (α) -
отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе.
Сильные электролиты α 30%
Слабые электролиты
n
α =
N
α 30%
19
1/14/20

Электролитическая диссоциация
 30%) Соли практически все Основания Слабые (α растворимые в воде нерастворимые Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов Кислоты водный раствор аммиака - бескислородные все кислородосодержащие HI, HBr, HCl HF, H 2 S HClO 4 H 2 SO 4 , HNO 3 H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , Н 3 РO 4 , CH 3 COOH и др. " width="640"
30%) Соли практически все Основания Слабые (α растворимые в воде нерастворимые Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов Кислоты водный раствор аммиака - бескислородные все кислородосодержащие HI, HBr, HCl HF, H 2 S HClO 4 H 2 SO 4 , HNO 3 H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , Н 3 РO 4 , CH 3 COOH и др. " width="640"
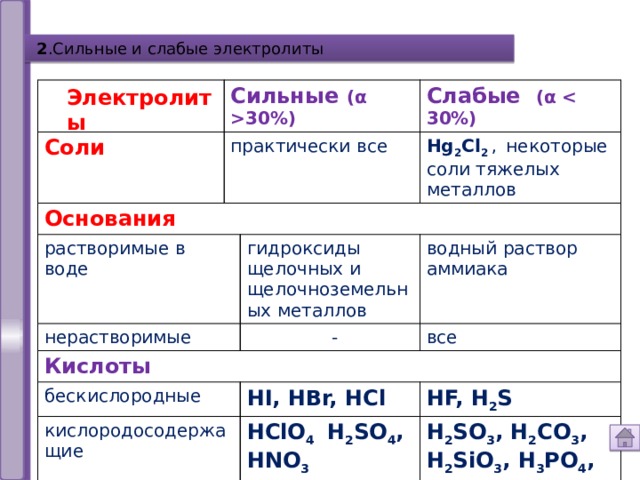
2 .Сильные и слабые электролиты
Электролиты
Сильные (α 30%)
Соли
практически все
Основания
Слабые (α
растворимые в воде
нерастворимые
Hg 2 Cl 2 , некоторые cоли тяжелых металлов
гидроксиды щелочных и щелочноземельных металлов
Кислоты
водный раствор аммиака
-
бескислородные
все
кислородосодержащие
HI, HBr, HCl
HF, H 2 S
HClO 4 H 2 SO 4 , HNO 3
H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , Н 3 РO 4 , CH 3 COOH и др.
























 30% Слабые электролиты n α = N α 30% 19 1/14/20 " width="640"
30% Слабые электролиты n α = N α 30% 19 1/14/20 " width="640"

 30%) Соли практически все Основания Слабые (α растворимые в воде нерастворимые Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов Кислоты водный раствор аммиака - бескислородные все кислородосодержащие HI, HBr, HCl HF, H 2 S HClO 4 H 2 SO 4 , HNO 3 H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , Н 3 РO 4 , CH 3 COOH и др. " width="640"
30%) Соли практически все Основания Слабые (α растворимые в воде нерастворимые Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов Кислоты водный раствор аммиака - бескислородные все кислородосодержащие HI, HBr, HCl HF, H 2 S HClO 4 H 2 SO 4 , HNO 3 H 2 SO 3 , H 2 CO 3 , H 2 SiO 3 , Н 3 РO 4 , CH 3 COOH и др. " width="640"



















