МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение высшего образования
«Югорский государственный университет» (ЮГУ)
НЕФТЯНОЙ ИНСТИТУТ
(ФИЛИАЛ) ФЕДЕРАЛЬНОГО ГОСУДАРСТВЕННОГО БЮДЖЕТНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ ВЫСШЕГО ОБРАЗОВАНИЯ «ЮГОРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
(НефтИн (филиал) ФГБОУ ВО «ЮГУ»)
ОП.03 ОРГАНИЧЕСКАЯ ХИМИЯ
РАЗДЕЛ УГЛЕВОДОРОДЫ
Методические указания к выполнению практических занятий
для обучающихся образовательных учреждений
среднего профессионального образования
по специальности 18.02.09
«Переработка нефти и газа»
Нижневартовск 2022
Методические указания разработаны по дисциплине ОП.03 Органическая химия по разделу Углеводороды для обучающихся образовательных учреждений среднего профессионального образования по специальности 18.02.09 Переработка нефти и газа.
Учебная дисциплина ОП.03 Органическая химия является обязательной частью общепрофессионального цикла основной образовательной программы в соответствии с ФГОС СПО по специальности 18.02.09 Переработка нефти и газа и обеспечивает формирование общих компетенций по всем видам деятельности ФГОС СПО по специальности 18.02.09 Переработка нефти и газа.
Данная дисциплина предусматривает изучение теоретических основ органической химии, способов получения и свойств различных классов органических соединений, практического применения органических веществ в экономике страны.
В результате изучения раздела Углеводороды дисциплины студент должен:
знать: основные классы углеводородов (предельные, непредельные, ароматические);
- состав, строение, свойства и область применения углеводородов
- название углеводородов по рациональной и международной номенклатуре;
уметь:
- составлять уравнения реакций, подтверждающие химические свойства и способы получения углеводородов;
- называть углеводороды и их производные по систематической и рациональной номенклатуре;
- проводить расчеты по уравнениям реакций;
В процессе выполнения заданий практических занятий обучающиеся закрепляют знания по различным классам углеводородов, что способствует изучению органических соединений других разделов.
Каждое практическое занятие способствует формированию диалектико-материалистического мировоззрения: единство окружающего мира, зависимость свойств углеводородов от их состава и строения, переход количественных изменений в качественные.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №1
РЕШЕНИЕ ЗАДАЧ ПО УСТАНОВЛЕНИЮ ФОРМУЛ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА ОСНОВЕ ДАННЫХ ЭЛЕМЕНТАРНОГО АНАЛИЗА
Цель: закрепить умения решать задачи на: а) расчет объемов газов, образующихся или участвующих при горении органических веществ; б) вывод молекулярной формулы органического соединения по его относительной плотности и массовой доле элементов.
ВАРИАНТ 1
1. Какой объем воздуха (н.у.) потребуется для сжигание смеси метана объемом 5 литров с пропаном объемом 10 литров? Какой объем углекислого газа при этом образовался?
2. Выведите формулу углеводорода, содержащего 82,75% углерода. Относительная плотность этого вещества по воздуху равна 2. Назовите это вещество. Составьте его структурную формулу
3. Выведите молекулярную формулу хлорпроизводного предельного углеводорода, содержащего 83,53 % хлора, 2,35 % водорода и 14,12 % углерода. Относительная молекулярная масса этого вещества равна 85. Дайте название веществу.
4. Найдите молекулярную формулу углеводорода, массовая доля углерода в котором составляет 81,8 %. Относительная плотность вещества по азоту равна 1,57. Назовите вещество.
ВАРИАНТ 2
1. Найдите объем кислорода и воздуха, который израсходовали на сжигание смеси этана объемом 15 литров с пропаном объемом 5 литров? Какой объем углекислого газа при этом образовался?
2. Выведите формулу органического вещества, содержащего 81,8% углерода и 18,2% водорода, если относительная плотность по водороду равна 22. Составьте его структурную формулу. Дайте ему название.
3. Относительная плотность паров органического вещества по водороду равна 30. Определите молекулярную формулу этого вещества, если массовая доля углерода в нем равна 40%, водорода – 6,7 %, а кислорода – 53,3 %. Назовите вещество.
4. Найдите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 15,79 %. Относительная плотность паров этого вещества по воздуху равна 3,93. Назовите вещество.
ВАРИАНТ 3
1. Сколько литров кислорода и воздуха израсходовалось на сжигание 20 литров бутана и 5 литров метана? Какой объем углекислого газа при этом образовался?
2. Выведите молекулярную формулу углеводорода, содержащего 85,71% углерода. Относительная плотность паров этого вещества по водороду равна 21. Составьте его структурную формулу. Дайте название углеводороду
3. Выведите молекулярную формулу вещества, содержащего 54,55% углерода, 9,09% водорода и 36,36% кислорода. Относительная плотность паров этого вещества по водороду равна 22. Дайте название веществу.
4. Найдите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 25%. Относительная плотность паров этого вещества по кислороду равна 0,5. Дайте название веществу.
ВАРИАНТ 4
1. Сколько литров кислорода и воздуха израсходовалось на сжигание 20 литров метана и 10 литров этана? Какой объем углекислого газа при этом образовался?
2. Выведите молекулярную формулу и дайте название углеводороду, содержащему 85,7% углерода. Относительная плотность паров этого вещества по водороду равна 14. Составьте его структурную формулу. Дайте ему название.
3. Выведите молекулярную формулу органического соединения, содержащего 40 % углерода, 6,7 % водорода, 53,3 % кислорода. Относительная молекулярная масса этого вещества равна 180. Назовите вещество.
4. Найдите молекулярную формулу углеводорода, массовая доля углерода в котором составляет 75 %. Относительная плотность паров этого вещества по азоту равна 0,572. Назовите вещество.
ВАРИАНТ 5
1. Найдите объем кислорода и воздуха, который израсходовали на сжигание 50 литров метана и 20 литров пропана? Какой объем углекислого газа при этом образовался?
2. Выведите молекулярную формулу углеводорода, содержащего 92,3% углерода. Относительная плотность паров этого вещества по водороду равна 13. Дайте название веществу. Составьте его структурную формулу.
3. Выведите молекулярную формулу органического вещества содержащего 65,75 % углерода, 15,06 % водорода и 19,18 % азота. Относительная плотность паров этого вещества по воздуху равна 2,52. Дайте название веществу.
4. Найдите молекулярную формулу алкена, в котором массовая доля углерода составляет 85,7 %. Относительная плотность вещества по азоту равна 2. Назовите вещество.
ВАРИАНТ 6
1. Какой объем воздуха (н.у.) потребуется для сжигания смеси метана объемом 5 л с этаном объемом 20 л? Какой объем углекислого газа при этом образовался?
2. Найдите молекулярную формулу углеводорода, массовая доля углерода в котором составляет 83,3% углерода. Относительная плотность паров этого вещества по водороду равна 36. Дайте название веществу. Составьте его структурную формулу, дайте ему название
3. Выведите молекулярную формулу органического соединения, содержащего 38,7 % углерода, 16,2 % водорода и азот. Относительная плотность паров этого вещества по водороду равна 15,5. Назовите вещество.
4. Найдите молекулярную формулу органического вещества, если известно, что массовая доля углерода в нем составляет 51,89 %, водорода 9,73 % и хлора 38,38 %. Относительная плотность паров этого вещества по воздуху равна 3,19. Назовите вещество.
ВАРИАНТ 7
1. Сколько литров воздуха израсходовали на сжигание смеси, состоящей из 7 литров метана и 3 литров бутана? Какой объем углекислого газа при этом образовался?
2. Найдите молекулярную формулу алкина, массовая доля углерода в котором составляет 90%. Относительная плотность его по водороду равна 20. Составьте его структурную формулу и дайте ему название.
3. Выведите молекулярную формулу органического вещества, содержащего 53,3 % углерода, 15,6 % водорода и 31,1 % азота. Относительная плотность паров этого вещества по воздуху равна 1,551. Дайте название веществу.
4. Выведите молекулярную формулу органического вещества, содержащего 40 % углерода, 6,7 % водорода и 53,3 % кислорода. Относительная плотность паров этого вещества по водороду равна 15. Дайте название веществу.
ВАРИАНТ 8
1. Какой объем воздуха (н.у.) потребуется для сжигания смеси этана объемом 6 литров с пропаном объемом 4 литра? Какой объем углекислого газа при этом образовался?
2. Найдите молекулярную формулу углеводорода, в котором массовая доля водорода равна 14,3 %. Относительная плотность паров этого вещества по водороду равна 21. Составьте его структурную формулу. Дайте ему название
3. Выведите молекулярную формулу вещества, содержащего 52 % углерода, 35 % кислорода, 13 % водорода. Относительная плотность паров этого вещества по водороду равна 23. Дайте название веществу.
4. Выведите молекулярную формулу органического вещества, содержащего 64,9 % углерода, 21,6 % кислорода и 13,5 % водорода. Относительная плотность паров этого вещества по воздуху равна 2,55. Дайте название веществу.
Критерии оценивания:
- оценка «зачтено»: обучающийся решил 2 задачи (задача 1 – на расчет объема и одна из задач на вывод формулы);
- оценка «хорошо»: обучающийся решил 3 задачи (задача 1 – на расчет объема и 2 задачи на вывод формулы);
- оценка «отлично»: обучающийся выполнил все задания без замечаний
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №2
РЕШЕНИЕ ЗАДАЧ ПО УСТАНОВЛЕНИЮ ФОРМУЛ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА ОСНОВЕ ПРОДУКТОВ СГОРАНИЯ
Цель: научиться находить молекулярную формулу органического соединения по его относительной плотности и продуктам сгорания; составлять их структурные формулы и давать им названия.
ВАРИАНТ 1
1. При сгорании 2,52 г органического соединения выделилось 7,92 г оксида углерода (4) и 3,24 г воды. Относительная плотность этого вещества по воздуху равна 2,9. Выведите молекулярную формулу вещества, составьте формулы трех изомеров и дайте им названия.
2. При сжигании 4,4 г углеводорода получили 13,2 г оксида углерода (4). Относительная плотность вещества по воздуху равна 1,52. Выведите молекулярную формулу этого вещества и дайте ему название.
3. При сжигании алкина массой 5,2 г выделилось 8,96 л оксида углерода (4) (н.у.) и 3,6 г воды. Относительная плотность этого вещества по водороду равна 13. Найдите молекулярную формулу алкина и дайте ему название.
ВАРИАНТ 2
1. При сгорании органического соединения массой 4,2 г получили оксид углерода (4) массой 13,2 г и воду массой 5,4 г. Относительная плотность этого вещества по воздуху равна 2,9. Выведите молекулярную формулу органического соединения, составьте структурные формулы трех изомеров и дайте им названия.
2. Определите молекулярную формулу вещества, при сжигании 3,75 г которого получили 2,25 г водяного пара и 5,5 г оксида углерода (4). Относительная плотность вещества по водороду равна 15.
3. При сгорании органического вещества массой 6,2 г образовалось 4,48 л оксида углерода (4) (н.у.), 9 г воды и азот. Относительная плотность паров вещества по водороду равна 15,5. Выведите молекулярную формулу этого вещества и дайте ему название.
ВАРИАНТ 3
1. При сгорании 4,3 г углеводорода получили 13,2 г оксида углерода (4). Относительная плотность паров этого вещества по водороду равна 43. Выведите молекулярную формулу вещества, составьте формулы трех изомеров и дайте им названия.
2. При сжигании органического вещества массой 9 г образовалось 17,6 г оксида углерода (4), 12,6 г воды и азот. Относительная плотность вещества по водороду равна 22,5. Найдите молекулярную формулу вещества и напишите структурные формулы изомеров, отвечающих этой молекулярной формуле.
3. Сожгли 4,8 г органического вещества, при этом получили 6,6 г оксида углерода (4) и 5,4 г воды. Относительная плотность этого вещества по водороду равна 16. Выведите молекулярную формулу вещества и дайте ему название.
ВАРИАНТ 4
1. При сгорании 3,6 г углеводорода образовалось 11 г оксида углерода (4) и 5,4 г воды. Относительная плотность этого вещества по водороду равна 36. Выведите молекулярную формулу вещества и дайте ему название.
2. При сжигании 9,3г вещества получили 6,72 л оксида углерода (4) (н.у.), 13,5 г воды и азот. Относительная плотность вещества по водороду равна 15,5. Выведите молекулярную формулу этого вещества и дайте ему название.
3. При сгорании 2,24 г углеводорода образовалось 7,04 г оксида углерода (4). Относительная плотность паров этого вещества по водороду равна 56. Выведите молекулярную формулу вещества, составьте формулы трех изомеров и дайте им названия.
ВАРИАНТ 5
1. При сгорании 36 г органического соединения получили оксид углерода (4) массой 52,8 г и воду массой 21,6 г. Относительная молекулярная масса вещества равна 180. Выведите молекулярную формулу этого вещества и дайте ему название.
2. При сгорании 2,76 г органического вещества получили 9,24 г оксида углерода (4) и 2,16 г воды. Относительная плотность вещества по водороду равна 39. Выведите молекулярную формулу этого вещества и дайте ему название.
3. Найдите молекулярную формулу алкадиена, если при сжигании 2 г его образовалось 6,45 г оксида углерода (4). Относительная плотность вещества по водороду равна 48. Составьте структурные формулы трех изомеров и дайте им названия.
ВАРИАНТ 6
1. При сгорании 1,2 г органического соединения получили оксид углерода (4) массой 3,52 г и воду массой 2,16 г. Плотность вещества равна 1,35 г/л. Выведите молекулярную формулу этого вещества и дайте ему название.
2. При сжигании 11,2 г алкена получили 35,2 г оксида углерода (4). Относительная плотность алкена по воздуху 1,93. Найдите молекулярную формулу алкена и дайте ему название.
3. При сгорании углеводорода массой 2,34 г образовался оксид углерода (4) объемом 4,032 л. Относительная плотность паров этого вещества по водороду равна 39. Выведите молекулярную формулу углеводорода и дайте ему название.
ВАРИАНТ 7
1. При сгорании 1,8 г органического соединения образовалось 3,96 г оксид углерода (4) и 1,62 г воды. Относительная плотность паров этого вещества по водороду равна 29. Выведите молекулярную формулу вещества и дайте ему название.
2. При сжигании 3,34 г органического соединения получено 6,6 г оксид углерода (4) и 3,05 г воды. Относительная молекулярная масса этого вещества равна 88. Выведите молекулярную формулу вещества и дайте ему название.
3. При сгорании 3,9 г органического соединения образовалось 13,2г оксида углерода (4) и 2,7 г воды. Относительная плотность этого вещества по водороду равна 39. Выведите молекулярную формулу вещества и дайте ему название.
ВАРИАНТ 8
1. При сжигании 7,8 г ароматического углеводорода получено 26,4 г оксид углерода (4). Относительная плотность вещества по воздуху равна 2,69. Выведите молекулярную формулу этого вещества и дайте ему название.
2. При сжигании органического вещества массой 3,2 г образовалось 9,9 г оксида углерода (4) и 4,5 г воды. Относительная плотность паров этого вещества по водороду равна 63. Найдите молекулярную формулу углеводорода, дайте ему название
3. При полном сжигании 0,7 г органического вещества получили 1,12 л оксида углерода (4) (н.у.) и 0,9 г воды Относительная плотность по водороду равна 42. Определите молекулярную формулу этого углеводорода, составьте формулы трех изомеров и дайте им названия.
Критерии оценивания:
- оценка «зачтено»: обучающийся решил 1 задачу на вывод формулы с подробными объяснениями;
- оценка «хорошо»: обучающийся решил 2 задачи на вывод формулы (одна задача должна быть с подробными объяснениями);
- оценка «отлично»: обучающийся решил все задачи на вывод формул без замечаний (одна задача должна быть с подробными объяснениями).
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 3
СОСТАВЛЕНИЕ СТРУКТУРНЫХ ФОРМУЛ ИЗОМЕРОВ АЛКАНОВ, НОМЕНКЛАТУРА
Цель: закрепить знания о строении, гомологии, изомерии алканов; научиться составлять формулы изомеров алканов, давать им названия по систематической и рациональной номенклатуре.
ВАРИАНТ 1
1. Строение алканов на примере этана (молекулярная, структурная, электронная формулы, валентное состояние атомов углерода, характеристика). Причины инертности алканов.
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
СН3 С2Н5СН3 СН3
I ll 1 I
а) СН3-СН-СН-СН2-СН-СН3 б) СН3-СН-С-СН3 в) СН3-С-СН-СН3
ll ll ll l l
СНз С2Н5 СНз С2Н5С2Н5
СНз
I
Г) СН3-СН2-СН-СН2-СН3 д) СН3-С-СН3
[ I
С2Н5 СНз
3. Составьте структурные формулы для следующих веществ:
А) 2-метилбутан
Б) 3-этилпентан
В) 3,4-диметилгептан
Г) 2,4-диметил-З-этилгексан
Д) 2,2-диметилпропан
Е) 3,4,4-триэтилоктан
Ж) 2,3-диметил-3,4-диэтилгептан
3) 3,3,5-триэтилоктан
Для трех любых соединений дайте названия по рациональной номенклатуре
4. Задача
На полное сгорание октана было израсходовано 50 моль кислорода. Вычислите массу сгоревшего октана
ВАРИАНТ 2
1. Строение алканов на примере пропана (молекулярная, структурная, электронная формулы, валентное состояние атомов углерода, характеристика). Причины зигзагообразного строения молекул алканов в пространстве
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
С2Н5
I
а) СН3-СН2-СН-СН3 б) СН3-СН-СН3 в) СН3-СН-СН-СН3
l I I
СН3 С2Н5 СН3
СН3 СН3 СН3
I I l
Г) СН3-СН2-С-СН2-СН3 д) СНз-С - СН-СНз е) СН3-СН-СН3
l I I
СН3 СН3 СН3
3. Составьте структурные формулы для следующих веществ:
А) 4,4-диметилгептан
Б) 2,3-диметил-3-этилгексан
В) 2,2-диметилпентан
Г) 3-метил-4,4-диэтилоктан
Д) 2,4-диметилпентан
Е) 3,3-диэтилгептан
Ж) 3-метил-2,4-диэтил--7-пропилоктан
3) 3,4-диметил октан
Для трех любых соединений дайте названия по рациональной номенклатуре
4. Задача
Какой объем пропана подвергся процессу дегидрирования, если в результате реакции образовался пропилен и выделилось 11,2 литров водорода (н.у.)?
ВАРИАНТ 3
1. Строение алканов на примере бутана (молекулярная, структурная, формулы, валентное состояние атомов углерода, характеристика). Нахождение алканов в природе
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
СН3 СН3 СН3
I I I
а) СНз-СНз б) СН3-СН2-СН-СН3 в) СН3-СН-С-СН2 -СН3
I
С2Н5
С2Н5 СНз
I I
Г) СН3-СН2-СН-СН2-СН3 д)СН3-СН-СНгСН-СН2-СН3 е)СН3-СН-СН3
I I
СНз С2Н5
3. Составьте структурные формулы для следующих веществ:
А) 3-метилпентан.
Б) 3-этилгексан
В) 2,3-диметилбутан
Г) 2,3,3-триметилгексан
Д) 2,3-диметил-3-этилпентан.
Е) 3-метил-4,4-диэтилгептан
Ж) 3,4-диэтилоктан
З) 3,3,4-триметил- 4-этилоктан
Для трех любых соединений дайте названия по рациональной номенклатуре
4. Задача
Какой объем воздуха понадобится для того, чтобы сжечь 56 литров бутана (н.у.)?
ВАРИАНТ 4
1. Строение алканов на примере пентана (молекулярная, структурная, формулы, валентное состояние атомов углерода, характеристика). Причины сжигания попутного газа при условии его неполной переработки
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
СНз СН3 СНз
I
I I
а) СН3-С-СН3 б) СН3-С-СН2-СН3 в) СН3-СН-СН-СН3
I I I
СНз С2Н5 СНз
С2Н5 СНз
I I
г) С2Н5-СН-С2Н5 д) СН3-СН-СН2-СН3 е) СН3-СН2-СН2-С-СН3
I I
СН3 СНз
3. Составьте структурные формулы для следующих веществ:
А) 2-метилпропан
Б) 3,4-диэтилгексан
В) 2,3-диметил-4 -этил гептан
Г) 2,4,4-триметилгептан
Д) 3,3-диметил-4,4-диэтил октан
Е) 3,4-диэтил-4-проиилнонан
Ж) 3,5-диэтил октан
З) 3-пропилгексан
Для трех любых соединений дайте названия по рациональной номенклатуре
4. Задача
Какой объем пропана (н.у.) можно сжечь в 350 л кислорода (н.у.)?
ВАРИАНТ 5
1. Строение алканов на примере гексана (молекулярная, структурная, формулы, валентное состояние атомов углерода, характеристика). Болотный газ и его особенности
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
СНз СНз
1 I
а) СН3-СН-СН-СН-СН3 б) С2Н5-СН-СН2-СН3 в) С2Н5-СН-С2Н5
1 I I
СНз СНз СНз
СНз
I
г) С2Н5-СН-СН2-СН-СН3 д) СН3-СН-С-СН3 е) СН3-СН-СН2-СН3
| l I I I
СН3 СН3 СН3 СН3 СН3
3. Составьте структурные формулы для следующих веществ:
А) 3-метилгептан
Б) 3,4-диэтилгексан
В) 2,4-диметил-3,3-диэтил октан
Г) 2,5-диметилгептан
Д) 2-метилпропан
Е) 2,2,4-триметилоктан
Ж) 3,4,4-триэтилнонан
З) 2,4,4,5-тетраметилдекан
Для трех любых соединений дайте названия по рациональной номенклатуре
4. Задача
Какой объем воздуха потребуется на сжигание 6,72 л этана (н.у)? Найдите объем выделившегося углекислого газа
ВАРИАНТ 6
1. Строение алканов на примере гептана (молекулярная, структурная, формулы, валентное состояние атомов углерода, характеристика). Физические свойства алканов
2. Дайте названия следующим алканам по систематической и рациональной номенклатуре:
СНз СНз СНз
I I I
а) С2Н5-СН2-СН3 б) СН3-СН-СН2-СН3 в) СН3-С-СН2-СН-СН3
I
С2Н5
СНз СНз СНз СН3 С2Н5
1 \ / I I
г) СН3-СН-СН3 д) СН3-С-СН2-СН3 е) СН3-СН-СН-СН-СН3
I
С2Н5
3. Составьте структурные формулы для следующих веществ:
А) 3-метилпентан
Б) 3-этилпентан
В) 2,3-диметилбутан
Г) 2,3,3-триметилгексан
Д) 2,3-диметил-3-этилпентан
Е) 3-метил-3,4-диэтилгептан
Ж) 3,4-диэтилоктан
З) 3,3,4-триметил-4-этил октан
4. Задача
Сожгли смесь, состоящую из 3 л метана и 3 л пропана. Какой объем воздуха при этом потратили? (Объемы газов измерены при н.у.)
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 3 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 4 задания с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 4
ХИМИЧЕСКИЕ СВОЙСТВА И ПОЛУЧЕНИЕ АЛКАНОВ
Цель: повторить и закрепить знания по химические свойствам и способам получения алканов
ВАРИАНТ 1
1. Дайте названия углеводородам по систематической и рациональной номенклатуре. Укажите, какие из веществ являются изомерами:
а) СН3СН2СН2СН2СН3
б) СН3СНСНСН2СН3;
│ │
СН3 СН3
в) Н3ССНСН3;
l
СН3
г) СН3СНСНСН3
│ │
СН3 СН3
д) СН3
│
СН3ССН2СН2СН3
│
СН3
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
ССН4СН3Вr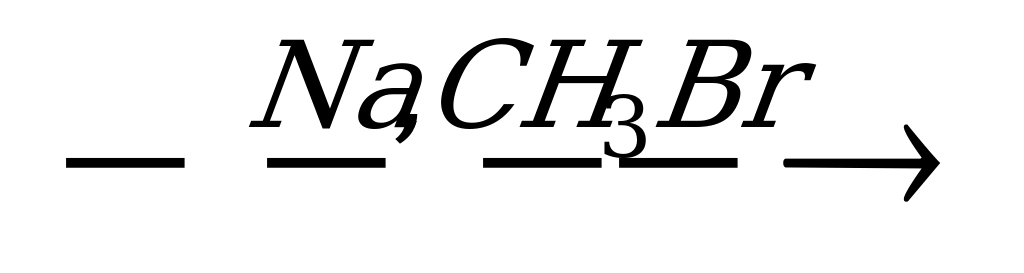 C2H6CO2
C2H6CO2
3. Напишите уравнение реакции получения 2,4-диметилпентана. Дайте названия исходным галогенпроизводным углеводородам
ВАРИАНТ 2
1. Дайте названия углеводородам по систематической и рациональной номенклатуре. Укажите, какие из веществ являются изомерами:
а) СН3СН2СНСН2СН3;
l
СН3
б) СН3СНСНСН3;
l l
СН3 СН3
в) СН3СНСН2СН3;
l
СН3
г) СН3
l
СН3С СНСН3;
│ │
СН3СН3
д) СН3
│
СН3ССН2СН3;
│
СН3
2. Напишите уравнения реакций: а) термического разложения метана; б) первой стадии хлорирования этана; в) изомеризации пентана (укажите условия протекания реакции); г) горения пропана в кислороде
3. Напишите уравнение реакции получения 3,5-диметилгептана. Дайте названия исходным галогенпроизводным углеводородам
ВАРИАНТ 3
1. Дайте названия углеводородам по систематической и рациональной номенклатуре. Укажите, какие из веществ являются изомерами:
а) СН3СН2СН2СН3;
б) СН3СНСНСН3;
│ │
СН3 С2Н5
в) СН3СН2СНСН3;
│
СН3
г) СН3
│
СН2ССН3;
│ │
СН3 СН3
д) СН3СН2СНСН2СН3 ;
│
СН3
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этанбромэтан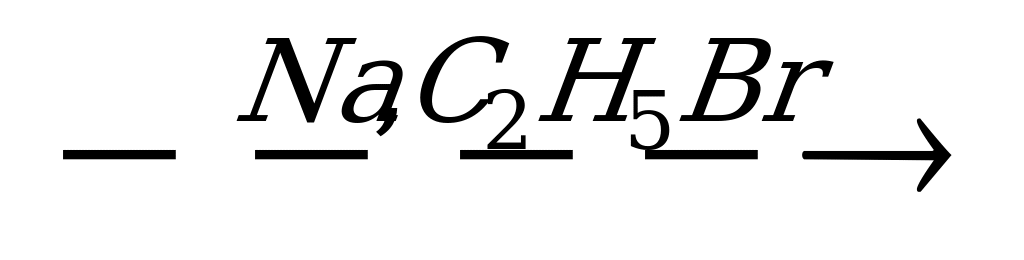 бутанизобутаноксид углерода (IV).
бутанизобутаноксид углерода (IV).
3. Напишите уравнение реакции получения 2, 3-диметилбутана. Дайте названия исходным галогенпроизводным углеводородам
ВАРИАНТ 4
1. Дайте названия углеводородам по систематической и рациональной номенклатуре. Укажите, какие из веществ являются изомерами:
а) СН3СН2СН3;
б) СН3СНСН2СН3;
│
С2Н5
в) СН3
│
СН3СНСНСН3;
│
СН3
г) СН3
│
СН3ССН2СН3;
СН3
д) СН3
l
 СН3ССН3
СН3ССН3
│
 СН3
СН3
2. Напишите уравнения реакций: а) горения метана в кислороде; б) дегидрирования этана; в) первой и второй стадий хлорирования метана; в) получения синтез-газа из метана.
3. Напишите уравнение реакции получения 3, 4-диметилгексана. Дайте названия исходным галогенпроизводным углеводородам
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 2 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 3 задания с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 5
НОМЕНКЛАТУРА И ИССЛЕДОВАНИЕ СВОЙСТВ ЦИКЛОАЛКАНОВ
Цель: закрепить знания о строении, свойствах, получении и применении циклоалканов. Научиться писать формулы циклоалканов, их изомеров и давать им названия, уравнения химических реакций и получения.
ВАРИАНТ 1
1. Напишите формулы четырех изомеров для вещества бромциклогексан. Дайте им названия
2. Напишите структурные формулы органических соединений по названиям:
а) 1-метил,2-этилциклопропан;
б) 1, 2, 3- триметилциклогексан
3. Напишите уравнение реакции получения циклоалкана из 1,3-дибромбутана.
Напишите уравнения реакций взаимодействия полученного вещества с водородом и хлором. Дайте названия полученным веществам
4. Составьте уравнение реакции получения 1-метил, 2-этилциклопропана при взаимодействии с металлическим магнием. Дайте названия исходным дигалогеналканам. Напишите уравнение реакции горения полученного вещества
5. Определите формулу циклоалкана, если известно, что его относительная плотность по воздуху равна 2,41. Напишите уравнение реакции нитрования для полученного циклоалкана
ВАРИАНТ 2
1. Напишите формулы четырех изомеров для вещества метилциклопентан. Дайте им названия
2. Напишите структурные формулы органических соединений по названиям:
а) 1,1-диметил,2-этилциклопентан;
б) 1, 2- диметилциклобутан
3. Напишите уравнение реакции получения циклоалкана из 1,5-дибромгексана.
Напишите уравнения реакций взаимодействия полученного вещества с водородом и хлором. Дайте названия полученным веществам
4. Составьте уравнение реакции получения 1,2-диметилциклобутана при взаимодействии с металлическим магнием. Дайте названия исходным дигалогеналканам. Напишите уравнение реакции горения полученного вещества
5. Определите формулу циклоалкана, если известно, что его относительная плотность по воздуху равна 1,931. Напишите уравнение реакции гидрирования для полученного циклоалкана
ВАРИАНТ 3
1. Напишите формулы четырех изомеров для вещества пропилциклопропан. Дайте им названия
2. Напишите структурные формулы органических соединений по названиям:
а) 1-хлор, 1-метилциклобутан;
б) 1- метил, 2-этил, 3- пропилциклопентан
3. Напишите уравнение реакции получения циклоалкана из 1,3-дибромпропана.
Напишите уравнения реакций взаимодействия полученного вещества с водородом и хлором. Дайте названия полученным веществам
4. Составьте уравнение реакции получения пропилциклобутана при взаимодействии с металлическим магнием. Дайте названия исходным дигалогеналканам. Напишите уравнение реакции горения полученного вещества
5. Определите формулу циклоалкана, если известно, что его относительная плотность по воздуху равна 2,9. Напишите уравнение реакции бромирования для полученного циклоалкана
ВАРИАНТ 4
1. Напишите формулы четырех изомеров для вещества хлорциклопентан. Дайте им названия
2. Напишите структурные формулы органических соединений по названиям:
а) 1-метил,2,2-диэтилциклогексан;
б) 1-бром, 2, 3- диметилциклобутан
3. Напишите уравнение реакции получения циклоалкана из 1,6-дибромгексана.
Напишите уравнения реакций взаимодействия полученного вещества с водородом и хлором. Дайте названия полученным веществам
4. Составьте уравнение реакции получения 1-метил, 2-этилциклопентана при взаимодействии с металлическим магнием. Дайте названия исходным дигалогеналканам. Напишите уравнение реакции горения полученного вещества
5. Определите формулу циклоалкана, если известно, что его относительная плотность по водороду равна 28. Напишите уравнение реакции нитрования для полученного циклоалкана
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 3 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 4 задания с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №6
АЛКЕНЫ: ИЗОМЕРИЯ, НОМЕНКЛАТУРА, СВОЙСТВА
Цель: повторить и углубить знания о способах получения, химических свойствах , изомерии и номенклатуре алкенов
ВАРИАНТ 1
1. Напишите уравнение реакции крегинга октана, дегидрирования бутана, дегидратации пропанола. Дайте название полученным веществам
2. Напишите уравнения химических реакций: а) гидратации, б) галогенирования, в) гидрогалогенирования пропена.
Укажите условия химических реакций. Дайте названия полученным веществам
3. Для вещества, имеющего строение СН2=СНСН2СН2СН3, составьте
формулы:
а) изомера положения кратной связи; б) ближайшего гомолога; в) изомера углеродной цепи. Дайте веществам названия по систематической и рациональной номенклатуре
4. Даны вещества бутан и бутен. В каком из данных веществ наибольшее содержание углерода? Каким пламенем будут гореть данные вещества? Подтвердите расчетами
ВАРИАНТ 2
1. Напишите уравнение реакции крегинга нонана, дегидрирования пентана, дегидратации 3-метил,2-бутанола. Дайте название полученным веществам
2. Напишите уравнения химических реакций: а) гидратации, б) галогенирования, в) гидрогалогенирования 1-бутена. Укажите условия химических реакций. Дайте названия полученным веществам
3. Для вещества, имеющего строение CH2=CНCHCH3, составьте формулы:
│
СН3
а) гомолога; б) изомера углеродной цепи; в) межклассового изомера. Дайте названия веществам названия по систематической и рациональной номенклатуре
4. Пользуясь раздаточным материалом, составьте таблицу: Применение алкенов
| Название | Молекулярная и структурная формулы | Получение | Применение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вывод:основное применение алкенов
ВАРИАНТ 3
1. Напишите уравнение реакций: а) крегинга гексана, б) дегидрирования пропана, в) дегидрогалогенирования 1-бром,2-метилбутана.
Дайте название полученным веществам
2. Напишите уравнения химических реакций: а) гидратации, б) галогенирования, в) гидрогалогенирования 2-бутена. Укажите условия химических реакций. Дайте названия полученным веществам
3. Напишите формулы алкенов по названиям: а) 3,3-диметил,1-пентен;
б) 4,5-диметил,2-гексен; в) 2,3,3-триметил,1-бутен; г) 2,3-диметил,2-бутен. Дайте названия веществам А, В, Г по рациональной номенклатуре. Для вещества Г составьте формулы геометрической изомерии
4. Найдите молекулярную формулу алкена, если 682,5г этого вещества могут присоединить 216,9л водорода
ВАРИАНТ 4
1. Напишите уравнение реакции крегинга 2,4-диметилгексана, дегидрирования этана, дегалогенирования 2,3-дибромбутана. Дайте название полученным веществам
2. Напишите уравнения химических реакций: а) гидратации, б) галогенирования, в) гидрогалогенирования 1-пентена
3. Напишите структурные формулы алкенов по названиям: а) 2,3-диметил,1-бутен; б) 3-метил,2-пентен; в) 2-метил,1-пентен; 2,3-диметил,2-бутен. Дайте названия веществам по рациональной номенклатуре. Чем являются эти веществапо отношению друг другу. Найдите изомеры по положению кратной связи. Напишите 2 примера межклассовой изомерии
4. Пользуясь раздаточным материалом, составьте таблицу: Применение алкенов
| Название | Молекулярная и структурная формулы | Получение | Применение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вывод: основное применение алкенов
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 3 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 4 задания с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
РАЗДАТОЧНЫЙ МАТЕРИАЛ
ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ ОТДЕЛЬНЫХ ПРЕДСТАВИТЕЛЕЙ АЛКЕНОВ
Этилен (этен) – бесцветный газ, горящий на воздухе коптящим пламенем. Широко применяют для синтеза различных органических веществ: этилового спирта, стирола, галогенпроизводных, полиэтилена и т.д. Кислородно-этиленовым пламенем можно резать и сваривать металлы. С воздухом этилен образует взрывоопасные смеси.
Пропилен (пропен) – бесцветный газ. Выделяется из газов нефтепереработки. В лабораторных условиях можно получать, пропуская пары пропилового или изопропилового спирта над оксидом алюминия при температуре 300 – 400о. Служит сырьем для получения изопропилбензола, ацетона, фенола, глицерина, акрилонитрила, синтетического каучука, изопропилового спирта и т.д.
Бутилены (1-бутен и 2-бутен), изобутилен (2-метилпропен) С4Н8 можно выделять из газов крекинга и пиролиза нефти, также из природных газов. 1-бутен применяют для получения 1,3-бутадиена и изооктана. 2-бутен используют в качестве среды для полимеризации 1,3-бутадиена. Из изобутилена получают изооктан и изопрен.
ПОМНИТЕ, что алкены применяют в основном в качестве мономеров для производства высокомолекулярных соединений.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №7
СОСТАВЛЕНИЕ СТРУКТУРНЫХ ФОРМУЛ, НОМЕНКЛАТУРА И ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Цель: повторить и углубить знания о химических свойствах, изомерии и номенклатуре алкинов. Научиться осуществлять цепочки превращений углеводородов и решать расчетные задачи
ВАРИАНТ 1
1. Для вещества, имеющего строение СНССН2СН2СН3, дайте название, составьте формулы:
а) изомера положения тройной связи;
б) ближайшего гомолога;
в) изомера углеродной цепи.
Дайте всем веществам названия по систематической и рациональной номенклатуре.
2. Напишите уравнения реакций взаимодействия пропина с избытком веществ:
водорода, бромоводорода, хлора, аммиачного раствора оксида серебра.
Укажите условия протекания химических реакций. Дайте названия продуктам реакций
3. Дайте названия веществам по систематической номенклатуре:
а) Н3С – СН – СН – С С – СН3 б) Н3С – С ≡ С – СН – СН2 – СН3
│ │ │
СН3 СН3 С2Н5
в) НС С – СН2 – СН – СН2 – СН – СН3 г)Н3С – С = С – СН = СН2
│ │ │ │
СН3 СН3 СН3 СН3
4. Задача
Рассчитайте объем кислорода и воздуха, необходимые для сжигания 20г 2-бутина
ВАРИАНТ 2
1. Для вещества, имеющего строение НС С – СН – СН3
│
СН3
дайте название и составьте формулы:
а) изомера углеродной цепи;
б) ближайшего гомолога;
в) изомера из другого класса углеводородов.
Дайте всем веществам названия по систематической и, где возможно, по рациональной номенклатуре
2. Осуществите цепочку превращений:
CaC2C2H2C2H4C2H5BrC4H10
Напишите уравнения реакций в структурном виде, укажите условия реакций, дайте названия полученным веществам
3. Напишите структурные формулы следующих веществ:
а) 3 – метил,3 – этил,1 – гексин;
б) 3, 4 – диметил,1 – пентин
в) 3, 3 – диметил, 1 – бутин
г) 2, 3 – диметил, 3- этил, 1,4- пентадиен
Для вещества «в» дайте название по рациональной номенклатуре
4. Задача
Какой объем ацетилена (н.у.) можно получить из карбида кальция массой 80 г, содержащего 10% примесей?
ВАРИАНТ 3
1. Напишите структурную формулу вещества: 1-пентин
Напишите формулы трех изомеров и двух ближайших гомологов.
Дайте им названия по систематической и, где возможно, рациональной номенклатуре
2. Напишите структурные формулы и сравните строение молекул пропена и пропина. Что у них общего? В чем различия?
Напишите уравнения реакций для данных веществ:
а) галогенирования (с бромом);
б) гидрогалогенирования (с бромоводородом);
в) гидратации (с водой)
г) замещения (с гидроксидом диамин серебра)
Уравнения реакций напишите в структурном виде, укажите условия проведения реакций, дайте названия полученным веществам по систематической номенклатуре.
Какое вещество более химически активно и почему?
3. Осуществите цепочку превращений:
СН4C2H2C6H6
↓
С2Н4О
Напишите уравнения реакций в структурном виде, укажите условия реакций, дайте названия полученным веществам
4. Даны вещества: бутан, бутен, бутин. В каком из данных веществ наибольшее содержание углерода? Подтвердите расчетами.
Каким пламенем будут гореть данные вещества?
ВАРИАНТ 4
1. Используя раздаточный материал, заполните таблицу «Применение алкинов»
| Молекулярная формула и название УВ по систематической номенклатуре | Структурная формула и название УВ по рациональной номенклатуре | Физические свойства | Действие на живые организмы | Применение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вывод: (основное применение полиинов)
2. Составьте формулы следующих веществ, выберите изомеры:
а) 3-метил, 1- пентин;
б) 2- пентин;
в) 2- метил, 1,3- бутадиен;
г) 1,4- гексадиен
3. Как из ацетилена в две стадии получить циклогексан? Напишите уравнения реакций и укажите условия их протекания?
4. Даны вещества: пропан, пропен, пропин. В каком из данных веществ наибольшее содержание углерода? Подтвердите расчетами.
Каким пламенем будут гореть данные вещества?
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 3 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 4 задания с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
РАЗДАТОЧНЫЙ МАТЕРИАЛ
ПРИМЕНЕНИЕ АЛКИНОВ
Алкины являются сырьем для производства большого количества органических соединений и материалов: альдегидов, кетонов, растворителей (тетрагалогенэтанов), исходных веществ для получения синтетических каучуков, поливинилхлорида и других полимеров.
Ацетилен является ценнейшим горючим с очень высокой теплотой горения.
ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ И ИХ
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ
АЦЕТИЛЕН (НС ≡ СН) – бесцветный газ, температура кипения:
-83,6оС, плохо растворяется в воде, растворим в ацетоне. Применяется в производстве винилхлорида, ацетальдегида, акрилонитрила, винилацетата, тетрахлорэтилена, а также при сварочных работах. Обладает слабым наркозным действием, в смеси с воздухом вызывает удушье.
ПРОПИН (метилацетилен), Н3С - С ≡ СН – бесцветный газ с неприятным запахом, температура плавления: -104,7оС, температура кипения: -23,2оС, плохо растворяется в воде, хорошо растворим в диэтиловом эфире, спиртах и других органических растворителях, пожароопасен. В смеси с воздухом взрывоопасен. Обладает слабым наркозным действием.
1 – БУТИН (этилацетилен), Н3С – СН2 – С ≡ СН – бесцветный газ, температура плавления: -122,5оС, температура кипения: -8,6оС, не растворяется в воде, растворяется в большинстве органических растворителей.
1 –БУТЕН, 3 – ИН (винилацетилен), Н2С = СН – С ≡ СН – бесцветный газ, температура плавлении: -138оС, температура кипения: -5,5оС. Плохо растворяется в воде, растворяется в большинстве органических растворителей, легко окисляется и полимеризируется. Смеси с воздухом взрываются. Применяется для получения хлоропрена. Раздражает слизистые оболочки, обладает наркозным действием.
3 – МЕТИЛ,1 – БУТИН (изопропилацетилен) – летучая жидкость, температура кипения: 32ОС, не растворяется в воде, растворим в большинстве органических растворителей. Обладает слабым наркотическим действием.
ПОЛИАЦЕТИЛЕНЫ (полиины). Некоторые из них, особенно с спряженными тройными связями, разлагаются со взрывом. Применяются для получения особой группы ароматических углеводородов (аннуленов).
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №8
АРЕНЫ: ИЗОМЕРИЯ, НОМЕНКЛАТУРА, СВОЙСТВА
Цель: закрепить знания о строении и свойствах аренов. Уметь составлять формулы изомеров и давать им названия, осуществлять цепочки превращений, решать задачи различных типов
ВАРИАНТ 1
1. Строение бензола: главный признак аренов, правило Хюккеля, показать противоречие формулы Кекуле
2. Получение аренов: в промышленности и в лаборатории:
- ароматизация парафинов;
- тримеризация ацетилена;
- реакция Вюрца – Фиттига (получить пропилбензол);
- реакция Фриделя – Крафтса (получить бутилбензол
Уравнения реакций запишите в структурном виде. Укажите условия реакций
3. Задача
Вычислите массу нитробензола, полученного при взаимодействии 15,6г бензола с 15г азотной кислоты. Какое вещество взято в избытке. Найдите массу избытка
Дополнительно:
Осуществите цепочку превращений. Уравнения реакций запишите в структурном виде, укажите условия реакций.
циклогексан → бензол →бромбензол→толуол→трибромтолуол
↓
углекислый газ
ВАРИАНТ 2
1. Химические свойства бензола:
а) реакция нитрования;
б) реакции галогенирования в присутствии катализатора и на свету;
в) реакция сульфирования.
Уравнения реакций запишите в структурном виде, укажите условия реакций, дайте названия полученным веществам, определите тип реакции
Почему реакции замещения у ароматических углеводородов идут легче, чем присоединения?
Каким пламенем будет гореть бензол? Подтвердите расчетами
2. Написать изомеры для вещества бутилбензол: по три изомера для двухзамещенных и трехзамещенных.
Дайте названия всем изомерам
3. Задача
Определите молекулярную формулу углеводорода, содержащего 91,3% углерода. Относительная плотность паров этого вещества по воздуху равна 3,17. Напишите его структурную формулу и дайте название
Дополнительно:
Напишите структурные формулы следующих веществ:
а) бромбензол; б) 1,3 –диметил, 5 – хлорбензол; в) о – диэтилбензол;
г) м – динитробензол; д) пропилбензол
ВАРИАНТ 3
1. Применение аренов (оформите таблицу)
| Названия аренов | Формулы (молекулярная и структурная) | Применение аренов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вывод:
2. Осуществите цепочку превращений:
С7Н8
↑
С2Н2 → С6Н6 → С6Н5-NO2
↓
С6Н6Cl6
Уравнения реакций запишите в структурном виде. Укажите условия реакций. Дайте названия продуктам реакций
3. Задача
Какую массу бензола можно получить из 33,6л (н.у) ацетилена, если выход продукта составляет 80% от теоретически возможного
Дополнительно:
Напишите структурные формулы следующих веществ:
а) нитробензол; б) 1,2 –диметил, 5 –пропилбензол; в) м – динитробензол;
г) о – дибромбензол; д) 1,2,3- триэтилбензол
ВАРИАНТ 4
1. Химические свойства толуола:
а) реакция нитрования;
б) реакции галогенирования при катализаторе и на свету;
в) реакция гидрирования
Уравнения реакций запишите в структурном виде, укажите условия реакций, дайте названия полученным веществам, определите тип реакций.
Почему толуол в реакции замещения вступает легче, чем бензол?
Каким пламенем будет гореть толуол? Подтвердите расчетами
2. Для вещества о-хлорпропилбензол составьте формулы четырех изомеров.
Дайте названия всем веществам
3. Задача
Какой объем водорода (н.у.) присоединится к 156г бензола при его гидрировании. Какая масса циклогексана образуется, если выход продукта составляет 75% от теоретически возможного?
Дополнительно:
Осуществите цепочку превращений. Уравнения реакций запишите в структурном виде, укажите условия реакций.
циклогексан → бензол →бромбензол→толуол→трибромтолуол
↓
углекислый газ
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 2 задания с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 3 задания (задачу можно поменять на дополнительное занятие) с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.
РАЗДАТОЧНЫЙ МАТЕРИАЛ
ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
1.Бензол – сырье для производства различных продуктов: нитробензола, хлорбензола, анилина, фенола, стирола и т. д.
2. Толуол – для производства красителей, лекарственных и взрывчатых веществ (тротил), исходный продукт для получения СМС, хороший растворитель.
3. Этилбензол – для получения стирола (винилбензола), который легко полимеризуется и используется для получения полимеров полистирола и бутадиенстирольного каучука.
4. Ксилолы (диметилбензолы).
Технический ксилол – смесь трех изомеров (о-, м-,п-) – применяют в качестве растворителя.
Разделить их сложно, т.к. температуры кипения их близки, но иногда разделяют. О-ксилол используют для получения фталевого ангидрида (ангидрид фталевой – бензолдиовой кислоты). П-ксилол – для получения терефталевой кислоты (п-фталевая кислота), является сырьем для производства синтетического волокна – лавсан.
5. Изопропилбензол (кумол) – используют для одновременного
получения фенола и ацетона.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №9
УГЛЕВОДОРОДЫ
Цель: обобщить и систематизировать знания по разделу органической химии Углеводороды. Уметь сравнивать углеводороды различных классов по химическим свойствам, делать вывод, осуществлять цепочки превращений, решать задачи различных типов
ВАРИАНТ 1
1. Сравните по химическим свойствам метан и бензол. (Найдите сходство и отличие). Запишите соответствующие уравнения реакций
2. Дано вещество состава С5Н10 . Напишите пять изомеров и дайте им названия.
3. Осуществите превращения:
С2Н2 → С2Н4→ С2Н6 → С2Н5Cl
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам.
4. Задача
Определите объем водорода (н.у.), который можно присоединить к 15 литрам пропена. Найдите массу полученного пропана.
ВАРИАНТ 2
1. Сравните по химическим свойствам этен и ацетилен. (Укажите сходство и отличие). Запишите соответствующие уравнения реакций
2. Дано вещество 3-метил, 1,3-пентадиен, составьте его формулу, запишите формулы двух его гомологов и двух изомеров. Дайте им названия
3. Осуществите превращения:
С6Н14 → С6Н6 → С6Н6Cl6
↓
С6Н5NO2
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам
4. Задача
При нитровании бензола массой 117 г получено 180 г нитробензола. Сколько это составляет процентов от теоретически возможного выхода?
ВАРИАНТ 3
1. Сравните по химическим свойствам бутан и 1,3-бутадиен. (Найдите сходство и отличие). Запишите соответствующие уравнения реакций
2. Дано вещество состава С5Н8 . Напишите 5 формул изомеров и дайте им названия
3. Осуществите превращения:
С → СН4→ СН3Cl → С2Н6
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам
4. Задача
Определите формулу красителя анилина, если массовая доля углерода в нем 77,4%, водорода – 7,5%, азота 15,1%. Относительная плотность этого вещества по воздуху равна 3,21.
ВАРИАНТ 4
1. Сравните по химическим свойствам бензол и толуол. (Укажите сходство и отличие). Запишите соответствующие уравнения реакций
2. Составьте формулы следующих веществ:
а) о-метилэтилбензол, б) п-диэтилбензол, в) о-диметилбензол,
г) м-диметилбензол, д) п-диметилбензол, е) м-метилэтилбензол,
ж) п-метилэтилбензол, з) о-метилпропилбензол.
Выберите изомеры
3. Осуществите превращения:
СН4 → С2Н2 → С6Н6 → С6Н12
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам.
4. Задача
Найдите массу бензола, который необходим для получения 4 кг гексахлорциклогексана.
ВАРИАНТ 5
1. Сравните по химическим свойствам пропан и пропен. (Найдите сходство и отличие). Запишите соответствующие уравнения реакций
2. Дано вещество 4,5,5-триметил,2-гексен. Напишите формулы двух его гомологов и двух изомеров, дайте им названия
3. Осуществите превращения:
СаС2 → С2Н2→ СН3CОН → СО2
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам
4. Задача
Определите формулу органического вещества, если массовая доля углерода в нем 80%, водорода – 20%. Относительная плотность этого вещества по водороду равна 15.
ВАРИАНТ 6
1. Сравните по химическим свойствам бензол и ацетилен. (Укажите сходство и отличие). Запишите соответствующие уравнения реакций
2. Составьте формулу бутилбензола. Предложите формулы двух гомологов и четырех изомеров, дайте им названия.
3. Осуществите превращения:
С2Н6 → С2Н5Cl → С4Н10 → СО2
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам
4. Задача
Определите объем кислорода и воздуха, который необходим для сжигания 210 л ацетилена
ВАРИАНТ 7
1. Сравните по химическим свойствам этан и этен. (Найдите сходство и отличие). Запишите соответствующие уравнения реакций
2. Дано вещество 1-хлор,2-пропилбензол. Напишите формулы двух его гомологов и двух изомеров, дайте им названия.
3. Осуществите превращения:
С6Н6 → С6Н5Br→ С6Н5CН3 → С6Н5CООН
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам.
4. Задача
Вычислите массу нитробензола, полученного при действии на 15,6 г бензола 15 г азотной кислоты.
ВАРИАНТ 8
1. Сравните по химическим свойствам этан и ацетилен. (Укажите сходство и отличие). Запишите соответствующие уравнения реакций
2. Составьте формулу 3,3-диметил,1-гексена. Предложите формулы двух гомологов и четырех изомеров, дайте им названия
3. Осуществите превращения:
СН4→ С2Н2→ С2Н4Cl2
↓
CO2
Запишите уравнения реакций, укажите их условия, дайте названия полученным веществам
4. Задача
Определите объем кислорода и воздуха, который необходим для сжигания 210 л ацетилена
Критерии оценивания:
- оценка «зачтено»: обучающийся выполнил 2 задания (задание 1 обязательно) с незначительными замечаниями;
- оценка «хорошо»: обучающийся выполнил 3 задания (задание 1 обязательно) с незначительными замечаниями;
- оценка «отлично»: обучающийся выполнил все задания без замечаний.






 СН3ССН3
СН3ССН3


















