
Республика Татарстан
Г.Нижнекамск
МБОУ «Средняя общеобразовательная школа №7»
Общая
характеристика
серы
Выполнила:
Учитель химии и биологии
Губарева Вера Александровна
11/15/16
Губарева В.А.

Общая характеристика серы
11/15/16
Губарева В.А.

1
- Историческая справка.
- Историческая справка.
2
- Нахождение в природе.
- Нахождение в природе.
3
- Положение в ПСХЭ. Строение атома.
- Положение в ПСХЭ. Строение атома.
4
- Строение и физические свойства.
- Строение и физические свойства.
5
- Химические свойства.
- Химические свойства.
6
7
8
- Проверь свои знания!
- Проверь свои знания!
Общая характеристика серы
Содержание
11/15/16
Губарева В.А.

11/15/16
Историческая справка
- Элементарную природу серы установил
француз (по
образованию юрист, а по призванию химик)
в своих опытах по сжиганию в 1770 году..
- Древнерусское название "сера"
употребляется очень давно. Оно происходит от
санскритского слова "сира", что означает светло-желтый.
Антуан Лоран Лавуазье
- Химический символ Дальтона
S
- Химический символ Берцелиуса
11/15/16
Губарева В.А.
сера

Нахождение в природе
В земной коре в свободном и связанном состоянии серы находится 0,03% от общего количества атомов, по массе – 0,05%.
Самородная сера - S
Глауберова соль – Na 2 SO 4 ∙10H 2 O
Цинковая обманка - ZnS
Сера в природе
Гипс – CaSO 4 ∙2H 2 O
Киноварь - HgS
Свинцовый блеск - PbS
Железный колчедан – FeS 2
Медный колчедан – Cu 2 S
11/15/16
Губарева В.А.

Положение серы в ПСХЭ.
Строение атома.
Вспомни!
11/15/16
Губарева В.А.

Общая характеристика серы
Вставьте пропущенные слова:
- Сера - элемент VI группы, главной подгруппы.
- Заряд ядра атома cеры равен +16 .
- В ядре атома серы 16 протонов.
- В ядре атома серы 16 нейтронов.
- В атоме серы 16 электронов.
- Атом серы имеет 3 энергетических уровня.
- Электронная оболочка имеет строение 2е, 8е, 6е .
- На внешнем уровне в атоме 6 электронов.
- Высшая степень окисления атома серы равна +6 .
- Простое вещество сера является неметаллом .
- Высший оксид и гидроксид серы имеют
кислотный характер.
11/15/16
Губарева В.А.

Строение атома серы
S
p + = 16
Электронное строение
32
0
n 0 = 16
+16
Валентные возможности
e - = 16
8
2
6
3d 2
3d 1
3d 0
3p 4
3p 3
3p 4
3s 1
3s 2
3s 2
2p 6
2p 6
2s 2
2s 2
1s 2
1s 2
IV,
VI
II,
Валентные возможности -
Краткая электронная формула
11/15/16
Губарева В.А.
8

Сера – простое вещество
8
Аллотропные модификации
Ромбическая
Моноклинная
Пластическая
Аллотро́пия— существование одного и того же химического элемента в виде двух и более простых веществ, различных по строению и свойствам: так называемых аллотропических модификаций или аллотропических форм.
?
11/15/16
Губарева В.А.
8

2,05Å
Ромбическая сера
- S 8
- Твердая хрупкая
- Цвет лимонно – желтый
- Без вкуса и запаха
- t пл. = 112,8 0 С
- t кип. = 444 0 С
- Плотность - 2,07 г/см
- В воде не растворяется, не смачивается
- Растворяется в сероуглероде
108 0 C
Губарева В.А.
11/15/16
10
 96 0 С, при обычных условиях превращается в ромбическую. Выше 96 0 С Вставить Flash : Единая коллекция ЦОР - http://files.school-collection.edu.ru/dlrstore/bed068ab-8cff-11db-b606-0800200c9a66/ch09_22_06.swf Ниже 96 0 С Губарева В.А. 11/15/16 11 " width="640"
96 0 С, при обычных условиях превращается в ромбическую. Выше 96 0 С Вставить Flash : Единая коллекция ЦОР - http://files.school-collection.edu.ru/dlrstore/bed068ab-8cff-11db-b606-0800200c9a66/ch09_22_06.swf Ниже 96 0 С Губарева В.А. 11/15/16 11 " width="640"
Моноклинная сера
- Желтые иглы - S 8
- Без вкуса и запаха
- t пл. = 119 0 С
- t кип. = 444 0 С
- Плотность - 1,96 г/см
- Устойчивая при t 96 0 С, при обычных условиях превращается в ромбическую.
Выше 96 0 С
Вставить Flash : Единая коллекция ЦОР - http://files.school-collection.edu.ru/dlrstore/bed068ab-8cff-11db-b606-0800200c9a66/ch09_22_06.swf
Ниже 96 0 С
Губарева В.А.
11/15/16
11

S
S
S
S
S
S
S
Пластическая сера
резину коричневая масса,
растягивающаяся в нити;
- Плотность - 2,046 г/см
- Не растворяется в
сероуглероде
хрупкой, желтеет,
превращается в
ромбическую
Губарева В.А.
11/15/16
12

2,05Å
Аллотропия серы
12
Получение пластической серы
108 0 C
t
S
S
S
S
S
S
S
Видео плеер химических экспериментов
11/15/16
Губарева В.А.
13

Природные соединения серы
13
Фотография
Описание минерала
Химический состав
S
Цвет
Серно-желтый, желто-оранжевый, желто-бурый.
Плотность
Твердость
2 – 2,1 г/см 3
2
Сера
самородная
Источник информации
W
Губарева В.А.
11/15/16

Природные соединения серы
Фотография
Описание минерала
Химический состав
FeS 2
Цвет
Латунно-желтый
Плотность
4,95 - 5,1 г/см 3
Твердость
6 -6,5
Пирит
Источник информации
W
Губарева В.А.
11/15/16

Природные соединения серы
Фотография
Описание минерала
Химический состав
HgS
Цвет
Красный, коричневый, серый
Плотность
8,0 – 8,2 г/см 3
Твердость
2 – 2,5
Киноварь
Источник информации
W
Губарева В.А.
11/15/16

Природные соединения серы
Фотография
Описание минерала
Химический состав
ZnS
Цвет
Серовато-бурый, коричневый, реже желтый, красный
Плотность
3,9 – 4,2 г/см 3
Твердость
3,5 – 4
Сфалерит (цинковая обманка)
Источник информации
W
Губарева В.А.
11/15/16

Природные соединения серы
Фотография
Описание минерала
Химический состав
PbS
Цвет
Свинцово - серый
Плотность
7,2 – 7,6 г/см 3
Твердость
2,5
Галенит (свинцовый блеск)
Источник информации
W
Губарева В.А.
11/15/16

Природные соединения серы
Фотография
Описание минерала
Химический состав
Na 2 SO 4 * 10 H 2 O
Цвет
Бесцветный, белый
Плотность
Твердость
1.49 г/см 3
1.5
Мирабилит (глауберова соль)
Источник информации
W
11/15/16
Губарева В.А.

Природные соединения серы
Фотография
Описание минерала
Химический состав
Cu 2 S
Цвет
Плотность
Синевато-черный, серый, черный, стальной черный
5,5 – 5,8 г/см 3
Твердость
2 - 3
Халькозин (медный колчедан)
Источник информации
W
11/15/16
Губарева В.А.

Природные соединения серы
Фотография
Описание минерала
Химический состав
CaSO 4 ∙ 2H 2 O
Цвет
Белый, серый, красный
Плотность
2,31 – 2,33г/см 3
Твердость
1,5 - 2
Гипс
Источник информации
W
11/15/16
Губарева В.А.

11/15/16
Химические свойства серы
Взаимодействие с водородом
Взаимодействие с металлами
Химические свойства серы
Взаимодействие c окислителями
Взаимодействие с кислородом
Взаимодействие с галогенами
Сера – типичный химически активный неметалл, вступающий в реакции со многими металлами, неметаллами и сложными веществами, но она менее активна по сравнению с кислородом и галогенами. Все эти реакции относятся к окислительно-восстановительным, в которых свободная сера выступает в роли как окислителя, так и восстановителя, проявляя при этом степени окисления S -2 ← S 0 → S +4 → S +6
Общий вывод
11/15/16
Губарева В.А.
сера
22

Химические свойства серы
23
Взаимодействие с металлами
?
2 Na 0 + S 0 = Na +1 2 S -2
При взаимодействии с металлами сера проявляет окислительные свойства. Реакции протекают при нагревании и приводят к образованию сульфидов. Исключение – благородные металлы: золото, платина и иридий, которые с серой не реагируют.
Na + S =
Al + S =
2Al 0 + 3S 0 = Al +3 2 S -2 3
Fe 0 + S 0 = Fe +2 S -2
Fe + S =
Опыт «Взаимодействие натрия с серой»: http://files.school-collection.edu.ru/dlrstore/3e6b77cf-8fff-882a-d3c3-c50221c6eba9/index.htm
Выводы
Видео плеер химических экспериментов
.
11/15/16
Губарева В.А.
23

Химические свойства серы
23
Взаимодействие с водородом
?
Н 2
S + H 2 = H 2 S ↑
При пропускании водорода через расплав серы появляется характерный запах тухлых яиц, т.к. образуется газообразный сероводород. В этой реакции сера также проявляет окислительные свойства
S
Н 2 О
.
11/15/16
Губарева В.А.
24

Химические свойства серы
25
Взаимодействие с кислородом
?
S + О 2 = SO 2
При нагревании сера вступает в реакцию с кислородом с образованием оксида серы(IV) SO 2 (сернистого газа). В этой реакции сера выступает в роли восстновителя.
Видео плеер химических экспериментов
.
11/15/16
Губарева В.А.
25

Химические свойства серы
25
Взаимодействие с галогенами
?
S 0 + 2Cl 0 2 = S +4 Cl -1 4
S x Cl y
С галогенами (кроме йода) сера проявляет восстановительные свойства, образуя соединения разного состава: SF 6 , SF 4 , SF 2 , SCl 4 , S 2 Cl 2 , S 2 Br 2 . большинство этих соединений легко разлагается водой(гидролиз)
.
11/15/16
Губарева В.А.
26
Химические свойства серы
26
?
Взаимодействие с окислителями
При нагревании сера взаимодействует с сильными окислителями – кислотами и солями, например, с концентрированной серной кислотой, с нитратом калия, хлоратом калия. В этих реакция сера является восстановителем.
S 0 +2H 2 SO 4 = 3S +4 O 2 +2H 2 O
S + H 2 SO 4 =
(Конц.)
3S + KClO 3 = 2KCl + 3SO 2
S + KClO 3 =
Видео плеер химических экспериментов
Выводы
.
11/15/16
Губарева В.А.
27

Расставить коэффициенты методом электронного баланса
27
0 +5 -1 +4
S + KClO 3 → KCl + SO 2 ↑
Электронный баланс
Порядок действий
Окисление
S 0
S 0
- 4ē → S +4
3
3
3
нок
12
3. Составить полуреакции окисления и восстановления
4. Расставить коэффициенты
2. Подчеркнуть элементы, изменившие степень окисления
1. Расставить степени окисления химических элементов
Восстановление
Cl +5
Cl +5
+ 6ē → Cl -1
2
2
2
2
- восстановитель
- окислитель
11/15/16
Губарева В.А.
28

11/15/16
Получение серы
28
В промышленных условиях серу получают без подъема руды на поверхность:
- путем выплавления из руды водяным паром
- восстановлением сернистого газа:
2 H 2 S + O 2 = 2 S + 2H 2 O
SO 2 + C = S + CO 2
SO 2 + 2 CО = S + 2 CO 2
11/15/16
Губарева В.А.
сера
28
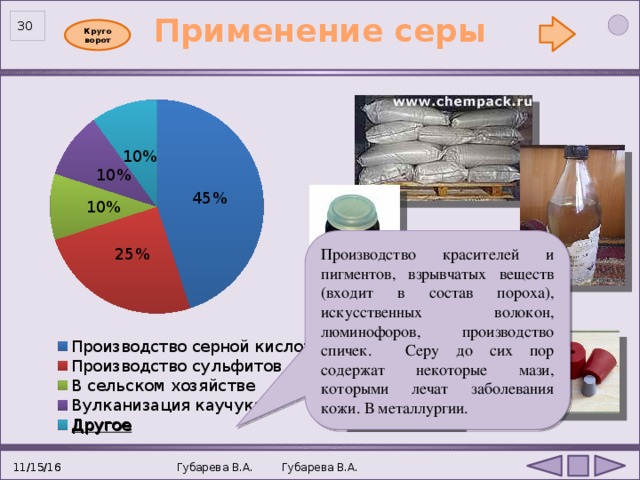
Применение серы
28
Круго
ворот
Производство красителей и пигментов, взрывчатых веществ (входит в состав пороха), искусственных волокон, люминофоров, производство спичек. Серу до сих пор содержат некоторые мази, которыми лечат заболевания кожи. В металлургии.
Другое
11/15/16
Губарева В.А.
11/15/16
Губарева В.А.
28

Проверь свои знания!
31
Выбери правильный ответ
Процесс демеркуризации – это взаимодействие серы с
Восстановительные свойства сера
проявляет в реакции
Количество энергетических уровней
у атома серы.
Сера не будет реагировать с
Для серы не характерны степени
окисления
Вопрос 1
ртутью
алюминием
с водородом
с кислородом
три
два
4 +
2 +
водородом
азотом
А
Б
Б
А
А
Б
А
Б
Б
А
Вопрос 2
Вопрос 3
железом
медью
с ртутью
с натрием
четыре
один
6 +
1 +
хлором
кислородом
В
Г
Г
В
В
Г
Г
Г
В
В
Вопрос 4
Вопрос 5
11/15/16
Губарева В.А.
31

Проверь свои знания!
32
Выберите уравнения реакций, в которых сера
является окислителем
S + Zn = ZnS
S + O 2 =SO 2
Молодец
Ошибка
S + Fe = FeS
S + Cu = CuS
Молодец
Молодец
S + Hg = HgS
3S + 2Al= Al 2 S 3
Ошибка
Молодец
S + 3F 2 = SF 6
3S+2KClO 3 =2KCl+SO 2
Молодец
Ошибка
S + 2Na =Na 2 S
S + H 2 = H 2 S
Молодец
Молодец
S + 2Cl 2 =SCl 4
2H 2 S +3O 2 =2H 2 O+2SO 2
Ошибка
Ошибка
Губарева В.А.
11/15/16
32

Проверь свои знания!
32
11/15/16
Губарева В.А.
32

Используемые источники
32
http://www.alhimikov.net/element/S.html
Академик. http://dic.academic.ru/dic.nsf/simvol/776
Популярная библиотека. http://n-t.ru/ri/ps/pb016.htm
http://www.chemnet.ru/rus/history/element/S.html
Викитека. http://ru.wikisource.org/wiki/ЭСБЕ/Сера,_в_технике
http://www.edimka.ru/text/sostav-produktov/sera
http://www.catalogmineralov.ru
http://ru.wikipedia.org/wiki
http://school-collection.edu.ru/
http://www.school316.spb.ru/chemistry/sera/index.html
11/15/16
Губарева В.А.
34

















 96 0 С, при обычных условиях превращается в ромбическую. Выше 96 0 С Вставить Flash : Единая коллекция ЦОР - http://files.school-collection.edu.ru/dlrstore/bed068ab-8cff-11db-b606-0800200c9a66/ch09_22_06.swf Ниже 96 0 С Губарева В.А. 11/15/16 11 " width="640"
96 0 С, при обычных условиях превращается в ромбическую. Выше 96 0 С Вставить Flash : Единая коллекция ЦОР - http://files.school-collection.edu.ru/dlrstore/bed068ab-8cff-11db-b606-0800200c9a66/ch09_22_06.swf Ниже 96 0 С Губарева В.А. 11/15/16 11 " width="640"










































