
Общая характеристика элементов VIA- группы (халькогены). https://yandex.ru/video/preview/1474554779763048083

Элементы VI группы главной подгруппы.
- O Халькогены , т.е
- S « рождающие руды».
- Se
- Te
- Po

Se и Te - минералов не образуют Ро - очень редкий радиоактивный элемент
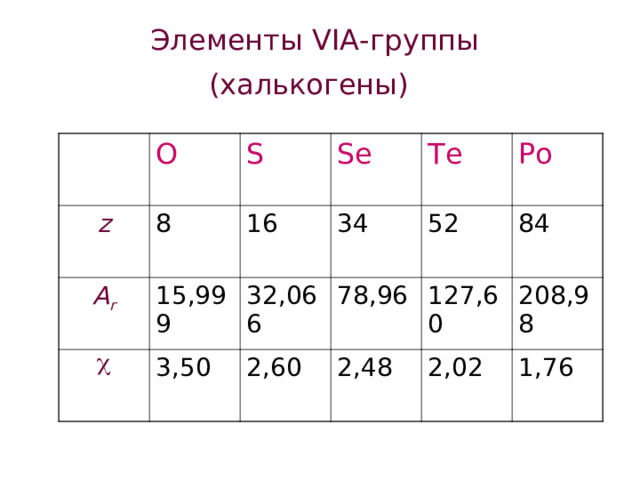
Элементы VI А-группы (халькогены)
z
O
8
A r
S
Se
16
15,999
34
3,50
32,066
Te
2,60
Po
78,96
52
84
2,48
127,60
208,98
2,02
1,76

Кислород

Кислород
- Кислород – самый распространенный элемент на Земле (49,5% масс.).
- Кислород существует в самородном виде (воздух) и входит в состав воды, горных пород и живых организмов.
- В атмосфере содержание кислорода – 23,13% масс. .

Аллотропные модификации кислорода.
???
???
Страница 1
Страница 1
Молекула кислорода
Газ без запаха, немного тяжелее воздуха. Плохо растворим в воде.
Молекула озона
Газ с резким запахом свежести, тяжелее воздуха. Растворим в воде лучше, чем кислород.
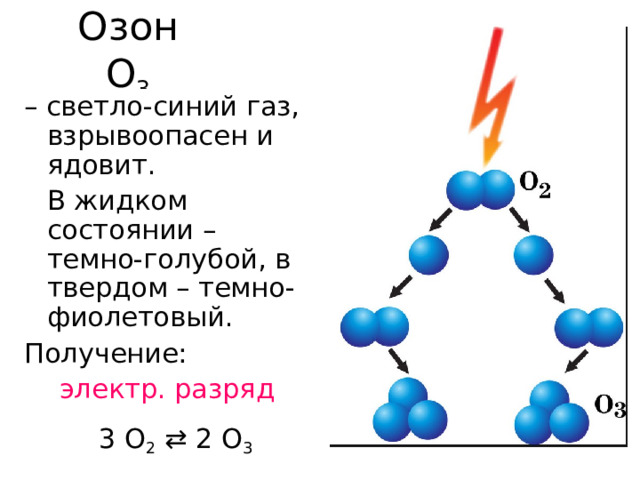
Озон O 3
– светло-синий газ, взрывоопасен и ядовит.
В жидком состоянии – темно-голубой, в твердом – темно-фиолетовый.
Получение:
электр. разряд
3 O 2 2 O 3
Химические свойства кислорода:
не взаимодействует с галогенами, благородными газами, золотом и платиновыми металлами.
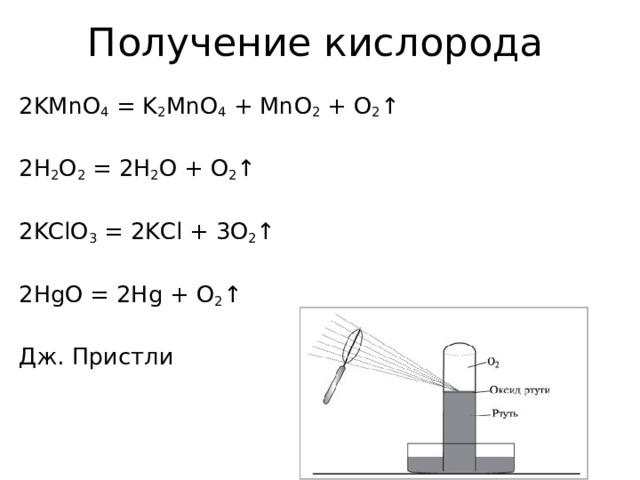
Получение кислорода
2 KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 ↑
2 H 2 O 2 = 2 H 2 O + O 2 ↑
2 KClO 3 = 2 KCl + 3 O 2 ↑
2HgO = 2Hg + O 2 ↑
Дж. Пристли

- Кислород активно взаимодействует со щелочными металлами даже без нагревания. Металлы средней и низкой активности реагируют с кислородом при нагревании.
4 Li + O 2 = 2 Li 2 O
3 Fe + 2 O 2 = Fe 3 O 4
2Mg + O 2 = 2MgO

Реакция горения
- При взаимодействии металлов и неметаллов с кислородом зачастую происходит выделение большого количества тепла и даже воспламенение.
S + O 2 = SO 2
4 P + 5 O 2 = 2 P 2 O 5

Взаимодействие кислорода с азотом происходит только при нагревании свыше 2000 °C или же при электрическом разряде.
N 2 + O 2 = 2NO - Q

Кислород довольно активно взаимодействует не только с простыми, но и со сложными веществами.
CH 4 + 2O 2 = 2H 2 O + CO 2
2NO + O 2 = 2NO 2
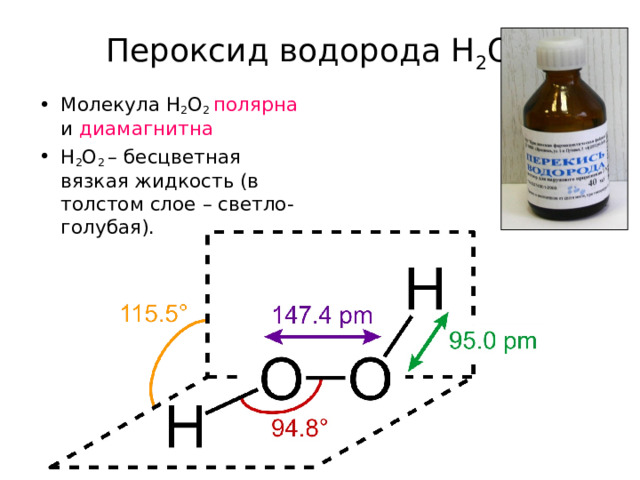
Пероксид водорода H 2 O 2
- Молекула H 2 O 2 полярна и диамагнитна
- H 2 O 2 – бесцветная вязкая жидкость (в толстом слое – светло-голубая) .

Пероксид водорода H 2 O 2
- В разбавленных растворах пероксид водорода неустойчив и самопроизвольно диспропорционирует:
2H 2 O 2 – I = 2H 2 O – II + O 2 0

Сера

Сера- химический элемент
- Сера - химический элемент ΙΙΙ ( малого) периода,3 ряда, V Ι(А) группы
- Атомный номер 16
- Заряд ядра
+16

Шкала степеней окисления серы
+VI
SO 3 , H 2 SO 4 , K 2 SO 4 , SF 6
SO 2 , Na 2 SO 3 , SF 4 , SCl 4
+IV
0
S (S 8 , S x , S 6 , S 4 , S 2 , S 0 )
I
Na 2 S 2 , FeS 2
II
H 2 S, Na 2 S, CS 2



— твердое агрегатное
состояние
— желтого цвета
— не растворима в воде
— не смачивается водой
— растворяется в
органических
растворителях
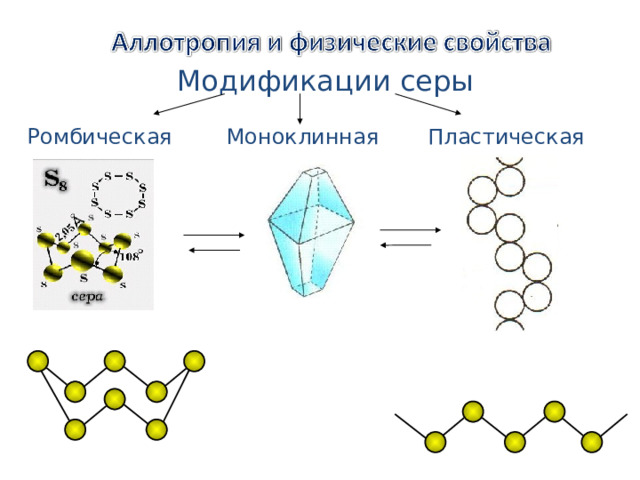
Модификации серы
Пластическая
Моноклинная
Ромбическая

В природе сера встречается как в виде самородной серы, так и в
составе минералов и горных пород, таких как сульфиды и сульфаты.
26

Обычная ромбическая сера состоит из циклических молекул S 8 . Кристаллы ромбической серы представляют собой октаэдры со срезанными углами. Ромбическая сера имеет полупрозрачную лимонно-жёлтую окраску, температура плавления — 112,8 ˚ С.

Пластическая сера
Резиноподобное вещество коричневого цвета.

Получение.
1. Выплавление из горных пород
FeS 2 → FeS + S ( без доступа воздуха )
2. В лаборатории
Неполное окисление сероводорода (при недостатке кислорода).
- H 2 S + O 2 → S + Н 2 О
- H 2 SO 3 + H 2 S → S + H 2 O

Химические свойства серы
https://yandex.ru/video/preview/6873508708064473057
Взаимодействует со многими металлами, кроме золота и платины:
Mg + S = MgS
2Al + 3S = Al 2 S 3
Взаимодействует со всеми щелочными, щёлочноземельными металлами, а также медью, ртутью и серебром при обычных условиях:
Cu + S = CuS
Hg + S = HgS
26

Химические свойства серы
С остальными металлами сера реагирует при нагревании:
Zn + S = ZnS
Окислительные свойства сера проявляет при взаимодействии с некоторыми неметаллами:
H 2 + S = H 2 S
26

Химические свойства серы
Из неметаллов с серой не реагируют только азот, йод и благородные газы . При взаимодействии с кислородом сера проявляет восстановительные свойства:
S + O 2 = SO 2
26
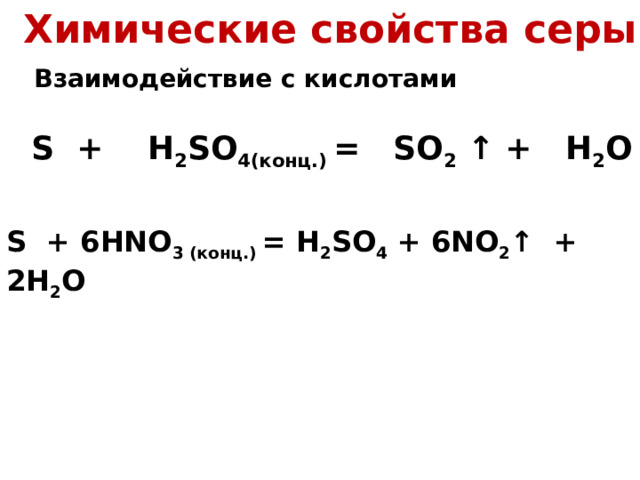
Химические свойства серы
Взаимодействие с кислотами
S + H 2 SO 4 (конц.) = SO 2 ↑ + H 2 O
S + 6HNO 3 ( конц. ) = H 2 SO 4 + 6NO 2 ↑ + 2H 2 O

Химические свойства серы
Взаимодействие со щелочами
S + KOH = K 2 S + K 2 SO 3 + H 2 O

СЕРА в организме человека
- Сера входит в состав белков(волосы)
- Сера- составная часть активных веществ:
витаминов и гормонов
- При недостатке серы в организме наблюдаются хрупкость и ломкость костей, выпадение волос.

Применение серы
Характеристика и свойства
H 2 S – сероводород
- Бесцветный газ с неприятным запахом
- Ядовит
- Растворим в воде
- Слабая кислота(двухосновная)
- Диссоциирует в две ступени


Получение.
- H 2 + S → H 2 S
- Вытеснение сероводорода из сульфидов сильными кислотами
HCl + FeS → H 2 S + FeCl 2

Диссоциация.
Диссоциация происходит в 2 ступени:
- H 2 S → H + + HS -
- HS - → 2H + + S 2 -

Химические свойства
!! Только восстановитель
2H2S + O2(недост) → 2S + 2H2O
2H2S + 3O2(изб) → 2S О 2 + 2H2O
H2S + Ca → CaS + H2
H2S + CaO→ CaS + H2O
H2S + 2NaOH→ Na2S + 2H2O
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
H2S + Br2 → S + 2HBr
Качественная реакция на сероводородную кислоту:
H2S + Pb(NO3)2 → PbS↓ + 2HNO3
( черный )

SO 2 – сернистый газ
Характеристика и свойства
- Бесцветный газ с резким запахом
- Ядовит
- Тяжелее воздуха
- Хорошо растворим в воде

Получение.
1. В промышленности: обжиг сульфидов
4 FeS 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2
2. В лаборатории:
Горение серы
S + O 2 → SO 2 ↑
Действие кислот на соли сернистой кислоты
Na 2 SO 3 + 2HCl → 2NaCl + SO 2 ↑ + H 2 O
При окислении тяжелых металлов концентрированной серной кислоты
Cu + 2H 2 SO 4 (к) → CuSO 4 + SO 2 + 2H 2 O
t o
t o
t o
t o

Химические свойства
SO 2 + H 2 O ↔ H 2 SO 3
2NaOH + SO 2 → Na 2 SO 3 + H 2 O (NaHSO3)
SO 2 – восстановитель:
2 SO 2 + O 2 → 2 SO 3
SO 2 + Br 2 + 2H 2 O → H 2 SO 4 + 2HBr
SO 2 – окислитель:
SO 2 + С → S + С O 2
SO 2 + 2H 2 S → 3S + 2H 2 O
t o
кат.

Характеристика и свойства
SO 3 – серный ангидрид
- Бесцветная жидкость
- При температуре
- Гигроскопичен

Получение.
2SO2 + O2 → 2SO3
Fe2(SO4)3 → Fe2O3 + 3SO3
t o , кат
t o

Химические свойства
SO3 + H2O → H2SO4

Серная кислота в природе https://yandex.ru/video/preview/10669047143570912439
Европа – спутник Юпитера
Кипящее озеро (Курильские острова)
Кислотное озеро на глубине вулкана Малый Семячик
Облака планеты Венера

Физические свойства
H 2 SO 4 - бесцветная маслянистая тяжелая жидкость, без запаха, нелетучая при н.у. Обладает сильным водоотнимающим свойством. Хорошо растворяется в воде.
Техника безопасности:
Кислоту приливают в воду осторожно, тоненькой струйкой.

Разбавление серной кислоты
https://www.youtube.com/watch?v=55AzmbliyyI
Химические свойства

Химические свойства разбавленной H 2 SO 4
1 . Взаимодействие с металлами
(Стоящими до Н в ЭРНМ)
Zn + H 2 SO 4 = ZnSO 4 + H 2 ↑
Cu + H 2 SO 4 ≠

Химические свойства разбавленной H 2 SO 4
2 . Взаимодействие с основными и амфотерными оксидами
H 2 SO 4 + CuO = CuSO 4 + H 2 O

Химические свойства разбавленной H 2 SO 4
3 . Взаимодействие с основаниями:
а) щелочами
H 2 SO 4 + 2NaOH = Na 2 SO 4 + 2H 2 O
б) нерастворимыми основаниями
H 2 SO 4 + Cu(OH) 2 = CuSO 4 + 2H 2 O

Химические свойства разбавленной H 2 SO 4
4 . Взаимодействие с солями
H 2 SO 4 + BaCl 2 = BaSO 4 ↓+ 2HCl
Качественная реакция – выпадение белого осадка
белый

Химические свойства концентрированной H 2 SO 4
Концентрированная H 2 SO 4 - сильный окислитель за счет S(+6)
1. Взаимодействие с металлами
+ активные металлы
H 2 S , S , SO 2
+ малоактивные металлы
SO 2
+ Fe, Al
Пассивация металла
Cu + 2H 2 SO 4 ( конц ) = CuSO 4 + SO 2 ↑ + 2H 2 O
окисление
Cu 0 – 2e -
Cu +2
восстановитель
восстановление
S +6 + 2e -
S +4
окислитель

СВОЙСТВА СЕРНОЙ КИСЛОТЫ
- https://yandex.ru/video/preview/13433926494551916525

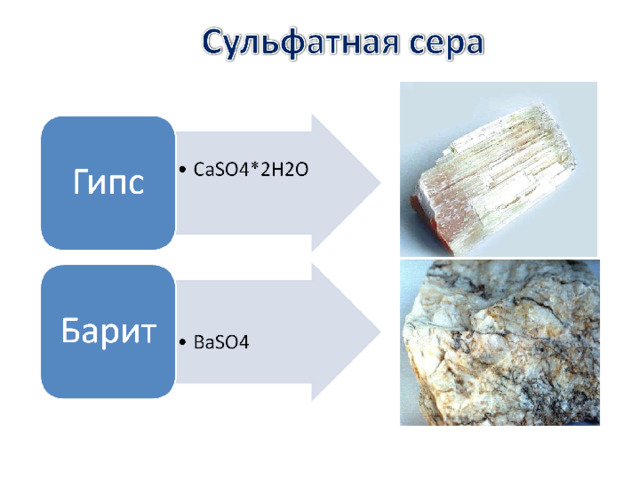
Соли серной кислоты
Na 2 SO 4 × 10H 2 O
Глауберова соль
CaSO 4 ×2H 2 O
Гипс
BaSO 4
Сульфат бария
CuSO 4 ×5H 2 O
Медный купорос

Качественная реакция на сульфит и сульфат- ионы
- https://yandex.ru/video/preview/7047296868101507721

Задание.
Определите степени окисления серы в соединениях :
SO 2 , H 2 S, SO 3 , CaS, Na 2 SO 4 , NaHS,
KHSO 4 , MgSO 4 , H 2 SO 4 , K 2 SO 3 .

Тест
1. Концентрированная серная кислота при комнатной температуре не действует на каждое из двух веществ:
А) Mg, Cu; Б) Na, Zn; В) Ca, Li; Г) Fe, Al.
2. Разбавленная серная кислота реагирует с каждым из веществ:
А) Cu и KO H; Б) Na 2 CO 3 и Al(OH) 3
В) AlCl 3 и Ag; Г) FeSO 4 и H 2 SO 4
3. При разбавлении серной кислоты всегда приливают кислоту к воде. Чем опасно разбавление концентрированной серной кислоты приливанием к ней воды?:
А) Может возникнуть пожар;
Б) Может произойти разложение воды;
В) Может выделиться ядовитое вещество;
Г) Может произойти разбрызгивание раствора вследствие выделения теплоты.
4. Водный раствор серной кислоты реагирует с каждым из веществ:
А) С цинком и оксидом натрия;
Б) С железом и оксидом углерода (II);
В) С алюминием и хлоридом натрия;
Г) С медью и гидроксидом калия.

Тест (ответы)
1 – Г
2 – Б
3 – Г
4 – А

1.Распределение электронов по энергетическим уровням в атоме серы:
А. 2, 6. В. 2, 8, 6.
Б. 2, 8. Г. 2, 8, 8.
2.Ряд формул веществ, в котором степень окисления серы уменьшается:
А . SO 3 -FeS-SO 2 . В . SO 2 -S-H 2 S.
Б . MgS-S-SO 2 . Г. S - H 2 S - Al 2 S 3 .

3.Свойство, характерное для серы:
А.Хорошо растворима в воде.
Б.Имеет металлический блеск.
В.Твердое вещество желтого цвета.
Г.Проводит электрический ток.
4. Уравнение реакции, в котором элемент сера является восстановителем:
А . Fe+H 2 SO 4 =FeSO 4 +H 2 .
Б . S+O 2 =SO 2 .
В. 2Li+S=Li 2 S.
Г. SO 3 +H 2 O=H 2 SO 4


СПАСИБО ЗА ВНИМАНИЕ!



























































































