Алгоритм составления ОВР
1.Определить степени окисления элементов в соединениях, участвующих в реакции.
2.Выявить элемент, степень окисления которого понизилась, повысилась, окислитель и восстановитель.
3.Выявить число отданных и принятых электронов.
Просмотр содержимого презентации
«ОВР»

Реакции
Взаимодействие красного
фосфора с кислородом
Взаимодействие оксида фосфора ( V )
с водой
0
+5
+5 -2
+1 -2
+1 -2
+5 -2
0
2
2
3
4
5
P 2 O 5 + H 2 O → H 3 PO 4
P + O 2 → P 2 O 5

Окислительно – восстановительные реакции
… – реакции, протекающие с изменением степени окисления элементов.

Два антипода парою ходят, Первый – теряет; второй - находит, Ролью меняясь при этом порой… Кто ж из них первый и кто же второй?
- восстановитель
- окислитель
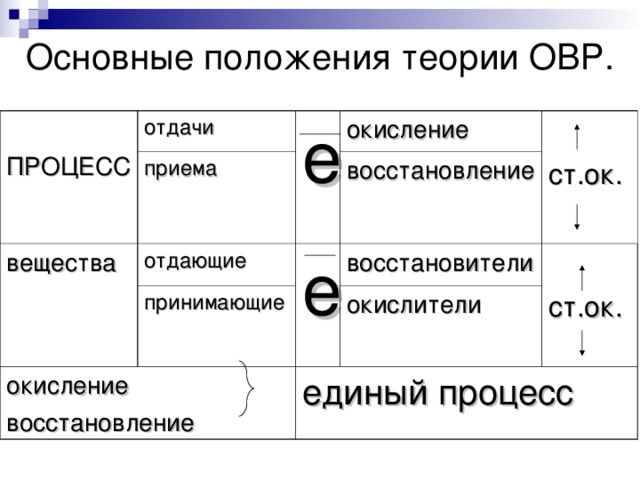
Основные положения теории ОВР.
ПРОЦЕСС
отдачи
приема
е
вещества
отдающие
окисление
восстановление
ст.ок.
окисление
восстановление
принимающие
е
восстановители
единый процесс
окислители
ст.ок.
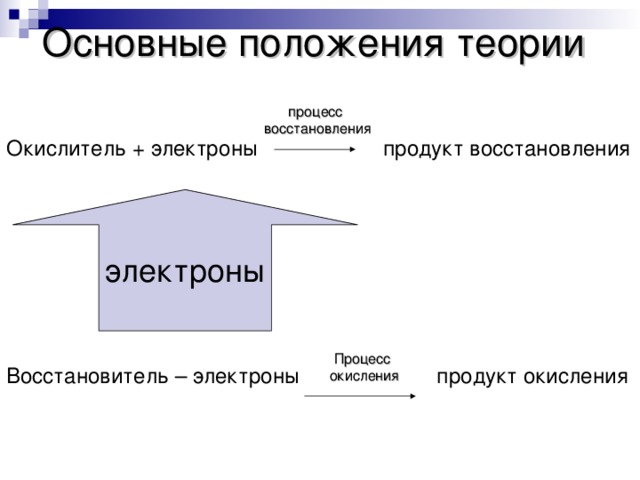
Основные положения теории
Окислитель + электроны продукт восстановления
Восстановитель – электроны продукт окисления
процесс
восстановления
электроны
Процесс
окисления
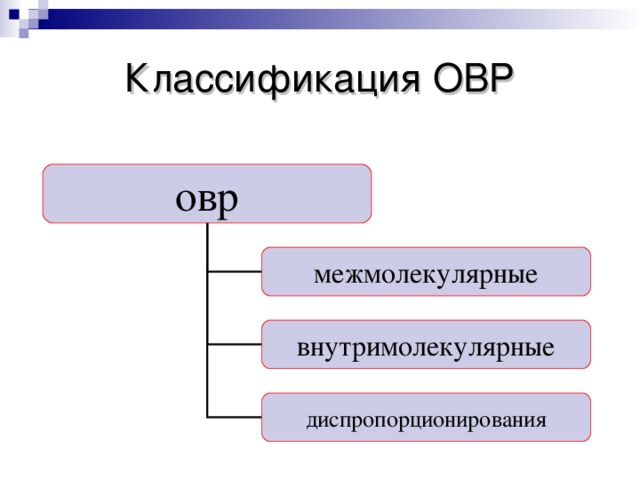
Классификация ОВР
овр
межмолекулярные
внутримолекулярные
диспропорционирования

Алгоритм составления ОВР
- Определить степени окисления элементов в соединениях, участвующих в реакции.
- Выявить элемент, степень окисления которого понизилась, повысилась, окислитель и восстановитель.
- Выявить число отданных и принятых электронов.

Число отданных и принятых электронов должно быть одинаковым.
Если это не так, то составить электронный баланс:
- Найти НОК числа отданных и принятых электронов;
- Делением НОК на число отданных и принятых получить коэффициент перед восстановлением;
- Делением НОК на число принятых электронов получить коэффициент перед окислением;
- Умножить полуреакции окисления и восстановления на соответствующие коэффициенты.
- Перенести коэффициенты в общее уравнение.

Алгоритм определения степеней окисления

Восстановитель
Калий
Галлий

Восстановитель
- nē
Э Э n+
- Атомы металлов ( I и II гр . , Al, Fe, Zn… ).
- Отрицательно заряженные ионы неметаллов ( S 2– , Cl – , Br – … до свободных элементов).
- Ионы металлов в низких степенях окисления ( Mn 2+ Mn 1+ ) .
- Ионы и молекулы, содержащие атомы в промежуточных степенях окисления (бисульфит).
- 1 ē

Окислитель
Фтор
Азот

Окислитель
+ nē
Э Э n -
- Атомы элементов VI–VII групп (О 2 , С l 2 … ).
- Ионы металлов в высоких степенях окисления ( Cu 2- Cu + )
- Ионы молекул содержат атомы неметаллов в высоких степенях окисления (КМ n О 4 – Mn 7+ ).
- Ионы и молекулы, содержащие атомы неметаллов в высоких степенях окисления.
+ 1 ē

Степень окисления – Условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все соединения только ионные.
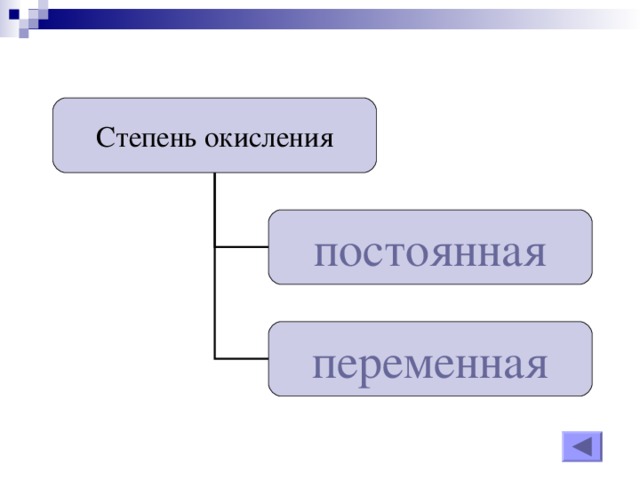
Степень окисления
постоянная
переменная

Сера ( -2,0,+2,+4,+6)
Железо ( +2, +3)

Высшая степень окисления
- Характерна для Ме и нМе
- Определяем по номеру группы ?
элемент
Na
№ группы
I
P
высшая ст.ок
S
+ 1
V
Al
+5
?
SI
?
?
?
?
Br
?
?
?
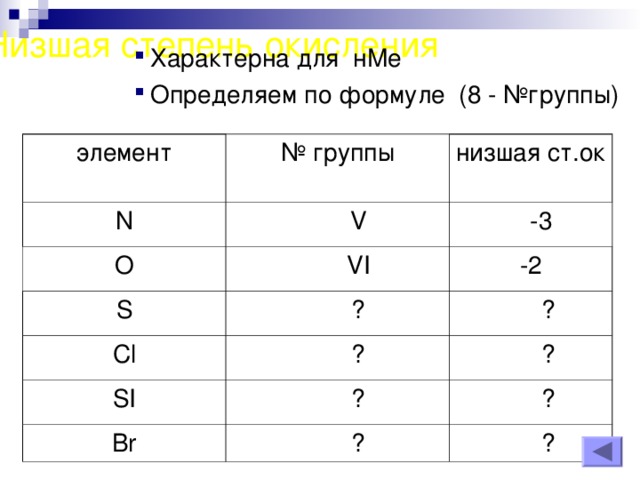
Низшая степень окисления
- Характерна для нМе Определяем по формуле (8 - №группы)
- Характерна для нМе Определяем по формуле (8 - №группы)
- Характерна для нМе Определяем по формуле (8 - №группы)
- Характерна для нМе Определяем по формуле (8 - №группы)
- Характерна для нМе
- Определяем по формуле (8 - №группы)
элемент
№ группы
N
низшая ст.ок
V
O
VI
S
-3
-2
?
Cl
?
?
SI
?
?
Br
?
?
?

Нулевая ( 0) Все простые вещества
Йод
Бром
Литий

постоянная
Степень окисления
Элементы
-1
F
+1
Li, Na, K, Rb, Cs
+2
Be, Mg, Ca, Ba, Ra
+3
Al

Тест для 8 класса
Тема: «Окислительно – восстановительные реакции»

Инструкция по выполнению теста
- Внимательно прочитайте задание и выберите правильный ответ – нажмите справа на нужную кнопку
- Время тестирования ограничено: 10 минут

Степень окисления серы K 2 SO 3 в равна
Окислительно - восстановительная реакция
- CaO+Co 2 =CaCO 3
- NaOH+HCl=NaHCl+H 2 O
- Fe+CuSO 4 =FeSO 4 +Cu
- Na 3 SiO 3 +2HCl=2NaCl+H 2 SiO 3

Окислитель
- Принимает электроны
- Окисляется
- Отдаёт электроны
- Не изменяет степень окисления

Магний имеет минимальное значение степени окисления

Фтор имеет максимальное значение степени окисления

Конец тестирования
- Молодец!
- Справились верно с 5 заданиями
- Отличная работа!

Вы ответили неправильно!
- Прочитайте параграф 43 ещё раз.
- Выполните тестовое задание снова.
Вернуться на тестовое задание
Закончить тестирование!

Степень окисления
Высшая
Нулевая ( 0)
Низшая









































