11-1
Металл А является важным компонентом сульфидных полиметаллических руд. Для его отделения руду обжигают, затем действуют на нее избытком газа Б, при этом металлы находящиеся в составе руды восстанавливаются до элементного состояния, А соединяется с Б, образуя летучее соединение В, которое при высоких температурах разлагается с выделением чистого металла А. Известно, что химические связи в тетраэдрической молекуле В с центральным атомом А образуются по донорно-акцепторному механизму.
Для получения 85,35 г В требуется 44,8 л (н.у.) газа Б. Газ Б способен гореть, причем продукт горения Г при пропускании над раскаленным углем увеличивает объем вдвое, образуя газ Б.
Определите вещества А, Б, В и Г? Составьте уравнения описанных реакций.
11-2
В норме концентрация глюкозы в крови человека составляет 5-7 ммоль/л. При анализе крови объемом 0,100 мл (после отделения белков) добавляют избыток гексацианоферрата (III) калия, который в присутствии карбоната калия взаимодействует с глюкозой.
К раствору прибавляют избыток йодида калия, который взаимодействует с непрореагировавшим гексацианоферратом (III) калия. Образовавшийся йод удаляют действием тиосульфата натрия.
Запишите уравнения всех описанных реакций.
Грозит ли донору диабет, если при анализе было добавлено 2,00 мл раствора K3[Fe(CN)6] с концентрацией 5,00 · 10-3моль/л, а на последнюю реакцию израсходовано 1,28 мл раствора Na2S2O3 такой же концентрации?
11-3
В книге Н.Н. Зинина «Работы казанского периода» описано выделение и свойства органического соединения, которое плавится при 500С, кипит около 3000С, перегоняется без разложения, представляет собой шелковисто-белые кристаллы в виде нескольких игл:
«Нафталидам имеет своеобразный, сильный, неприятный запах и острый, горький, едкий вкус. Он почти нерастворим воде и легко растворяется в винном спирте и эфире. Нафталидам не дает щелочной реакции на лакмус, из всех солей вытесняется аммиаком. Он соединяется со всеми кислотами, образуя белые соли, большей частью легко кристаллизующиеся».
Его состав определяли по следующим данным:
Опыт 1.
«0,341 г перегнанного нафталидама при сожжении с окисью меди дали 0,203 г воды и 1,0483 углекислоты, что соответствует 6,61% водорода и 83,84% углерода
Опыт 2.
0,361 г нафталидама …при сожжении с хромовокислым свинцом дали 0,2312 г воды и 1,1105 углекислоты, что соответствует 6,4% водорода и 83,9% углерода.
Опыт 3.
0,543 г вещества, сожженные по методу Вилля и Варентрапа, дали 0,8380 платинохлористоводородного аммония, что соответствует 9,62% азота.
Из винного спирта солянокислый нафталидам выпадает в виде маленьких блестящих чешуек.
Опыт 4.
0,3339 г возогнанной (солянокислой) соли при сожжении с окисью меди дали 0,1687 воды и 0,8153 углекислоты, следовательно, в 100 г : 5,61% водорода и 66,59% углерода.
Опыт 5.
0,3608 г возогнанной соли при сожжении с чистой негашеной известью и окисью меди дали 0,2784 г хлористого серебра, следовательно соль содержит 19,03% хлора.
Результаты опытов представлены в таблице
| Опыт % | 1 | 2 | 3 | 4 | 5 |
| С | 83,84 | 83,9 | - | 66,59 | - |
| Н | 6,61 | 6,4 | - | 5,61 | - |
| N | - | - | 9,62 | - | - |
| Cl | - | - | - | - | 19,03 |
Что такое винный спирт?
По данным опытов 1-5 установите брутто-формулу «нафталидама».
Напишите уравнения реакций в 1,2 и 4 опытах. Для чего в опытах 1 и 2 используют оксид меди и хромат свинца?
11-4
Предложите оптимальные пути синтеза, используя любые реактивы.
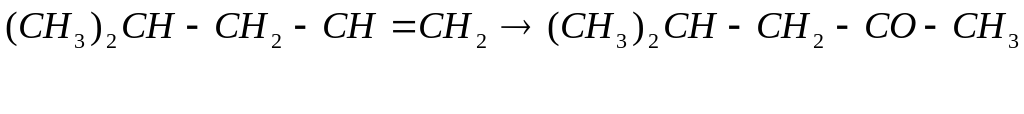
11-5
Напишите уравнение реакции, происходящей при попадании капли соляной кислоты на капроновый чулок (чулок «прожигается»).