
«Активизация познавательной деятельности на уроках химии при работе со схема-конспектами».
Логвиненко С.В .
Преподаватель химии и биологии 1 категории Приморского Промышленного техникума

Педагогическая технология: интенсивное обучение на основе схемных и знаковых моделей учебного материала»
(автор В.М.Шаталов)
ПЛАН
1 . Введение.
Виды малых графических пособий (МГП)
Опорный конспект.
- 2 . Аналитическая часть. Требования к опорному конспекту. Опорный сигнал, опорные конспекты.
Следящие и структурные опорные конспекты.
Требования к опорному конспекту.
Составление плана-конспекта
Примеры различных схема-конспектов

Один из методов оптимизации учебной деятельности, развития природных способностей обучающегося – создание малых графических пособий (МГП).
- МГП могут быть представлены разными символико-графическими формами: схемами, схематическими рисунками, таблицами, диаграммами, схемами-конспектами.
- Я остановлюсь на применении схема-конспектов.

Опорный сигнал (ОС) – это своеобразный план излагаемого материала, система взаимосвязанных ключевых слов, условных знаков, рисунков .
Сигнал может быть в форме ключевого слова, термина, цифры, рисунка, схемы, стрелки.
Например: Н2О, СО2,
- При составлении схем содержания важную роль отводим цветовому оформлению. Цветовое структурирование позволяет вычленить подсистемы информации в комплекте схем.

Опорные конспекты
Опорный конспект
Схемы-конспекты

Три этапа :
- I этап – обучающие читают параграф, выделяются фрагменты текста, содержащие относительно законченную мысль.
- II этап – составление следящего конспекта. Предлагаем обучающимся выбрать в тексте опорное слово, сочетание слов, символ, указывающий на предмет мысли. Последовательность полученных записей и образует следящий конспект.
- III этап – состоит в преобразовании следящего конспекта в структурный. Учитель кратко разъясняет цель такого преобразования, показывает подготовленный заранее образец структурного конспекта и объясняет, в результате каких преобразований он был получен из следящего конспекта.
Образец такого конспекта обучающие заносят в тетрадь.

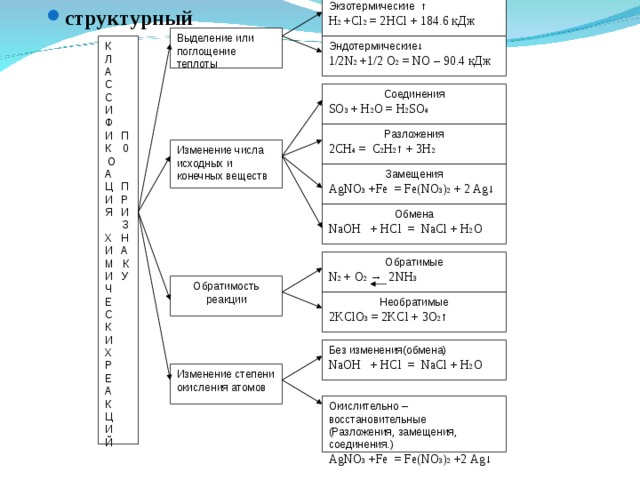
Следящий конспект . Классификация химических реакций.
- 1.Классификация реакций по изменению степени окисления.
- 2.Классификация по числу и составу исходных и образующих веществ.
А) реакции разложения 2СН4 = С2Н2↑ + 3Н2
Б) реакции соединения SO 3 + H 2 O = H 2 SO 4
B ) замещения: AgNO3 + Fe = Fe(NO3)2 + 2 Ag↓
Г) обмена: NaOH + HCl = NaCl + H 2 O
- 3) Классификация по тепловому эффекту .
А)Тепловой эффект –количество теплоты, которое выделяется или поглощается.
Б)Экзотермические – протекают с выделением теплоты.
H 2 + Cl 2 = 2 HCl + 184.6 кДж
В)Эндотермические – протекают с поглощением теплоты
1/2 N 2 +1/2 O 2 = NO – 90.4 кДж
Г)Термохимические уравнения.
- 4)Классификация по признаку обратимости.
А) необратимые – протекающие до конца
2 KClO 3 = 2 KCl + 3 O 2↑
Б) обратимые – протекающие во взаимно противоположных направлениях.
N 2 + O 2 → 2 NH 3 + Q
2 NH 3→ N 2 + O 2 - Q
Экзотермические ↑
H 2 + Cl 2 = 2 HCl + 184.6 кДж
Выделение или поглощение теплоты
Эндотермические↓
К
Л
А
С
С
И
Ф
И П
К 0 О
А
Ц П
И Р
Я И
З
Х Н
И А
М К
И У
Ч
Е
С
К
И
Х
Р
Е
А
К
Ц
И
Й
1/2 N 2 +1/2 O 2 = NO – 90.4 кДж
Соединения
SO 3 + H 2 O = H 2 SO 4
Разложения
2СН 4 = С 2 Н 2 ↑ + 3Н 2
Изменение числа исходных и конечных веществ
Замещения
AgNO 3 +Fe = Fe(NO 3 ) 2 + 2 Ag↓
Обмена
NaOH + HCl = NaCl + H 2 O
Обратимые
N 2 + O 2 → 2 NH 3
Обратимость реакции
Необратимые
2KClO 3 = 2KCl + 3O 2 ↑
Без изменения(обмена)
NaOH + HCl = NaCl + H 2 O
Изменение степени окисления атомов
Окислительно – восстановительные
(Разложения, замещения, соединения.)
AgNO 3 +Fe = Fe(NO 3 ) 2 +2 А g↓

Рекомендации по составлению опорного конспекта.
- 1. Вспомните материал, изученный на уроках по данной теме.
- 2. Изучите текст, выделите основные понятия и термины.
- 3. Составьте план конспекта.
- 4. Придумайте символику опорных схем.
- 5. Приступайте к графическому изображению опорных сигналов
- 6. Не злоупотребляйте фактическим материалом, иначе опорный конспект будет громоздким и трудным для запоминания.
- 7. Составляйте конспект сначала простым карандашом, и только убедившись, что достигли цели, приступайте к его раскрашиванию, помните о смысловой нагрузке цвета.
- 8. Подготовьте устный рассказ по составленному конспекту.

Опорный конспект ПОЗВОЛЯЕТ обучающему:

Опорный конспект ПОМОГАЕТ преподавателю:
- наглядно представить весь изучаемый материал студентам;
- сконцентрировать внимание на отдельных наиболее трудных местах изучаемого материала;
- многократно повторять изучаемый материал;
- быстро, без больших временных и энергетических затрат, проверить, как студент понял и запомнил изученный материал;
- привлечь к контролю знаний родителей. Даже не зная и не особенно понимая, что он учит, они, проверив опорный конспект, могут увидеть, готов ли он к уроку.

Органическая химия схема-конспект по теме «Алкены»


Функции схема- конспектов в обучении
Познавательная (абстрагирования, обобщения, прогнозирования, систематизации, фиксации главного);
Формирующая понятия и личность обучающихся;
Развивающая и воспитывающая (пространственное и абстрактное мышление, системный и символический стиль мышления, экономность ума, интерес к учению);
Коммуникативная (кодирование и компактное предъявление информации, обсуждение результатов деятельности и обобщение );
Организующая (учебный материал, деятельность, сотрудничество).

В основе нового ФГОС лежит системно-деятельностный подход, который предъявляет к преподавателю новые требования.
Преподаватель должен быть профессионалом, демонстрировать универсальные и предметные способы действия, инициировать пробные действия обучающихся, искать способы включения в работу каждого.

Опорные конспекты помогают четко распределять учебное время, совмещать различные виды работ в единое целое, активизирует мыслительную деятельность, развивает логическое и абстрактное мышление, повышать интерес к предмету, помогают более осознанно запомнить материал за счет подключения к долговременной памяти человека.











































