
Координационная теория…
Самсонова Валентина, 11 "В" класс

- Координационная теория комплексных соединений Вернера включает в себя три основных положения:
- а) Элемент может иметь две валентности - главную (степень окисления) и побочную (так называемое координационное число).
- б) Каждый элемент стремится насытить обе эти валентности.
- в) Главная валентность не направлена, побочная валентность направлена к фиксированным положениям в пространстве.
… была создана в 1893 году швейцарским химиком Альфредом Вернером.
Самсонова Валентина, 11 "В" класс

Комплексообразователь…
в молекуле любого комплексного соединения один из ионов,
… обычно положительно заряженный,
занимающий центральное место.
- Также называется центральным ионом.
Самсонова Валентина, 11 "В" класс

некоторое число противоположно заряженных ионов…
Лиганды…
… или электронейтральных молекул, расположенное (или координированное)
вокруг комплексообразователя в непосредственной близости.
Самсонова Валентина, 11 "В" класс

Координационное число (КЧ)..
- число химических связей между комплексообразователем и лигандами.
Меняется от 2 до 8 (иногда выше). Чаще 4 и 6.
- Между значениями КЧ и степенью окисления комплексообразователя чаще всего существует зависимость:
- КЧ = степень окисления комплексообразователя х 2.
Самсонова Валентина, 11 "В" класс

- Число координационных мест, занимаемых лигандом называют дентатностью лиганда. Большинство лигандов – монодентатные, т.е. занимают одно координационное место (единицу валентности) центрального атома, например Cl -, NH 3. Встречаются и полидентатные лиганды (как правило, это органические вещества), одна частица которых занимает два и более координационных мест.
Самсонова Валентина, 11 "В" класс

- Центральный атом или ион с координированными вокруг него лигандами образуют внутреннюю сферу. В формулах комплексных соединений внутреннюю сферу (комплекс) часто заключают в квадратные скобки.
- Ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального иона, составляют внешнюю координационную сферу (противоионы).
Самсонова Валентина, 11 "В" класс

В зависимости от заряда внутренней сферы комплексные соединения подразделяются на анионные, катионные и нейтральные комплексы. Комплексный анион:
Самсонова Валентина, 11 "В" класс
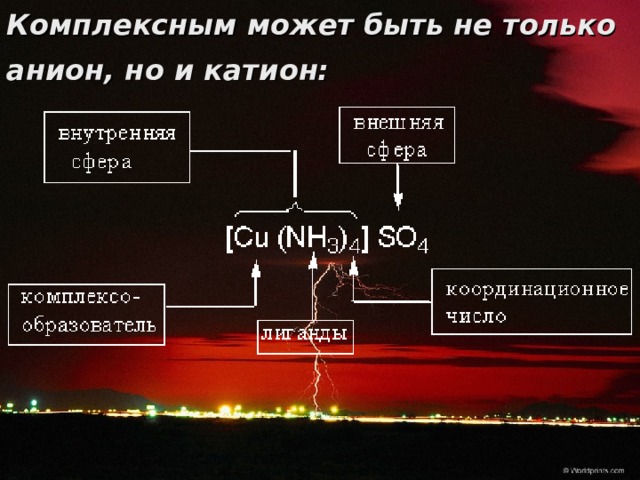
Комплексным может быть не только анион, но и катион:
Самсонова Валентина, 11 "В" класс

Комплексной может быть также нейтральная частица:
Самсонова Валентина, 11 "В" класс
![При составлении названия комплексного соединения его формула прочитывается справа налево. Рассмотрим конкретные примеры: K 3 [ Fe ( CN ) 6 ] гексацианоферрат(III) калия Na [ Al ( OH ) 4 ] тетрагидроксоалюминат натрия Na 3 [ Co ( NO 2) 6 ] гексанитрокобальтат(III) натрия [ Cu ( NH 3 ) 4 ] SO 4 сульфат тетраамминмеди( II ) [ Cr ( H 2 O ) 6 ] Cl 3 хлорид гексааквахрома( III ) [ Ag ( NH 3 ) 2 ] OH гидроксид диамминсеребра(I) Самсонова Валентина, 11](https://fsd.multiurok.ru/html/2020/08/25/s_5f455338396b5/img10.jpg)
При составлении названия комплексного соединения его формула прочитывается справа налево. Рассмотрим конкретные примеры:
- K 3 [ Fe ( CN ) 6 ] гексацианоферрат(III) калия
- Na [ Al ( OH ) 4 ] тетрагидроксоалюминат натрия
- Na 3 [ Co ( NO 2) 6 ] гексанитрокобальтат(III) натрия
- [ Cu ( NH 3 ) 4 ] SO 4 сульфат тетраамминмеди( II )
- [ Cr ( H 2 O ) 6 ] Cl 3 хлорид гексааквахрома( III )
- [ Ag ( NH 3 ) 2 ] OH гидроксид диамминсеребра(I)
Самсонова Валентина, 11 "В" класс

В названиях комплексных соединений число одинаковых лигандов указывают числовыми приставками, которые пишут слитно с названиями лигандов: 2 – ди, три, 4 – тетра, 5 – пента, 6 – гекса, 7 – гепта, 8 – окта.
Названия отрицательно заряженных лигандов, анионов различных кислот, состоят из полного названия (или корня названия) аниона и окончания с гласной буквой –о. Например:
- I – иодо-
- H – гидридо-
- CO 32– карбонато-
Некоторые анионы, выполняющие роль лигандов, имеют специальные названия:
- ОН– гидроксо-
- S 2– тио-
- CN – циано-
Самсонова Валентина, 11 "В" класс

- В названия нейтральных лигандов обычно специальные приставки не используются, например: N 2 H 4 - гидразин, С2Н4 – этилен, С5Н5 N – пиридин.
- По традиции оставлены специальные названия у небольшого числа лигандов: H 2 O – аква-, NH 3 – амин, CO – карбонил, NO – нитрозил.
Названия положительно заряженных лигандов оканчивается на –ий: NO + - нитрозилий, NO 2+ - нитроилий и т.д.
Самсонова Валентина, 11 "В" класс
![Если элемент, являющийся комплексообразователем, входит в состав комплексного аниона, то к корню названия элемента (русского или латинского) добавляется суффикс –ат и в скобках указывается степень окисления элемента-комплексообразователя. (Примеры приведены выше). Если элемент, являющийся комплексообразователем, входит в состав нейтрального комплекса без внешней сферы, то в названии остается русское название элемента с указанием его степени окисления. Например: [ Ni ( CO ) 4 ] – тетракарбонилникель(0). Самсонова Валентина, 11](https://fsd.multiurok.ru/html/2020/08/25/s_5f455338396b5/img13.jpg)
- Если элемент, являющийся комплексообразователем, входит в состав комплексного аниона, то к корню названия элемента (русского или латинского) добавляется суффикс –ат и в скобках указывается степень окисления элемента-комплексообразователя.
- (Примеры приведены выше). Если элемент, являющийся комплексообразователем, входит в состав нейтрального комплекса без внешней сферы, то в названии остается русское название элемента с указанием его степени окисления. Например: [ Ni ( CO ) 4 ] – тетракарбонилникель(0).
Самсонова Валентина, 11 "В" класс

Презентацию подготовила учитель химии МОУСОШ №5 Рощепкина Нина Алексеевна…
Самсонова Валентина, 11 "В" класс

















![При составлении названия комплексного соединения его формула прочитывается справа налево. Рассмотрим конкретные примеры: K 3 [ Fe ( CN ) 6 ] гексацианоферрат(III) калия Na [ Al ( OH ) 4 ] тетрагидроксоалюминат натрия Na 3 [ Co ( NO 2) 6 ] гексанитрокобальтат(III) натрия [ Cu ( NH 3 ) 4 ] SO 4 сульфат тетраамминмеди( II ) [ Cr ( H 2 O ) 6 ] Cl 3 хлорид гексааквахрома( III ) [ Ag ( NH 3 ) 2 ] OH гидроксид диамминсеребра(I) Самсонова Валентина, 11](https://fsd.multiurok.ru/html/2020/08/25/s_5f455338396b5/img10.jpg)


![Если элемент, являющийся комплексообразователем, входит в состав комплексного аниона, то к корню названия элемента (русского или латинского) добавляется суффикс –ат и в скобках указывается степень окисления элемента-комплексообразователя. (Примеры приведены выше). Если элемент, являющийся комплексообразователем, входит в состав нейтрального комплекса без внешней сферы, то в названии остается русское название элемента с указанием его степени окисления. Например: [ Ni ( CO ) 4 ] – тетракарбонилникель(0). Самсонова Валентина, 11](https://fsd.multiurok.ru/html/2020/08/25/s_5f455338396b5/img13.jpg)











