Просмотр содержимого документа
«Презентация к уроку химии на тему "Предельные углеводороды (алканы)"»

Предельные углеводороды (алканы)
Автор: преподаватель химии ГБПОУ ВМТ
Дзагоева Ф.Б.

План
- Понятие «алканы».
- Гомологический ряд алканов.
- Изомерия и номенклатура алканов.
- Химические свойства алканов.
- Получение алканов.
- Области применения алканов.

Определение
Предельными углеводородами или алканами , называют углеводороды, в молекулах которых все атомы углерода связаны одинарными связями и подчиняются общей формуле С n H 2n+2
Ряд веществ, сходных по строению и свойствам. Но отличающихся друг от друга по составу на одну или несколько групп –СН 2 -, называют гомологическим рядом. Вещества такого ряда называют гомологами .
Радикалы – это активные частицы, образующиеся за счет отщепления от молекулы алкана одного атома водорода.
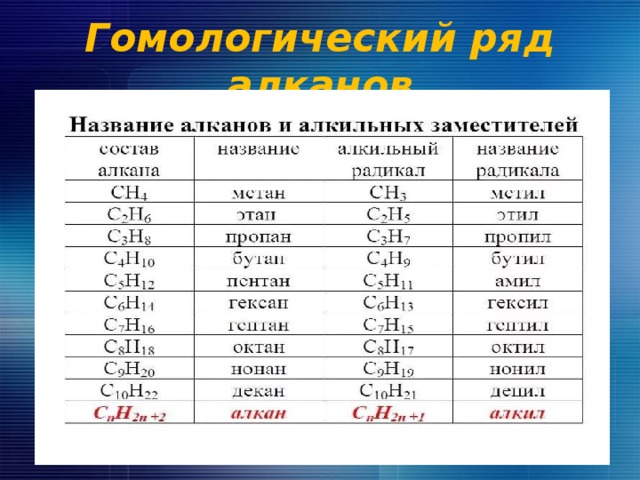
Гомологический ряд алканов

Изомерия алканов
- Структурная изомерия алканов – изомерия углеродного скелета
- Например : C 4 H 10 – бутан
С – С – С – С С – С – С
|
С
CH 3 – CH 2 - CH 2 - CH 3 CH 3 - CH - CH 3
|
CH 3

Номенклатура алканов
- Выбрать в молекуле самую длинную цепочку атомов углерода.
- Пронумеровать атомы углерода в цепочке с того конца, к которому ближе разветвление.
- Записать основу названия вещества - название углеводорода с тем же числом атомов углерода, что и в пронумерованной цепи.
- Перед основой названия перечисляют все заместители основной цепи с указанием номеров атомов углерода, при которых они стоят. Если одинаковых заместителей несколько, то перед их названиями указывают ди-, три-, тетра-, пента-, и т.д.
- Все цифры отделяют друг от друга запятыми, буквы от цифр – дефисами. Если при одном углеродном атоме имеется не один, а два заместителя его цифру повторяют в названии дважды.

Химические свойства
CH 4 + О 2 → CО 2 + 2H 2 О + Q
С 3 Н 8 + 5О 2 → 3CО 2 + 4H 2 О + Q
- Реакции замещения - хлорирования
Свет
CH 4 + Cl 2 → CH 3 Cl + HCl
метан хлорметан
CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl
хлорметан дихлорметан
CH 2 Cl 2 + Cl 2 → CH 3 Cl + HCl
дихлорметан трихлорметан
CH 3 Cl + Cl 2 → CCl 4 + HCl
трихлорметан тетрахлориетан

Химические свойства
3. Реакция разложения.
CH 4 → C + 2H 2
Продуктом неполного разложения метана является ацетилен
2 CH 4 → CН ≡ СН + 3H 2
4. Реакция отщепления (дегидрирования).
СН 3 -СН 3 → СН 2 =СН 2 + Н 2
этан этилен
5. Реакция изомеризации.
AlCl 3
СН 3 –СН 2 – СН 2 – СН 3 → СН 3 – СН – СН 3
|
н- бутан СН 3
изобутан ( 2-метилпропан)

Получение алканов
- Природный способ : из природного газа и нефти.
- Синтез из простых веществ: С + 2Н 2 → СН 4 + Q
- Реакция Вюрца: 2СН 3 Сl + 2Na → C 2 H 6 + 2NaCl
- Из солей карбоновых кислот (лабораторный способ):
t
CH 3 -COONa (тв.) + NaOH (тв.) → CH 4 ↑ + Na 2 CO 3

Применение алканов
- В качестве топлива в быту, на производстве. А так же для двигателей внутреннего сгорания.
- В органическом синтезе:
- Получают водород, сажу, резину, типографскую краску.
- Получение ацетилена.
- Синтетические моющие средства.
- Получают спирты, альдегиды, карбоновые кислоты.
- Получение растворителей.
- Получение хладагентов, используемых в холодильниках.

Задания
- Какие из приведенных формул принадлежат предельным углеводородам: С5Н10, С2Н6, С6Н8, С3Н6, С4Н10, С12Н26?
- Назовите следующие алканы по международной номенклатуре: а) СН 3 -СН 2 -СН 3 ; б) б) СН 3 -СН 2 -СН-СН 2 -СН 3
|
СН 3
в) СН 3 -СН-СН-СН 3
| |
СН 3 СН 3
СН 3
|
г) СН 3 -СН 2 -С-СН 3
|
СН 3
д) СН 3 -СН 2 -СН-СН 2 -СН 2 -СН 3
|
С 2 Н 5

Задания
- Напишите структурные формулы следующих углеводородов: а) 2-метилгексан; б) н-пентан; в) 2,2-диметилбутан; г) 2,2-диметил,4-этилгексан; д) 2-метил, 4-этилгекс ан; е) 2.3.4- триметилпентан.
- Напишите структурные формулы двух гомологов и двух изомеров пентана. Назовите эти углеводороды.
- Напишите уравнения следующих реакций: а) горение этана; б) взаимодействие 1моль этана с 1 молем хлора; в) дегидрирование пропана.
- Какое количество теплоты выделится при сгорании 448 л (н.у.) метана в соответствии с термохимическим уравнением: СН 4 + 2О 2 → С О 2 + 2Н 2 О + 900 кДж



































