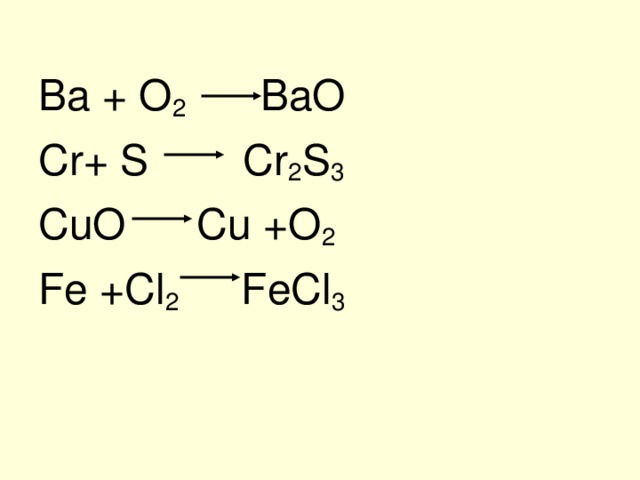Просмотр содержимого документа
«Презентация к уроку "Закон сохранения массы вещества.Химические уравнения"»

Закон сохранения массы вещества. Химические уравнения.
Заполните схему:
Явления
?
?
→

Укажите химические явления:
а) Распространение запаха духов;
б) Ржавление железа;
в) Испарение воды;
г) Получение сахарной пудры из кристаллов сахара;
д) Гниение растительных остатков;
е) Почернение серебряных изделий.

Признаки реакций:
- Появление осадка;
- Выделение газа;
- Выделение ( или поглощение ) энергии( тепла и света)
- Изменение цвета;
- Появление запаха.
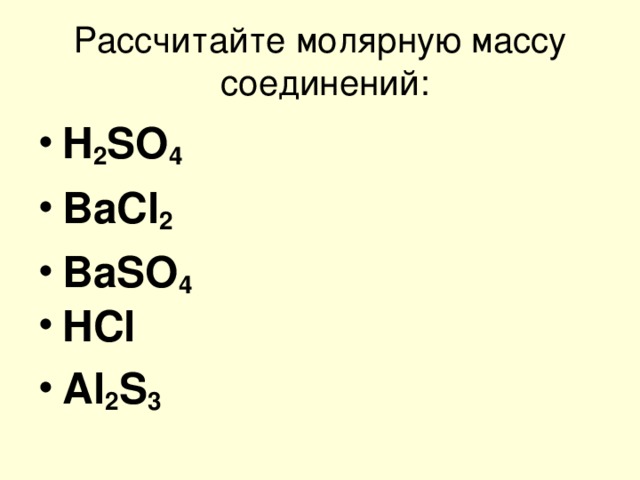
Рассчитайте молярную массу соединений:
- H 2 SO 4
- BaCl 2
- BaSO 4
- HCl
- Al 2 S 3

- H 2 SO 4 98г/моль
- BaCl 2 208г/моль
- BaSO 4 233 г/моль
- HCl 36,5 г/моль
- Al 2 S 3 150 г/моль

Коллекция учебных динамических слайдов по химии 8 класс.
Уравнение химической реакции – это условная запись химического процесса, посредством химических знаков и символов.
H 2
H 2
NH 3
N 2
NH 3
+
N 2
+
t 0 C кат.
t 0 C кат.
- реагирующие вещества
- продукты реакции
- взаимодействие
- условие протекания реакции
Баженов Алексей Анатольевич
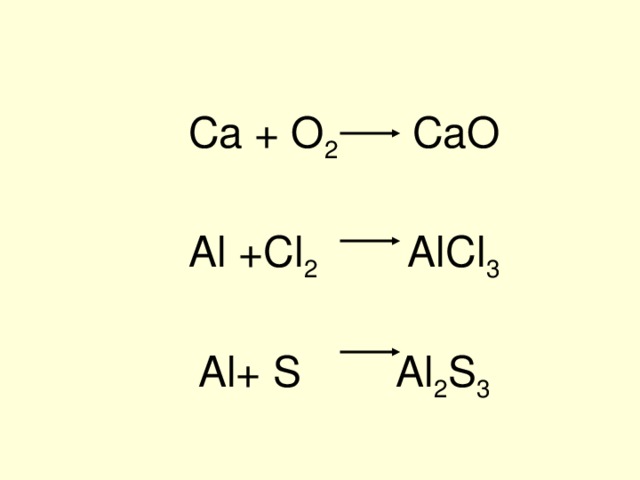
Ca + O 2 CaO
Al +Cl 2 AlCl 3
Al+ S Al 2 S 3
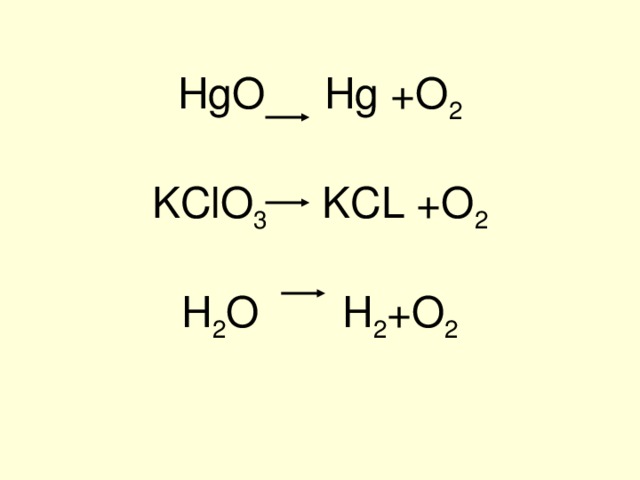
HgO Hg +O 2 KClO 3 KCL +O 2 H 2 O H 2 +O 2
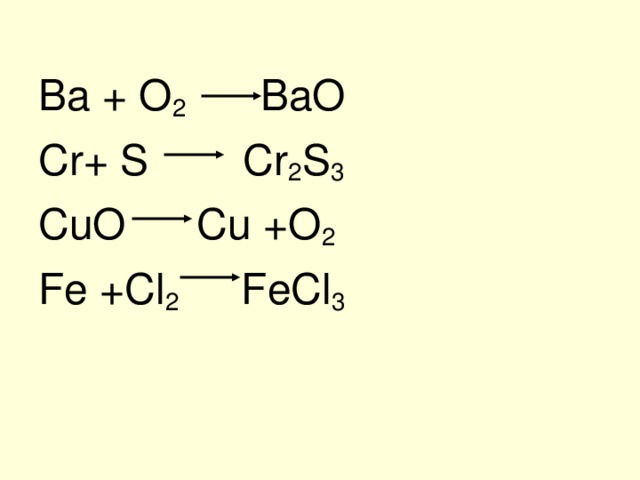
В a + O 2 В aO
С r+ S Cr 2 S 3
CuO Cu +O 2
Fe +Cl 2 FeCl 3
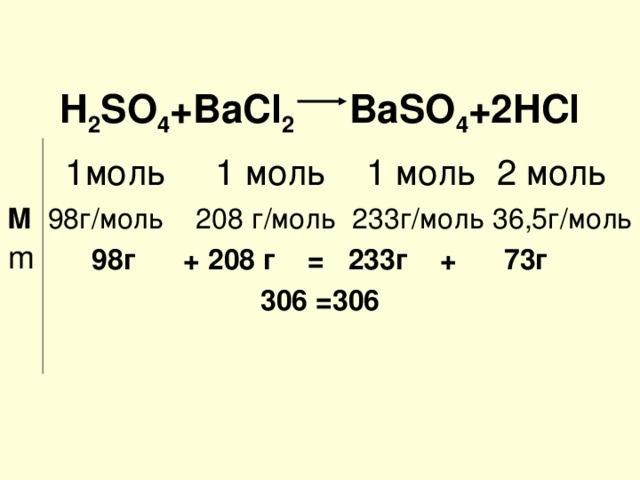
H 2 SO 4 +BaCl 2 BaSO 4 +2HCl
1 моль 1 моль 1 моль 2 моль
М 98 г/моль 208 г/моль 233г/моль 36,5г/моль
98 г + 208 г = 233г + 73г
306 =306
m
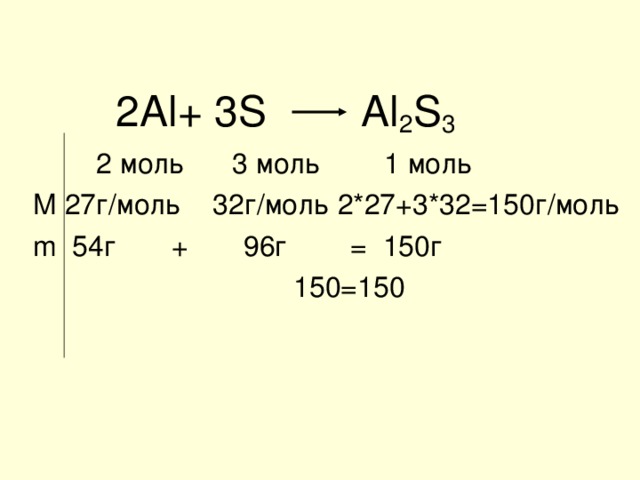
2Al+ 3S Al 2 S 3
2 моль 3 моль 1 моль
M 27г/моль 32г/моль 2*27+3*32=150г/моль
m 54г + 96г = 150г
150=150

- Почему при проведении опыта между раствором карбоната натрия и соляной кислоты в открытом сосуде массы веществ до и после реакции не равны?Почему нарушился закон сохрания массы вещества?
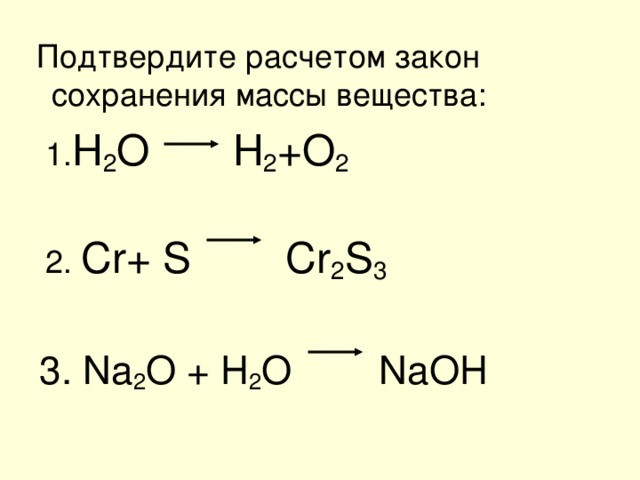
Подтвердите расчетом закон сохранения массы вещества:
1. H 2 O H 2 +O 2
2. С r+ S Cr 2 S 3
3. Na 2 O + H 2 O NaOH
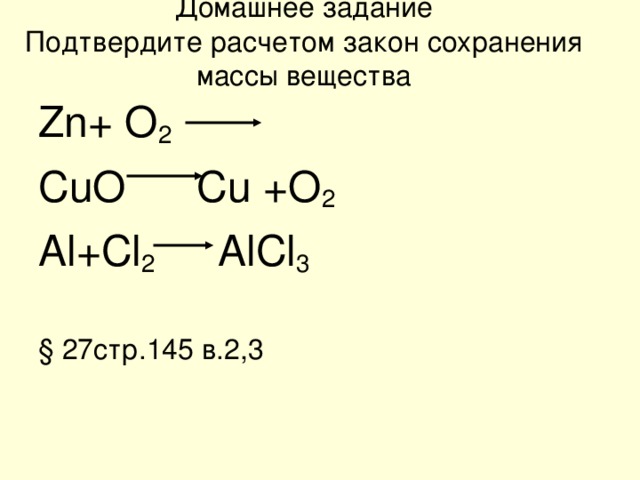
Домашнее задание Подтвердите расчетом закон сохранения массы вещества
Zn+ O 2
CuO Cu +O 2
Al+Cl 2 AlCl 3
§ 27стр.145 в.2,3