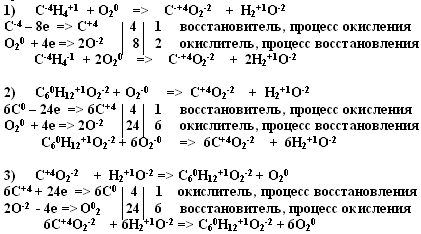Проект
Реализация требований ФГОС при изучении темы:
«Электролитическая диссоциация»
Содержание:
Введение. 3
Основная часть 8
1. Тематическое планирование уроков химии 9 класс 8
2. Урок по теме: "Кто-то теряет, а кто-то находит" 14
3. Урок по теме: «Гидролиз солей» 24
4. Итоговая контрольная работа 33
Заключение. 36
Список используемой литературы: 40
Введение.
Федеральные государственные образовательные стандарты общего образования отражают понимание научно-педагогическим сообществом вызовов, возникших перед отечественной системой образования в условиях её интеграции в мировое образовательное пространство. На современном этапе информационной революции в значительно изменились требования к образованному человеку. Сегодня ему невозможно знать всё о достижениях в естественных и гуманитарных науках, но очень важно научиться применять свои знания в конкретных жизненных ситуациях. В XXIв. актуальным становится формирование личностной готовности и способности к непрерывному образованию, формированию компетенций, востребованных на рынке труда. В условиях повышения мобильности, развития миграционных процессов все более значимым становится воспитание российской гражданской идентичности молодых россиян, выпускников общеобразовательных учреждений. В связи с формированием современной насыщенной информационно-образовательной среды не менее важно обеспечить переход к новой образовательной парадигме системно-деятельностного обучения. Стандарты общего образования первого поколения, регламентирующие содержание образования в дидактических единицах, соответствовали классической образовательной парадигме конца XX в. В начале XXI в. они перестали выполнять функцию педагогической поддержки развития образовательного пространства. Осознание экспертным научно-педагогическим сообществом потребности в новых инструментах развития образовательного пространства России в XXI в. привело к разработке новых образовательных стандартов. Принципиальным отличием государственных образовательных стандартов второго поколения является усиление их ориентации на результаты образования как системообразующий компонент конструкции стандартов. В новых стандартах объектом стандартизации стало не содержание образования, ориентированное на достижение относительно частных предметных образовательных результатов, а система требований к образовательным результатам – личностным, метапредметным и предметным. Стандарт общего образования второго поколения представляет совокупность требований, обязательных при реализации основной образовательной программы основного общего образования образовательными учреждениями, имеющими государственную аккредитацию. В соответствии с новым методологическим подходом изменились структура и содержание стандартов. Основными документами, составляющими нормативный пакет ФГОС, выступают требования к результатам, структуре и условиям освоения основной образовательной программы основного общего образования. В сочетании с документами инструктивно-методического и рекомендательного характера они образуют систему всестороннего и разноуровневого сопровождения стандартов (нормативное, методологическое, инструментальное, технологическое, информационно-методическое).
Модернизация образования является в настоящее время приоритетной задачей российской образовательной политики.
Под модернизацией подразумевается – «повышение доступности качественного образования, соответствующего требованиям инновационного развития экономики, современным потребностям общества и каждого гражданина». Процесс модернизации направлен на приведение системы образования в соответствие с новыми показателями качества.
Качество образования зависит, с одной стороны, от соблюдения требований образовательных стандартов. А с другой стороны, ФГОС – лишь инструмент, для попыток управлять качеством образования в масштабах страны. Этот инструмент может быть интерпретирован по-своему всеми участниками образовательного процесса.
Сейчас отсутствуют критерии оценки образования, включая самооценку участников образовательного процесса и общественную экспертизу, оценка качества происходит только в ракурсе результатов ЕГЭ и ОГЭ.
ЕГЭ хотя и является очень важным элементом системы оценки качества образования, но этот экзамен в полной мере не дает исчерпывающей информации для управления его качеством, из-за ряда случайных факторов. Так же следует отметить, что качество получаемого образования не всегда соответствует качеству предлагаемого образования. И поэтому,желательно, чтоб данный экзамен оставался основным, но не единственным. Есть необходимость создания системы оценки качества образования, в связи с потребностью получения объективной информации о результатах обучения.
Следовательно, необходимы ориентиры для сравнения надежности системы оценивания. Хотя интенсивно разрабатываются образовательные программы по совместной деятельности школ как партнеров в области общеевропейского образования и программ по участию в международных проектах, следует подчеркнуть слабую интеграцию в международные системы оценки качества.
Россия принимает участие в международных исследованиях достижений в области образования, к сожалению, результаты российских выпускников значительно ниже, чем средние международные результаты. Это подтверждают ту точку зрения, которая гласит, что «существующее содержание общего образования - крайне устаревшее и перегруженное, наукообразное и нефункциональное, оторванное от реальных потребностей жизни». В действительности, российская школа, обеспечивая довольно высокие академические знания, но недостаточно учит школьников их применению на практике, но ведь важнейшим социальным требованием к школе является ориентация образования на целостное развитие личности школьника, на формирование у него познавательных и созидательных способностей, необходимых для успешной социализации.
Поэтому, модернизация подразумевает сокращение объема обязательного для освоения содержания, но главное, в погоне за более качественным образованием, отвечающим требованиям современного общества, не утратить, то положительное, что существовало в старой системе образования!!!
Понятие «качество образования» - социально-педагогический феномен. На данном этапе наше образование приобрело большую социальную направленность. Родители могут участвовать в формировании индивидуальных образовательных маршрутов своих детей. Такой тандем «ученик - родитель – учитель» может добиться более высоких результатов, т.к. уровень познавательной мотивации у учащегося зависит не только от заинтересованности учителя и тех методов и приемов, которые он использует, но и от отношения родителей. К сожалению, даже при условии создания динамичной информационно-образовательной среды учебного заведения и доступности, многие родители не реализуют свои права в сфере образования, вследствие, присущего многим правового нигилизма.
В современных условиях радикально меняется статус учителя, меняются требования к его профессионально-педагогической компетентности. Учитель переходит с позиции носителя знаний на позицию организатора познавательной деятельности. У учителей появилось больше возможностей для экспериментов и большая свобода в выборе форм, способов и приемов обучения. Хочется отметить, когда обучение было ориентировано на передачу знаний, процесс обучения не превращался из творческого процесса в рутинную работу, ибо личностно-ориентированная парадигма образования существовала всегда.
Пока традиции продолжают преобладать над инновациями. Проблема заключается не в учительском консерватизме, просто необходимо научиться, нам педагогам, внедрять эти идеи модернизации современного школьного образования в практику преподавания, ведь от этого зависит эффективность всего образовательного процесса. Необходимо, обновлять и изменять содержание образования, осуществлять отбор содержания обучения, осуществлять процесс обучения с пользой для дела можно только с опорой на фундаментальные закономерности, лежащие в основе обучения, т.е. реализовывать стандарт.
Мною для проекта выбрана тема «Электролитическая диссоциация», на неё отводится 11 часов.
Основная часть
1. Тематическое планирование уроков химии 9 класс
(2 часа в неделю к учебнику Г.Е. Рудзитиса, Ф.Г. Фельдмана)
Тема 1. Электролитическая диссоциация (11ч)
| № | Темы уроков | К/ч | Цель урока | Оборудование | Планируемые результаты | Дом. задание |
| предметные | метапредмет-ные | личностные |
| Электролиты и неэлектро-литы. Электролитическая диссо-циация веществ в водных растворах
| 1 | Познакомить с понятиями: электролит, неэлектролит ЭД, гидратация, кристалло-гидраты, с практичес-ким примене-нием крис-таллогидра-тов в быту, промышлен-ности | Прибор для демонстрации электропровод-ности различных веществ, дистиллированная вода, растворы: сахара, спирта, серной и уксусной кислот, щёлочи, хлорида натрия, сухой сульфат меди (II), медный купорос | Знать: Электролиты проводники второго рода, неэлектро-литы, ион, процессы протекающие при растворении в воде в-в раз.природы, причина и механизм ЭД | Наблюдение, обсуждение, выдвижение гипотез объясняющих результаты увиденных опытов Что такое эл-й ток Главная причина диссоциации, объяснять механизм ЭД в-в с ионной и ковалентной полярной связью | Я умею объяснять причину электропро-водности водных р-ров кислот, щелочей, солей и иллюстриро-вать примерами изученные понятия | §1, на выбор: !Упр.1-5; !!Подготовить презентацию «Практичес-кое примене-ние кристал-логидратов в быту или в промышлен-ности»
Реш.зад.1 стр13 |
| Электролити-ческая диссо-циация кис-лот, щелочей и солей.
| 1 | Дать определение кислот, щелочей и солей с точки зрения ТЭД; Научить записывать уравнения диссоциации кислот, щелочей и солей; Познакомить со строением иона гидроксония | Индикаторы: универсальный, метилоранж растворы кислот и щелочей | Определение кислот, щелочей и солей с точки зрения ТЭД; Записывать уравнения диссоциации кислот, щелочей и солей; Знать строение Н3О+ | Записывать уравнения диссоциации кислот, оснований, солей, определять в водных р-рах катион Н+ и анион ОН- , прогнозировать по ним св-ва веществ, сравнивать по строению и свойствам ионы и атомы | Я могу объяснить, чем обусловлены общие св-ва растворов кислот и щелочей Я умею составлять уравнения ЭД кислот, щелочей и солей; | §2, упр.8 с.13 или подготовить презентацию демонстри-рующею диссоциацию либо кислот, либо щелочей или солей;
|
| Слабые и сильные электролиты. Степень диссоциации. | 1 | Познакомить с понятием сильный и слабый электролит, степень диссоциации; закрепить умение писать уравнения диссоциации кислот, щелочей и солей. | Прибор для демонстрации электропровод-ности различных веществ, в-ва: NaCl(кр), Н2О, NaCl(р-р), р-ры разл. конц-ии HCl, CH3COOH, C12H22O11, CH3COONa(кр) Zn | Сила электролита, степень диссоциации, кол-ные характерис-тики силы электролита, влияние концентра-ции, темп-ры одноимённых ионов на α | Определять силы электролита по значению α, уметь вычислять α | Я могу объяснить, чем разл-тся слабые и сильные электролиты Я умею рассчитывать степень диссоциации электролита |
|
| Реакции ионного обмена и условия их протекания.
| 1 | Познакомить с понятием «Реакции ионного обмена» и условиями, при которых они протекают Формировать навыки составления полных и сокращённых ионных ур-ий | Штатив с пробирками, р-ры в-в: NaOH, FeCl3, Na2CO3, CaCl2, HCl, KNO3, Ca(OH)2, CuSO4, BaCl2, AgNO3, KI, Al2(SO4)3 | Реакции ионного обмена и условия их протекания, качественные р-ции, реактив, полные и сокращённые ионные ур-ия | Составлять полные и сокращённые ионные ур-ия, физ.смысл сокращённого ионного ур-ния | Я знаю условия протекания реакций ионного обмена Я умею составлять полные и сокращенные ионные уравнения реакций |
|
| Урок - практикум по составлению реакций ионного обмена.
| 1 | Закрепить навыки составления полных и сокращённых ионных ур-ий, знание условий, при которых они протекают |
| Реакции ионного обмена и условия их протекания, качественные р-ции, реактив, полные и сокращённые ионные ур-ия | Составлять полные и сокращённые ионные ур-ия, физ.смысл сокращённого ионного ур-ния | Я знаю условия протекания реакций ионного обмена Я умею составлять полные и сокращенные ионные уравнения реакций |
|
| Окислитель-но-восстано-вительные реакции. Окисление и восстановле-ние. | 1 | Дать понятие о ОВР, о правилах составления электронного баланса; Познакомить с основными окислителями и восст-лями; Научить определять степень окисления элементов в соединениях |
| ОВР, метод электронного баланса, степень окисления, окислитель, восстанови-тель, процессы окисления и восстановле-ния | Уметь определять : ОВР, степень окисления, окислитель и восстановитель, процессы окислительный и восст-й | Я могу определить, явл-тся ли реакция окислитель-но-восстано-вительной Я умею расставлять коэффициен-ты в ур-ниях ОВР методом электронного баланса |
|
| Урок-практикум: Окислительно-восстанови-тельные реакции. | 1 | Совершенст-вовать умение составлять уравнения ОВР с исполь-зованием метода электронного баланса |
| ОВР, метод электронного баланса, степень окисления, окислитель, восстанови-тель, процессы окисления и восстановле-ния | Уметь определять : ОВР, степень окисления, окислитель и восстановитель, процессы окислительный и восст-й | Я могу определить, явл-тся ли реакция окислитель-но-восстано-вительной Я умею расставлять коэффициен-ты в ур-ниях ОВР методом элек-тронного баланса |
|
| Гидролиз солей.
| 1 | Познакомить с реакцией гидролиза; научить определять реакцию среды и прог-нозировать ход гидролиза | Штатив с пробирками, в-вa: NaCl, CuSO4, Na2CO3, Fe2S3, NH4Cl, H2O Индикаторы: универсальный, метилоранж | Гидролиз соли, классифика-ция солей по типу гидролиза | Записывать молекулярные и ионные уравнения гидролиза солей, определять рН среды | Я умею определять характер среды растворов солей по их составу |
|
| Практи-ческая работа №1. Решение эксперимен-тальных задач по теме «Электроли-тическая диссоциация». | 1 | Закрепить знания по данной теме, формировать практические умения и навыки выполнения лабораторных работ |
| Качественные реакции | Уметь | Я умею проводить качественные р-ции на ионы Я могу записывать ионные ур-ия реакций в полном и сокращенном виде |
|
| Повторитель-но – обоб-щающий урок по теме: «Электролитическая диссо-циация». | 1 | Закрепить, углубить знания учащихся по данной теме |
|
| Уметь применять знания, умения и навыки, полученные при изучении темы «Электролити-ческая диссоциация» |
|
|
| Контрольная работа №1 по теме: «Электроли-тическая диссоциация» | 1 | Закрепить, углубить и проконтроли-ровать знания учащихся по данной теме |
|
| Уметь применять знания, умения и навыки, полученные при изучении темы «Электролити-ческая диссоциация» | Работа с основными компонентами задания, проведения сравнения, формулирова-ние проблемы и определения способов её решения |
|
2. Урок по теме: "Кто-то теряет, а кто-то находит" (окислительно-восстановительные реакции)
Предлагается разработка урока по теме “Окислительно-восстановительные реакции” для обучающихся 8-х классов. Приоритет разработки данной темы в том, что с небольшими изменениями (с учетом специфики учебного заведения и способностями учащихся) ее можно использовать учителям, работающим по разным учебникам и разным программам, так как она очень актуальна. Представлена презентация к уроку и распечатка маршрутного листа для обучающихся.
Проблемная тема урока: “Кто-то теряет, а кто-то находит”.
Цели урока:
формирование общеучебных умений и навыков, носящих в современных условиях общенаучный и общеинтеллектуальный характер;
развитие у обучающихся теоретического, творческого, логического и операционного мышления.
Задачи урока:
1) Учебная – расширить и закрепить:
– знания обучающихся о свойствах металлов и неметаллов, типах химических реакций;
– умения показывать электронные переходы в ОВР, определять значение степени окисления химических элементов;
– навыки составления электронного баланса и расстановки коэффициентов в уравнениях окислительно-восстановительных реакциях.
2) Воспитательная – воспитывать чувство патриотизма.
3) Развивающая – расширение кругозора обучающихся, развитие умений и навыков применения полученных знаний для объяснения явлений окружающего мира.
Ход урока
I. Организационный момент
II. Введение в тему
Летом 2007 года в Европе были подведены итоги конкурса "Семь новых чудес света". Голосование проходило по Интернету, и отдать свой голос "за чудо" мог каждый желающий. Можно только догадываться, почему в список победителей не вошел ни один российский памятник, даже московский собор Василия Блаженного.
Газета "Известия", телеканал "Россия" и радиостанция "Маяк" выдвинули инициативу дать свой ответ "Семи новым чудесам света". Цель проекта “Семь чудес России” – возрождение чувства патриотизма и любви к своему Отечеству, а также привлечение внимания к восстановлению и сохранению исторических, культурных и природных объектов на территории нашей Родины. Итоги голосования по долгосрочному федеральному общероссийскому проекту были объявлены во время праздничного концерта на Красной площади по случаю Дня России. К “Чудесам” России относятся:
Долина гейзеров на Камчатке, озеро Байкал, дворцовый комплекс Петергоф под Санкт-Петербургом, природный памятник “Столбы выветривания” в Коми, собор Василия Блаженного в Москве, Мамаев курган и статуя Родины-матери в Волгограде, гора Эльбрус.
Результатом проекта стало составление нового “Золотого маршрута по России”, по которому, при желании, вы можете отправиться в путешествие.
Воображение правит миром
Наполеон 1
А если бы объявили конкурс “Семь чудес науки химии”? Какое, всем вам известное вещество возглавило бы список претендентов?
– Конечно же, вода. Я нисколько не сомневаюсь, что вы приведете массу доказательств того, что это удивительное вещество достойно первого места в списке. А вот на второе место я бы поставила окислительно-восстановительные процессы. Почему? На этот вопрос мы и постараемся ответить с вами в процессе урока.
Тема нашего урока: “Окислительно-восстановительные реакции”
III. Основная часть урока. Формирование новых знаний
П редставьте себе, что Вы стоите перед домом, где живут удивительные существа (Ме, НеМе). Каждый житель имеет свою квартиру, живет на определенном этаже и в определенном подъезде. Представители высшего общества занимают элитный 8 подъезд, они держатся особняком, в контакты ни с кем не вступают и очень самодостаточны (Почему?). Все остальные жители очень хотят быть похожими на них. Для этого одни отдают, а другие принимают электроны. В этом случае атомы превращаются в ионы, которые имеют такую же электронную конфигурацию, как ближайшие к ним инертные газы.
редставьте себе, что Вы стоите перед домом, где живут удивительные существа (Ме, НеМе). Каждый житель имеет свою квартиру, живет на определенном этаже и в определенном подъезде. Представители высшего общества занимают элитный 8 подъезд, они держатся особняком, в контакты ни с кем не вступают и очень самодостаточны (Почему?). Все остальные жители очень хотят быть похожими на них. Для этого одни отдают, а другие принимают электроны. В этом случае атомы превращаются в ионы, которые имеют такую же электронную конфигурацию, как ближайшие к ним инертные газы.
Ar +18 ) ) ) Ar0
2 8 8


Ca0 +20 ) ) ) ) Ca2+ +20 ) ) ) Ca0 - 2ē → Ca2+
2 8 8 2 2 8 8
атом ион


S0 +16 ) ) ) S2- +16 ) ) ) S0 + 2ē → S2-
2 8 8 2 8 8
2ē
![]()
![]()

Ca0 + S0 = Ca+2S-2
Электрон давно завоевал физику и химию, став для них почти что идолом. Все окислительно-восстановительные реакции находятся во власти электронных переходов от одного атома к другому как внутри молекулы, так и между ними. Перемещение электронов сопровождается изменением степени окисления атомов, участвующих в этих процессах.
Просмотр творческой работы обучающегося и его комментарии к ней:
Свойство металлов – отдавать электроны: у магния на последнем энергетическом уровне два электрона, которые он легко отдает, превращаясь в положительно заряженный ион. Свойство неметаллов – присоединять электроны: у серы на последнем энергетическом уровне 6 электронов, до завершения уровня не хватает двух электронов, которые она присоединяет, образуя анион.
Просмотр творческой работы обучающегося и его комментарии к ней:
“Окислитель, как грабитель, забирает электрон”. Хлор более сильный окислитель, чем сера, поэтому при взаимодействии железа с хлором образуется хлорид железа (+3)
2ē
![]()
![]()

2Fe0 + 3Cl20 = 2Fe+3Cl3-1
Вторая тема нашего урока: “Кто-то теряет, а кто-то находит”. (Почему?)
ОВР – это такие реакции, при которых происходит переход электронов от одних атомов, ионов или молекул к другим.
Окисление – это процесс отдачи электронов, степень окисления при этом повышается.
Восстановление – это процесс присоединения электронов, степень окисления при этом понижается.
Атомы, молекулы или ионы, отдающие электроны, являются восстановителями.
Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями.
Окисление всегда сопровождается восстановлением, а восстановление - окислением.
ОВР – это единство двух противоположных процессов: окисления и восстановления.
IV. Закрепление полученных знаний
Покажите электронные переходы в следующих ОВР.
2Li0 + O20 = Li2+O2-
C0 + O20 = C+4O2-2
2H20 + O20 = 2H2+O-2
2. Назовите окислитель и восстановитель.
V. Расширение и развитие полученных знаний

Во многих ОВР очень трудно расставить коэффициенты, для этого используют метод электронного баланса, который основан на сравнении степеней окисления в исходных и конечных веществах.
VI. Закрепление знаний
1. Из приведенных схем выпишите уравнения реакций, которые можно отнести к ОВР

2. Расставьте коэффициенты методом электронного баланса в следующих схемах ОВР

Определите окислитель, восстановитель, процесс окисления и восстановления.
3. Проверка выполнения задания (2)с помощью интерактивной доски (функция “штора”), или презентации
VII. Значение и применение ОВР
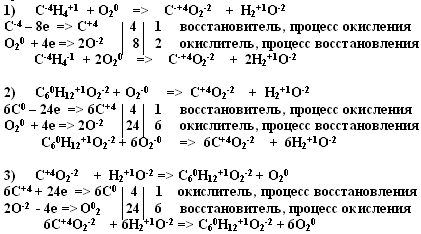
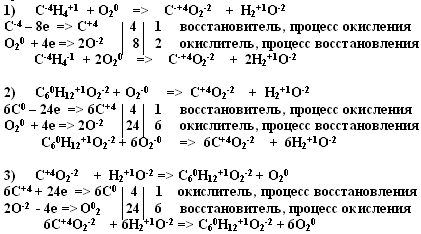
Вопросы к учащимся:
– Какой процесс отражает первое уравнение реакции?
– Какое значение имеют реакции горения?
– Какой процесс отражает второе уравнение реакции?
Первый вдох новорожденного говорит о начале новой жизни.
– Каковы функции дыхания?
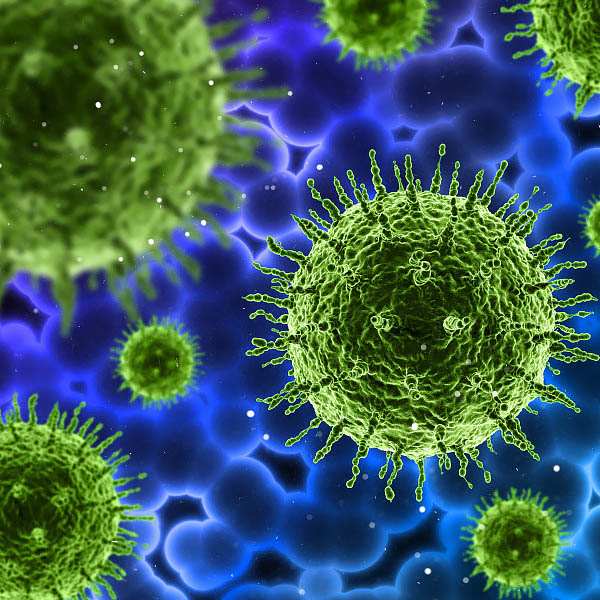
Дыхание — основная форма диссимиляции у человека, животных, растений и многих микроорганизмов. При дыхании богатые энергией вещества, принадлежащие организму, полностью разлагаются до бедных энергией неорганических конечных продуктов (диоксида углерода и воды), используя для этого молекулярный кислород. Под внешним дыханием понимают газообмен между организмом и окружающей средой, включающий поглощение кислорода и выделение углекислого газа, а также транспорт этих газов внутри организма.
– Какой процесс отражает третье уравнение реакции?
– Какова функция фотосинтеза. Его значение?
Фотосинтез – процесс образования органических веществ из углекислого газа и воды на свету в зеленых листьях. Фотосинтез, является одним из самых распространенных процессов на Земле, он обуславливает природные круговороты углерода, кислорода и других элементов и обеспечивает материальную и энергетическую основу жизни на нашей планете. Фотосинтез является единственным источником атмосферного кислорода. К тому же фотосинтез снабжает человечество топливом (древесина, уголь, нефть), волокнами (целлюлоза) и бесчисленными полезными химическими соединениями. Процесс фотосинтеза является также основой питания всех живых существ, так как связанный из воздуха в процессе фотосинтеза углекислый газ и вода, образуют около 90-95% сухого веса урожая. Остальные 5-10% приходятся на минеральные соли и азот, полученные из почвы.
Как вы считаете, возможно, ли было возникновение жизни на нашей планете без участия окислительно-восстановительных процессов?
Поведение итогов
Итак, приступаем к голосованию. Кто считает окислительно-восстановительные процессы, в основе которых лежат электронные переходы, “чудом” науки? Кто не согласен? Кто сомневается? Обсудить.
VIII. Домашнее задание
§5.
Творческое задание обучающимся. Рабочая тема “Семь аргументов в пользу “чуда””.
Предложите на звание “чуда” примеры из цикла наук предметов естественнонаучного цикла.
Маршрутный лист обучающихся
Проблемная тема урока: «Кто-то теряет, а кто-то находит»
Почему?
ОВР – это такие реакции, при которых происходит переход электронов от одних атомов, ионов или молекул к другим.
Окисление – это процесс отдачи электронов, степень окисления при этом повышается.
Восстановление – это процесс присоединения электронов, степень окисления при этом понижается.
Атомы, молекулы или ионы, отдающие электроны, являются восстановителями.
Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями.
Окисление всегда сопровождается восстановлением, а восстановление окислением.
ОВР - это единство двух противоположных процессов: окисления и восстановления.
Покажите электронные переходы в следующих ОВР.
Li0 + O20 = Li2O
C0 + O20 = CO2
H02 + O02 = H2O
Назовите окислитель и восстановитель.
______________________________________________________________________________________________________________________________________________________________________________
3. Mg + HNO3 = Mg(NO3)2 + N2 + H2O
- Расставим степень окисления химических элементов
- Выпишем те из них, в которых произошло изменение степени окисления
- Составим электронный баланс
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
- Определим окислитель и восстановитель
- Укажем процесс окисления и восстановления
- Расставим коэффициенты (уравнивая металлы, затем неметаллы, последним – водород)
- Проверяем правильность расстановки коэффициентов по кислороду
Ваши вопросы, которые требуют дополнительного объяснения
_________________________________________________________
_________________________________________________________
_________________________________________________________
4. С-4Н4+1 + О20 = C+4О2-2 + H2+1O-2
1 вариант
С60Н12+1О6-2 + О20 = С+4О2-2 + H2+1O-2
2 вариант
С+4О2-2 + H2+1O-2 = С60Н12+1О6-2 + О20
3 вариант
Кто считает окислительно-восстановительные процессы, в основе которых лежат электронные переходы, «чудом» науки? Почему?
____________________________________________________________________________________________________________________
Кто не согласен? Почему
____________________________________________________________________________________________________________________
Кто сомневается? Почему?
____________________________________________________________________________________________________________________
Домашнее задание
1. §5
2.Творческое задание обучающимся. Рабочая тема «Семь аргументов в пользу «чуда»»
3.Предложите на звание «чуда» примеры из цикла наук предметов естественнонаучного цикла.
Итоговая контрольная работа
«Теория электролитической диссоциации»
Вариант 1.
1. Какие из следующих электролитов при диссоциации образуют ионы H+ ; OH- ?
а) Са(OH)2 б) Zn(OH)2
в) H3PO4 г) Al(OH)3
2. Какие частицы являются анионами?
а) Fe3+ б) NO-3
в) SO42- г) Mn2+
3. Кислоты взаимодействуют с основными оксидами. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия оксида Mg (MgO) и серной кислоты.
4. Каким из следующих элементов могут соответствовать ионы с зарядом 2- ?
а) Ca б) O в) Fe г) S
5. Сколько ионов образуется при диссоциации молекулы Nа2SO4?
а) 2 б) 9 в) 3 г) 4
6. Нерастворимые основания растворяются под действием кислот. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия нерастворимого гидроксида железа Fe(OH)2 с азотной кислотой.
7. Какие электролиты являются сильными?
а) HI б)KOH
в) H2S г) Ba(NO3)2
8. Какие вещества образуют при диссоциации ионы Mn2+?
а) KMnO4 б) MnCl2
в) Na2MnO4 г) MnO2
9. Для солей характерно взаимодействие с кислотами. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия силиката Na (Na2SiO3) с соляной кислотой.
10. Какие частицы являются катионами?
а) Cr3+ б) SO32-
в)CrO42- г) Na+
Вариант 2.
1. При взаимодействии кислот с основаниями протекает реакция нейтрализации. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия гидроксида Na (NaOH) и бромводородной кислоты (HBr).
2. Каким из следующих элементов могут соответствовать ионы с зарядом 3+?
а) Ca б) O в) Fe г) Se
3. Какие из следующих электролитов при диссоциации образуют ионы H+ ; OH- ?
а) Сu(OH)2 б) Ba(OH)2
в) HCl г) Al(OH)3
4. Какие частицы являются анионами?
а) Al3+ б) Ca2+
в) Br - г) OH-
5. Какие электролиты являются сильными?
а) HCl б) NaOH
в) H2SО4 г) KNO3
6. Какие частицы являются катионами?
а) H+ б) CO32-
в)SO42- г) Mg 2+
7. Сколько ионов образуется при диссоциации молекулы K3PO4?
а) 2 б) 9 в) 3 г) 4
8. Основания взаимодействуют с растворами солей. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия гидроксида калия и сульфата меди (II) - CuSO4 .
9. Какие вещества образуют при диссоциации ионы Cl-?
а) KClO4 б) Ca(ClO)2
в) NaCl г) BaO
10. Для солей характерно взаимодействие друг с другом. Запишите молекулярное, полное и сокращенное ионные уравнения реакций взаимодействия нитрата серебра и бромида калия (KBr).
Заключение.
1.Роль теории электролитической диссоциации в развитии основных химических понятий.
Мы рассматрели методику изучения еще одной теории – теории электролитической диссоциации, она даёт возможность перевести знания учащихся на новый теоретический уровень. Давайте вспомним назначение научных теорий в школьном курсе химии:
теория позволяет объяснить,
научно описать,
предвидеть многие химические факты,
углубить понимание определенных вопросов,
развить базовые химические понятия,
усилить научность изложения,
усвоения химического содержания.
Образовательные цели темы:
сформировать представления о сущности процесса электролитической диссоциации, происходящей в растворах и расплавах веществ-электролитов;
развить понимание сущности и механизмов химических реакций, происходящих в растворе;
развить понятия о классах неорганических соединений на основе знаний их свойств как электролитов;
связать знания о поведении веществ в растворах со знаниями их внутреннего строения, типа химической связи, и пр.
Воспитательные задачи темы:
формировать научное мировоззрение, способствовать пониманию сущности важнейшей мировоззренческой идеи о связи свойств, состава и строения вещества,
создать дополнительные основания для понимания возможностей познания мира, заложить фундамент понимания многих химических процессов, происходящих в растворах,
объяснить причины реакционной способности веществ, научить определять направление многих реакций.
Развивающее значение темы:
тема позволяет углубить знания о веществах, их разнообразии,
о химических реакциях и их движущих силах;
в данной теме формируется целый комплекс новых практических умений – с помощью особой символики изображать и объяснять сущность процесса ЭЛД, реакций ионного обмена, гидролиза;
в теме учащиеся системно осваивают основы качественного анализа,
здесь решаются экспериментальные задачи по распознаванию веществ- электролитов.
Теория электролитической диссоциации изучается либо в 9 классе (1 четверть) – по учебникам Гузея, Рудзитиса и Кузнецовой, либо по программе Габриеляна – в конце 8 класса. В разных учебниках данная тема может быть выделена под соответствующим названием «Электролитическая диссоциация», или называться немного иначе это не имеет существенного значения, поскольку основное содержание данного учебного материала остается инвариантным и входит в любой учебный курс. Это четвертая теоретическая ступень, по которым происходит восхождение учащихся к научному химическому знанию.
Опорными знаниями для осознанного восприятия данной темы являются:
Теория строения атома и вещества, учение о химической связи
Учение о классах неорганических соединений, их общих свойствах, сходстве и различии различных представителей классов
Связь свойств веществ различных классов неорганических соединений с положением элементов в Периодической системе, предсказание этих свойств на основании положения в Периодической системе.
2.Логическая структура учебного материала
А теперь создадим Логическую структуру темы. Она может быть представлена следующими блоками понятий и логических суждений:
Что такое электролиты? Введение понятия «электролит» как вещество, проводящее ток в растворах или расплавах
Зависимость электролитических свойств от строения вещества, а именно типа химической связи - к электролитам относятся вещества с ионной и ковалентной полярной связью.
Сущность электролитической диссоциации – распад на ионы под действием полярного растворителя или высокой температуры. То есть условия электролитической диссоциации – строение вещества и присутствие растворителя или температуры
Механизм электролитической диссоциации – разрушение кристаллической решетки ионного соединения или разрыв полярной связи в молекуле ковалентного соединения
Свойства ионов, сравнении иона и нейтрального атома
Электролиты диссоциируют по – разному:
Введение понятия «сила электролита» - легкость распада вследствие сильно полярного строения – классификация на сильные, средние и слабые
Диссоциация по кислотному, основному типу и по типу соли
( уравнения диссоциации)
Объяснение свойств классов неорганических соединений с позиции ТЭД: свойства растворов электролитов - это свойства их ионов
Реакции ионного обмена - механизм, направление
Сравнение реакций ионного обмена с окислительно-восстановительными реакциями
Гидролиз солей - как следствие диссоциации электролитов различной силы.
Разумеется, что среди методов обучения в этой теме важное место занимает химический эксперимент. Он необходим
для демонстрации электропроводности растворов,
для сравнения силы различных электролитов,
для сравнения свойств нейтральных атомов и ионов,
для демонстрации окраски ионов в водных растворах,
для иллюстрации процесса гидролиза,
для обобщения свойств классов неорганических соединений на основе ТЭД.
При этом преобладает демонстрационный эксперимент.
Большое место здесь отводится на проблемное обучение.
Список используемой литературы:
Самоучитель по химии. Е.Н.Френкель изд. «Спутник» - 2012 г.
Все лабораторные работы 6-11 классы (физика, химия, биология). Н.Э.Варава, Н.Р.Парфеня, В.В.Петухов, М.С.Баранов, Л.И.Мицай, О.В.Мешков, А.А.Бутрименко изд. «Феникс» - 2010 г.
Практикум по методике обучения химии в средней школе. П.И.Беспалов, Т.А.Боровских, М.Д.Трухина, Г.М.Чернобельская изд. «Дрофа» - 2007 г.
Обучение химии. Решение интегративных учебных проблем. 8-9 классы. М.А.Шаталов, Н.Е.Кузнецова изд. «Вентана-Граф» - 2006г.
ОВР учебное пособие. Б.В.Румянцев, М.А.Усиченко изд. «Бином» - 2013 г.
Предметная неделя химии в школе. Под общей редакцией К.Н.Задорожного изд. «Феникс» - 2008г.






 редставьте себе, что Вы стоите перед домом, где живут удивительные существа (Ме, НеМе). Каждый житель имеет свою квартиру, живет на определенном этаже и в определенном подъезде. Представители высшего общества занимают элитный 8 подъезд, они держатся особняком, в контакты ни с кем не вступают и очень самодостаточны (Почему?). Все остальные жители очень хотят быть похожими на них. Для этого одни отдают, а другие принимают электроны. В этом случае атомы превращаются в ионы, которые имеют такую же электронную конфигурацию, как ближайшие к ним инертные газы.
редставьте себе, что Вы стоите перед домом, где живут удивительные существа (Ме, НеМе). Каждый житель имеет свою квартиру, живет на определенном этаже и в определенном подъезде. Представители высшего общества занимают элитный 8 подъезд, они держатся особняком, в контакты ни с кем не вступают и очень самодостаточны (Почему?). Все остальные жители очень хотят быть похожими на них. Для этого одни отдают, а другие принимают электроны. В этом случае атомы превращаются в ионы, которые имеют такую же электронную конфигурацию, как ближайшие к ним инертные газы.