Муниципальное казённое общеобразовательное учреждение
«Видимская средняя общеобразовательная школа»
Нижнеилимского района
Иркутской области
III Региональная учебно-практическая конференция детских исследовательских и проектных работ «Эврика!»
Направление: «Элементарно, Ватсон!» (химия, биология)
Тема проектной работы: «Исследование рН кислотности для бытовых веществ»
|
| Выполнил: Ученик 8 класса Титикаев Артур Руководитель проекта: Володенко А. В. |
Видим, 2023 год
Оглавление
| ВВЕДЕНИЕ ………………………………………………………………….. | 3 |
| ТЕОРЕТИЧЕСКАЯ ЧАСТЬ |
|
| Водородный показатель рН ……………………………………………......... | 4 |
| Методы определения водородного показателя раствора ………………….. | 6 |
| Значение рН растворов для живых организмов ………………………......... | 8 |
| ПРАКТИЧЕСКАЯ ЧАСТЬ |
|
| Социологический опрос «рН водных растворов»………………………...... | 10 |
| Определение значения рН кислотности для бытовых веществ …………… | 11 |
| ЗАКЛЮЧЕНИЕ ……………………………………………………………... | 12 |
| Список интернет-источников ……………………………………………...... | 13 |
| Приложение |
|
Введение
Буквы pH можно встретить на баночке с кремом для лица, в результатах медицинских анализов, отчете эколога или инженера-технолога. Меня заинтересовал этот момент на этикетках, и я решил узнать, что это за вездесущий показатель, как его рассчитать и где применять.
Для обоснования актуальности данного вопроса я провёл социологический опрос среди обучающихся 8-11 классов нашей школы. Выяснилось, что 55 % ребят 8-11 классов нашей школы, не знают, что такое рН раствора. При этом 57 % опрошенных полагают, что рН не влияет на организм человека.
На основании проведённого опроса делаю вывод, тема моей проектной работы «Исследование рН кислотности для бытовых веществ» актуальна, потому что вопрос здоровья и долголетия волнует человека всегда.
Перед собой я поставил цель: исследовать рН кислотности для бытовых веществ с помощью цифрового лабораторного оборудования «Архимед» образовательного центра «Точка роста».
Для достижения цели перед собой я поставил задачи:
Изучить литературные источники по данной проблеме;
Провести химический эксперимент с использованием оборудования цифровой лаборатории «Архимед» образовательного центра «Точка роста» на базе нашей школы;
Создать памятку (буклет) «Влияние рН кислотности на организм человека».
Предмет исследования: газированная вода, мыльный раствор, уксус, раствор соли, лимонный сок и раствор пищевой соды.
Объект исследования: водородный показатель рН растворов бытовых веществ.
Научная новизна: применение оборудования цифровой лаборатории «Архимед» образовательного центра «Точка роста».
Практическая значимость: полученные данные можно использовать в качестве материала для классных часов и конференций, посвященных здоровью и долголетию; для проведения предметных недель, для общего просвещения учащихся, возможно, однажды этот вопрос будет интересовать более широкий круг людей.
Теоретическая часть
Водородный показатель рН
Водородный показатель, pH раствора — это мера активности ионов водорода в растворе, и количественно выражающая его кислотность, выраженной в молях на один литр.
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogenI— сила водорода, или pondus hydrogen — вес водорода. Вообще в химии сочетанием pН принято обозначать величину, равную −lg, а буква H в данном случае обозначает концентрацию ионов водорода (H+).
Водные растворы веществ могут быть кислыми, нейтральными или щелочными. Кислотность среды зависит от концентрации положительно заряженных ионов водорода (H+) и отрицательно заряженных гидроксид-ионов (OH−) относительно друг друга.
Если в растворе [H+] [OH−], то его называют кислотным.
Если [OH−] [H+] — щелочным.
Если [H+] = [OH−] — нейтральным.
Название величины указывает лишь на то, что кислотность или щелочность среды можно выразить через концентрацию только ионов водорода. Значения pH могут варьироваться в интервале от 0 до 14. Чем меньше рН, тем выше кислотность среды. И наоборот: чем больше рН, тем выше щелочность среды.
Сильнокислотные свойства раствора характерны для pH = 0–3, а сильнощелочные — для pH = 12–14.
Значения pH в зависимости от характера среды:
В быту нейтральной средой принято считать диапазон pH = 5–8,5. Растворы такой кислотности (или щелочности) безопасны для кожи и слизистых человека. Ниже приведены pH некоторых веществ, которые мы встречаем в повседневной жизни:

Водородный показатель имеет важное значение во многих отраслях:
в косметологии многие продукты проходят проверку на оптимальное значение pH для безопасности кожи;
в сельском хозяйстве кислотность среды определяют для выращивания сельскохозяйственных культур;
в экологии изменение кислотности дождевых вод, рек, озер свидетельствует об ухудшении экологических условий и т. д.
Методы определения водородного показателя раствора
Проанализировав литературные источники с использованием интернет-ресурсов, я узнал, что характер среды (кислый, нейтральный или щелочной) определяют с помощью индикатора. Индикаторы — специальные вещества, которые изменяют окраску раствора при различных значениях pH. Чтобы определить характер среды, в исследуемый раствор достаточно добавить несколько капель водно-спиртового раствора индикатора — и окраска последнего изменится. На практике в лабораторных условиях наиболее распространены несколько индикаторов: метилоранж, лакмус и фенолфталеин. Окраска этих индикаторов в кислой, нейтральной и щелочной среде представлена в таблице:
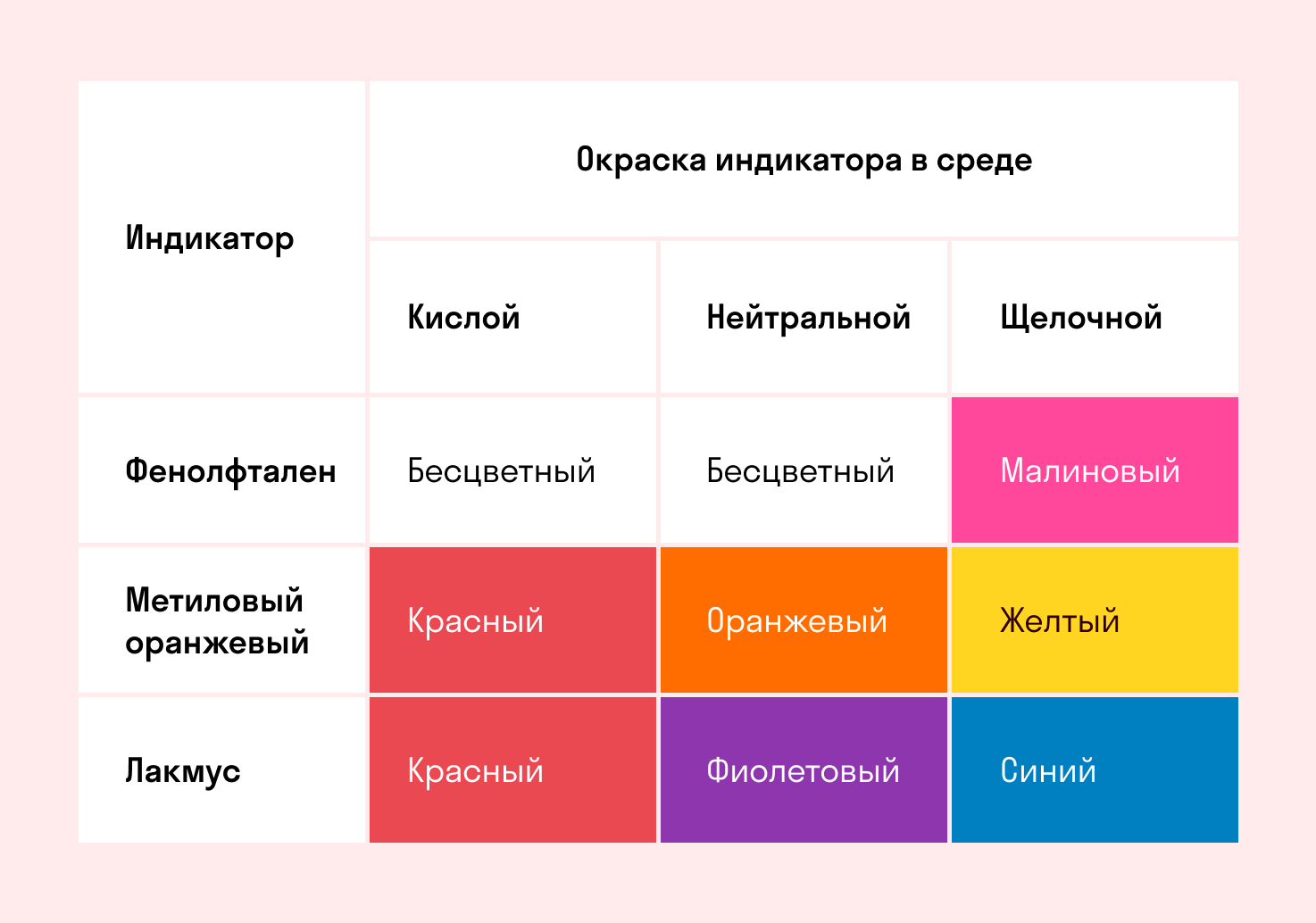
Определение pH среды с помощью индикатора — быстрый и наглядный метод, но для определения более точного значения pH используют универсальный индикатор.
Универсальный индикатор представляет собой смесь высушенных веществ, нанесенных на бумагу. С его помощью можно определить характер среды в широком диапазоне pH — от 1 до 14.
Для измерения водородного показателя pH на бумажную полоску наносят исследуемый раствор, а затем сравнивают цвет индикатора с эталонной шкалой.
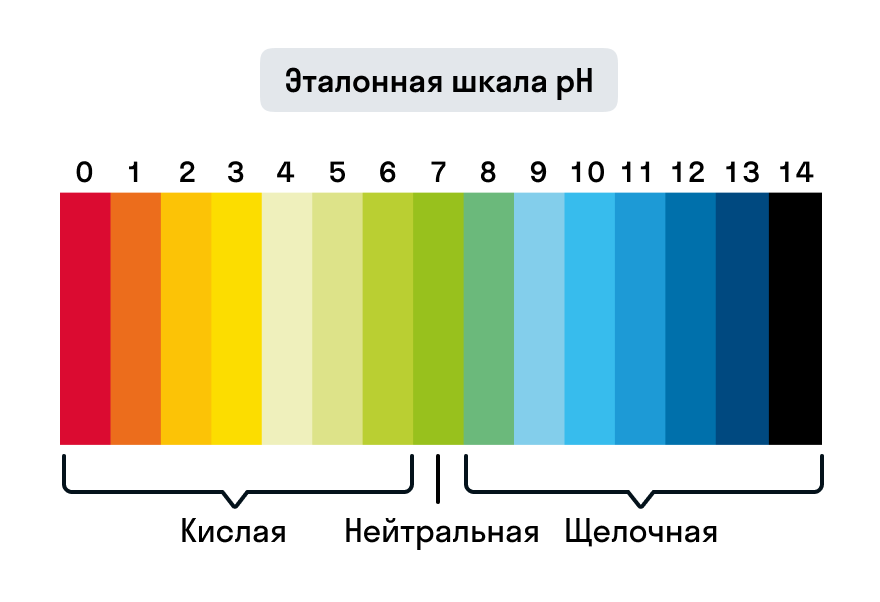
Использование специального прибора pH-метра позволяет измерять значения pH в более широком интервале и с большей точностью (до 0,01 единицы pH) по сравнению с индикаторами. Работа pH-метра основана на измерении электродвижущей силы (ЭДС), которая создается электродами после погружения в раствор.
Также определить количественное значение рН раствора можно с помощью цифрового рН-датчика образовательного центра «Точка роста» на базе нашей школы – это будет наш эксперимент в рамках проектной работы.
Значение pH растворов для живых организмов
Тело человека на 70-80% состоит из воды, и имеет определенное кислотно-щелочное соотношение, характеризуемое показателем pH.
Кислотность жидкостей внутри человеческого организма в норме совпадает с кислотностью крови и находится в пределах от 7,35 до 7,45 pH (нейтральная среда).
Кислотность плазмы артериальной крови человека колеблется в пределах от 7,37 до 7,43 рН, составляя в среднем 7,4 рН (нейтральная среда). Таким образом, я делаю вывод о том, что для живых организмов кислая и щелочная среда недопустима, пагубно будет влиять на их функциональную работу всего организма в целом.
Кислотно-щелочное равновесие в крови человека является одним из самых стабильных параметров, поддерживающее кислые и щелочные компоненты в определенном равновесии в очень узких границах. Даже небольшой сдвиг от указанных пределов может привести к тяжелой патологии.
При сдвиге в кислотную сторону возникает состояние, называемое ацидозом (в организме много органических кислот), в щелочную — алколозом (в организме много оснований). Изменение кислотности крови выше 7,8 рН или ниже 6,8 рН несовместимо с жизнью. К примеру, кислотность эритроцитов составляет 7,28–7,29 рН.
Американские ученые в начале 21 века сделали подлинное открытие, когда выявили, что у любого продукта есть еще один фундаментальный показатель, который имеет критическое значение для нашего здоровья. Это кислотная нагрузка пищи. Она складывается из соотношения в пище компонентов, которые в ходе метаболизма образуют либо кислоту, либо щелочь. Кислотная нагрузка измеряется по принципу кислота минус щелочь. Когда в пище преобладают компоненты, образующие серную кислоту (серосодержащие аминокислоты в белках) или органические кислоты (жиры, углеводы), то кислотная нагрузка имеет положительную величину. Если в пище больше компонентов, образующих щелочь (органические соли магния, кальция, калия), то кислотная нагрузка представляет собой отрицательную величину.
Водородный показатель имеет реальное значение, в связи с тем в процессе эволюции, у большинства живых организмов выработан механизм обеспечения постоянства этого показателя в клетке. Это может влиять на активность ферментов и состояние других белковых молекул.
Кислотно-щелочная среда является главным компонентом гомеостаза. Изменение рН крови всего на 0,3- 0,4 в любую сторону приводит организм к значительному снижению ферментативной активности в заданной среде организма и может закончиться летально. Количество веществ в организме, обладающих кислотными или щелочными свойствами зависит от приема пищи, интенсивности обменных процессов, от способа выделения этих веществ из организма и других факторов.
К физиологическим системам организма относятся легкие, почки, печень, желудочно- кишечный тракт. Механизм действия этих систем заключается в выведении ряда метаболитов, в результате которых происходит нормализация кислотно-щелочной среды в организме.
Практическая часть
Социологический опрос «рН водных растворов»
Мною был проведен опрос среди ребят 8-11 классов. Я опросил 47 человек из 65, что составляет 72% от общего числа опрошенных (Приложение 1).
Ребятам было предложено 2 вопроса:
Знаете ли вы, что такое рH раствора?
Как вы считаете, влияет ли рH раствора на организм человека?
Выяснилось, что 45% ребят нашей школы знают, что такое рH раствора. При этом 57% ребят считают, что рН раствора не влияет на организм человека.
В опрос 1. Знаете ли вы, что такое рH раствора?
опрос 1. Знаете ли вы, что такое рH раствора?
В опрос 2. Как вы считаете, влияет ли рH раствора на организм человека?
опрос 2. Как вы считаете, влияет ли рH раствора на организм человека?
Определение значение рН кислотности для бытовых веществ
Осторожно поместить рН-электрод в первый раствор, подождать, пока значение рН не стабилизируется, записать результат в таблицу;
Тщательно промыть электрод дистиллированной водой, затем повторить опыт для других растворов;
Подготовить таблицу испытанных растворов и записать, какие из них являются основными, а какие – кислотными (Приложение 2).
Результаты испытанных растворов
| Испытуемый раствор | Газированная вода «Тропики», «YASSEY» | Мыльный раствор (Хозяйственное мыло) | Уксус (70%) | Раствор соли (Поваренная соль) | Лимонный сок (Порошок лимонной кислоты) | Раствор пищевой соды (Гидрокарбонат натрия) |
| рН | 3.1 3.2
| 9.3 | 1.1 | 6.9 | 2 | 8.3 |
| Среда раствора | Кислая
| Щелочная | Кислая | Нейтральная | Кислая | Щелочная |
Исследование влияния уксусной кислоты на лист герани
Материалы и оборудование: лист герани, раствор уксусной кислоты (70%), предметное стекло, пинцет, цифровой микроскоп, ноутбук.
На предметной стекло поместили лист герани. Изучили строение листа герани под цифровым микроскопом.
На предметной стекло поместили лист герани и нанесли несколько капель уксусной кислоты. Изучили строение листа герани под цифровым микроскопом (Приложение 3).
Вывод: при действии уксусной кислоты на пластину герани наблюдается изменение окраски листа с зелёного на жёлтый цвет, что свидетельствует о губительном влиянии сильно кислой среды на живые организмы.
Заключение
Проанализировав литературные интернет источники, выяснил, что водородный показатель, pH раствора — это мера активности ионов водорода в растворе, и количественно выражающая его кислотность, выраженной в молях на один литр.
Проведенный социологический опрос показал, что 55 % ребят 8-11 классов нашей школы, не знают, что такое рН раствора. При этом 57 % опрошенных полагают, что рН не влияет на организм человека.
Проведенный химический эксперимент показывает, что у различных веществ рН раствора значительно отличается: от 1.1 до 9.3 (от кислой до щелочной среды).
Кислотно-щелочная среда является главным компонентом всей жизнедеятельности живых организмов. Для живых организмов изменение рН в любую сторону приводит к значительному снижению их жизненных показателей.
Проведенный химический опыт «Действие уксуса на листок герани» показывает, что высокая концентрация ионов водорода ( рН=1.1) губительно влияет на живой организм.
Влияние газировонной воды (рН=3.1-3.2) на организм человека отрицательно сказывается на его здоровье, особенно если имеются проблемы с желудком.
Список литературных источников
Онлайн школа Skysmart: https://skysmart.ru/articles/chemistry/vodorodnyj-pokazatel-ph.
Учебное пособие по химии, 8 класс, О.С.Габриелян: М:-2021 год.
Лабораторные работы по химии. Цифровая лаборатория «Архимед», Москва, 2021 год.
Приложение 1






Приложение 2


Приложение 3


Фотоснимок цифрового микроскопа «Микромед-Эврика»
«Действие уксусной эссенции, 70 %»
Контрольная проба
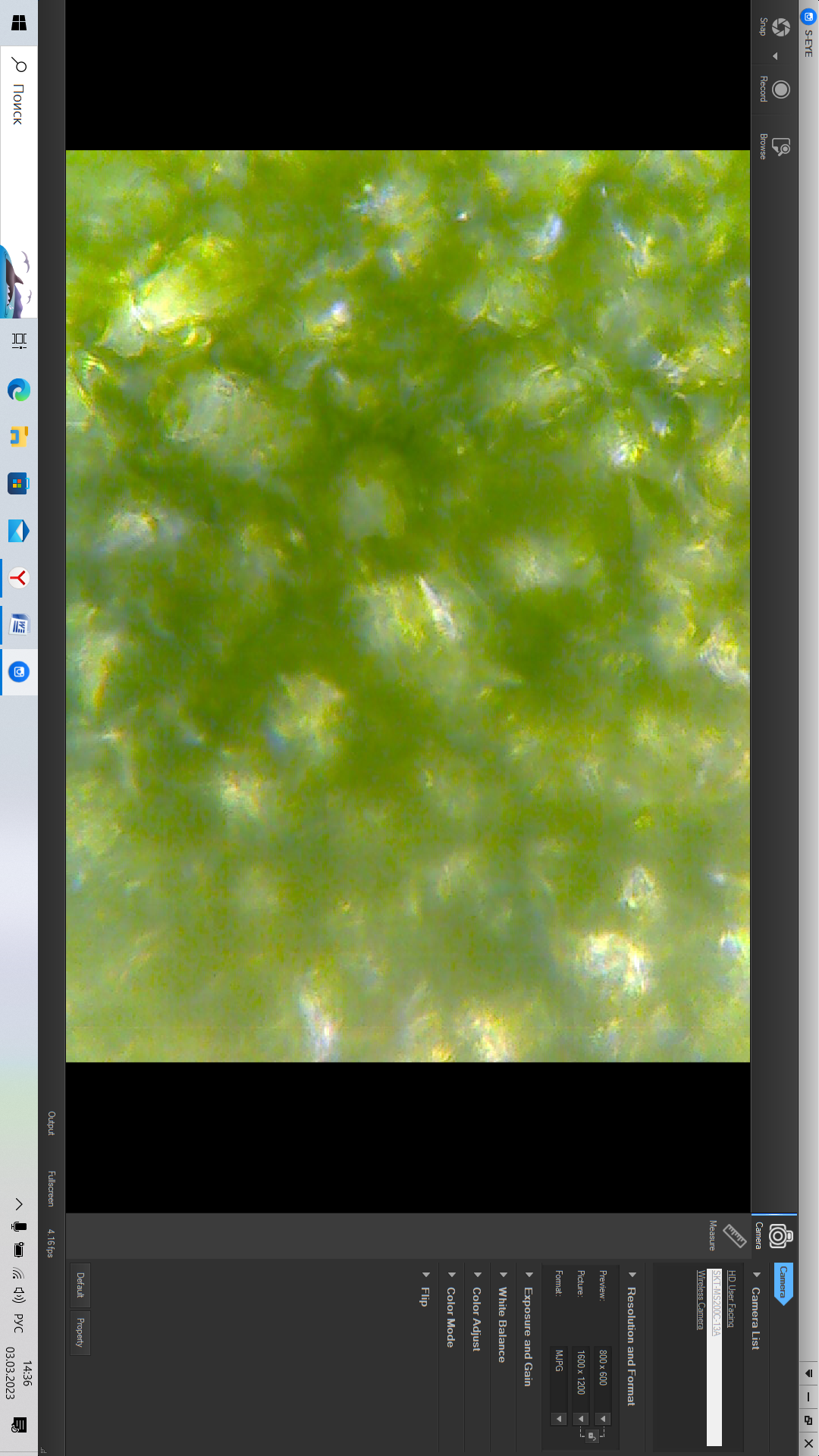
Фотоснимок цифрового микроскопа «Микромед-Эврика»
«Действие уксусной эссенции, 70 %»
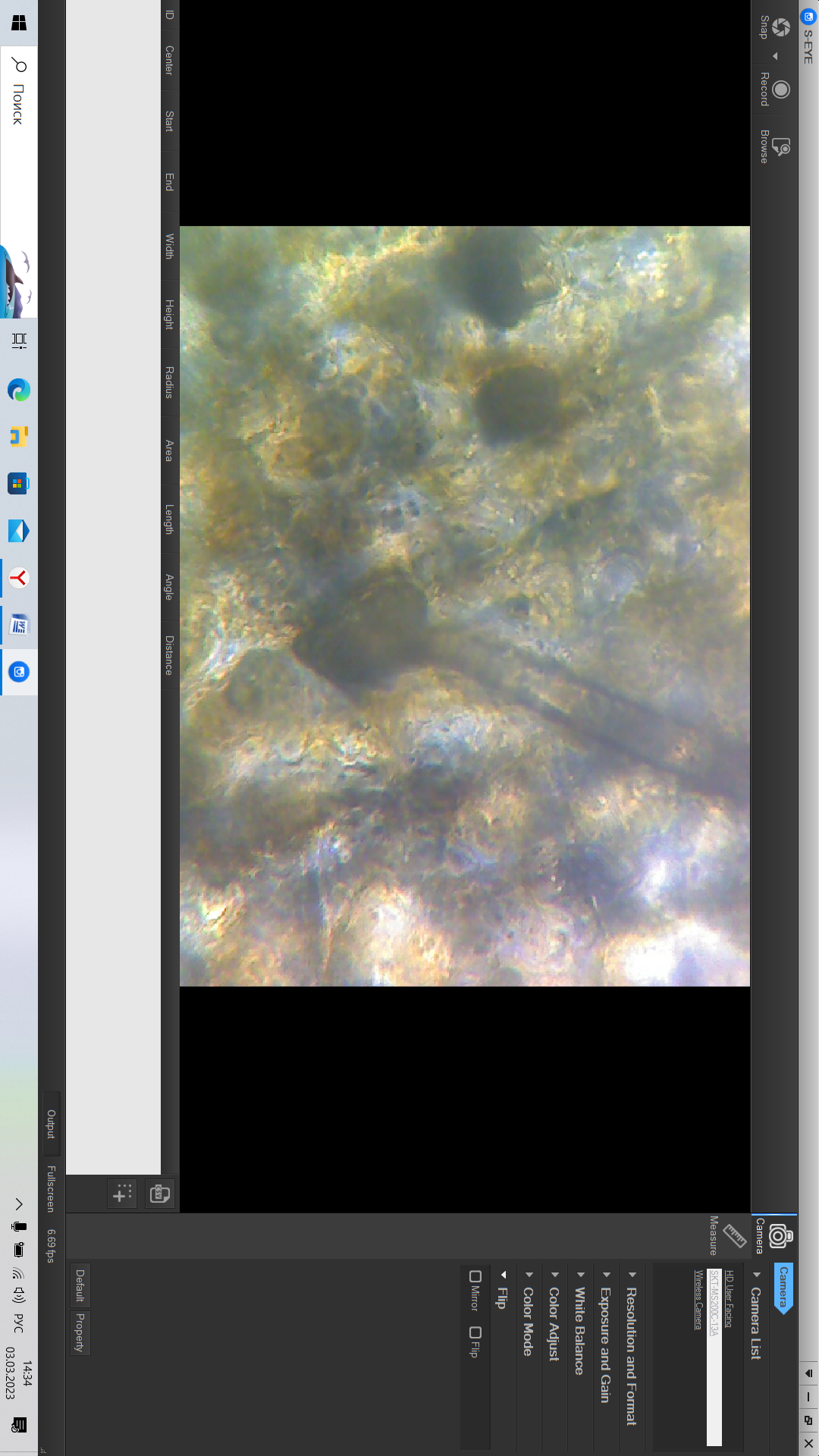
2








 опрос 1. Знаете ли вы, что такое рH раствора?
опрос 1. Знаете ли вы, что такое рH раствора? опрос 2. Как вы считаете, влияет ли рH раствора на организм человека?
опрос 2. Как вы считаете, влияет ли рH раствора на организм человека?




























