Тема урока: Применение метилового и этилового спиртов. Промышленный синтез метанола
Цели урока: Дать представления о промышленных способах получения спиртов, оптимальных
условиях их осуществления. Знать основные области применения спиртов,
вытекающие из их свойств. Уметь записывать уравнения химических реакций,
отражающие способы получения спиртов. Отработать теоретические и практические навыки, закрепить и углубить знания, полученные на предыдущих уроках.
Оборудование и реактивы: примеры органических веществ, которые получают из спирта –
одеколон, лаки, красители, уксусная кислота и пр., таблица «Производство
этилового спирта»
Ход урока
I. Организационный момент. Актуализация темы.
Учет знаний, умений, навыков
Фронтальный опрос
Какие вещества относят к кислородсодержащими?
Какие вещества называют спиртами?
Какова общая формула спиртов?
Какие виды изомерии характерны для спиртов?
Какие физические свойства характерны для спиртов?
Какие типы химических реакций характерны для спиртов?
Решение задач
I. Какой объем водорода (н.у.) можно получить при взаимодействии 160 г метанола с 140г металлического натрия?
160г 140г Х л
2СН3ОН + 2Na 2СН3 ОNa +Н2
2х32=64 2х23=46 22,4л
ν (СН3ОН) = 160 =2,5 г/Моль
64
ν (Na) = 140 = 3г/Моль
46
V (Н2) = 2,5х 22,4= 56 л.
Ответ: V (Н2) = 56 л.
II. Напишите структурные формулы всех изомеров спирта С5Н11ОН и дайте им названия по систематической номенклатуре
Составу С5Н11ОН соответствует 8 изомеров, которые можно вывести из изомеров состава С5Н12 (3-метилбутанол-1, 3-метилбутанол-2, 2-метилбутанол-2, 2-метилбутанол -1, 2,2-диметил пропанол-1)
III. Из этилена массой 32г было получено спирта массой 44г. Вычислите практический выход продукта от теоретически возможного.
32г 44г Х%
С2Н4 С2Н5 ОН + Н2О
28г 46г
1) 32г — Хг Х= 52,57г (теор)
28г 46г
2) 52,57г — 100% Х= 83,69%
44г Х%
Ответ: 83,69% практический выход
IV. При сжигании метилового спирта массой 4г выделилось 90,83 кДж теплоты. Составьте термохимическое уравнение этой реакции.
4г
2СН3ОН + 2О2 СО2+ 2Н2О+ 90,83кДж
2х32г Х кДж
Х= 64 х 90,83 / 4 = 1453,28 кДж
Ответ: 1453,28 кДж выделится теплоты при сгорании метанола массой 4г.
III.Объяснение нового материала
Из предельных одноатомных спиртов наибольшее значение имеют метанол и этанол. В природе спирты в чистом виде встречаются редко, в основном в виде производных (сложные эфиры).
В производстве метанола и синтетического этанола много общего, так как реакции протекают с газообразными веществами. Раньше метанол получали из продуктов пиролиза древесины, поэтому сохранилось его старое название – древесный спирт. Метанол получают из синтез-газа
СО+2 Н2 СН3ОН+Q
Синтез-газ сжимают процессором, смешивают с непрореагировавшим газом и направляют в теплообменник, где газовая смесь нагревается до необходимой температуры. Далее смесь направляется в колонну синтеза, где осуществляется целевой процесс. Выходящие продукты реакции поступают в теплообменник, где они нагревают газовую смесь, идущую на синтез, затем проходят через холодильник-конденсатор и поступают далее в сепаратор. Здесь спирт отделяется от непрореагировавших газов (очистка спирта), которые циркуляционным компрессором возвращаются в технологический процесс. А спирт поступает в специальный сборник спирта.
При синтезе метилового спирта протекают побочные реакции – возможно образование многих побочных продуктов – спиртов с большей молекулярной массой, диметилового и других эфиров, углеводородов и т.п. это предъявляет особо высокие требования к подбору катализаторов. Здесь необходимы так называемые селективные катализаторы, которые ускоряли бы целевую реакцию и подавляли другие возможные процессы. Такими свойствами и обладают оксида цинка, хрома, меди.
Схема промышленного получения метанола
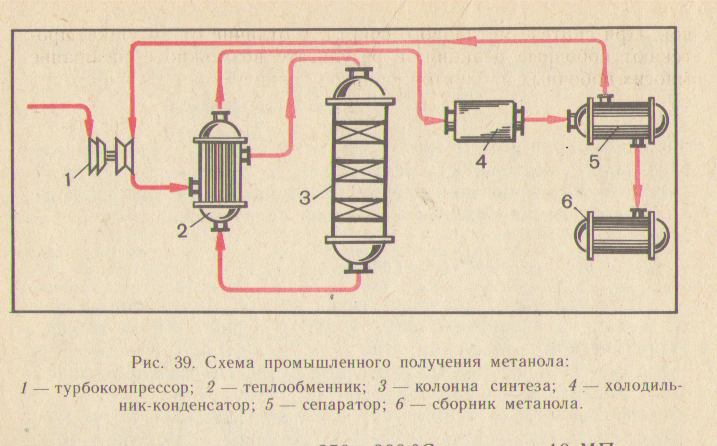
Вам известно, что спирты следует рассматривать как продукты частичного окисления предельных углеводородов. Казалось бы, их можно получить таким способом в промышленности, но задача оказалась весьма трудной и пока не решенной. Более доступен другой способ превращения предельного углеводорода в спирт – через галогенпроизводные.
Например, метанол можно получить путем следующих превращений
СН4СН3ClСН3ОН
Вначале проводят хлорирование или бромирование, затем полученное галогенпроизводное подвергают гидролизу
СН4 + Cl 2 — СН3Cl + НCl
СН3Cl + Н2О СН3ОН + НCl
Реакцию проводят в присутствии щелочи, которая нейтрализует хлороводород, поэтому химическое равновесие смещается в сторону прямой реакции.
Этот способ используют и в лабораториях. Он не имеет промышленного значения, т.к. дорог и сопровождается побочными реакциями.
Способы получения этилового спирта:
Основной промышленный способ получения этанола, он же наиболее экономичный, это гидратация этилена, который извлекают из газов нефтепродуктов. При этом получают синтетический спирт.
Брожение пищевого сырья (зерновые культуры, картофель, отходы сахарного производства). Такой спирт называют пищевым или винным спиртом.
Гидролиз древесины, с последующим сбраживанием. Полученный спирт называют гидролизным
Этиловый спирт получают двумя способами: биохимическим (брожение) и химическим (синтез).
Рассмотрим эти процессы
1. Большие количества этилового спирта получают синтетическим путем. Сырьем для этого служит этилен и пары воды. Реакция между веществами обратимая и экзотермическая
С2Н4 + 2Н2О С2Н5 ОН + 46кДж
Оптимальные условия протекания реакции: наличие катализатора (фосфорная кислота), повышенное давление (7-8 МПа), температура около 300°С.
2. Наиболее древний метод получения этанола – сбраживание сахаристых веществ, содержащих глюкозу.
Процесс брожения давно известен людям. Виноградный сок (содержит глюкозу) подвергается брожению, и получается спирт, который отгоняют из смеси. Для производства спирта используют более дешевые источники сахаристых веществ – крахмал и клетчатку (целлюлозу). Вначале их превращают в сахаристое вещество, которое потом подвергают брожению. Под действием ферментов (биологических катализаторов, вырабатываемых дрожжами) происходит спиртовое брожение.
Химизм этих процессов:
(С6Н10О5)n———— С12Н22О11—— С6Н12О6———2С2Н5 ОН +2СО2 ↑
крахмал сахароза глюкоза этанол
В конечном виде уравнение выглядит так:
дрожжи
С6Н12О6 —— 2С2Н5 ОН +2СО2 ↑
Сортировка сырья
Разваривание
Осахаривание
Брожение
Перегонка бражки
Ректификация
Позднее стали получать этанол из крахмалсодержащих продуктов.
3. Получение спирта из крахмала требует расхода пищевого сырья, поэтому широко развито получение спирта из древесины (клетчатки). Такой спирт называют пищевым или винным.
СПРАВКА
Из 1т сухих опилок можно получить 200 л спирта. Такое же количество спирта получают из 0,7 т зерна или 1,5 т картофеля.
Применение
Этанол применяют в разных отраслях народного хозяйства. В больших количествах его используют при производстве синтетических каучуков. Он является также растворителем и исходным материалам для производства лаков, медикаментов и душистых веществ. Из него получают уксусную кислоту, диэтиловый эфир, различные сложные эфиры, красители и другие вещества.
Этанол в медицине применяют как дезинфицирующее средство. Из этанола изготавливают также алкогольные напитки. Но следует учесть, что этанол – ядовитое, наркотическое вещество.
Метанол главным образом используется для производства формальдегида, используемого в производстве пластмасс, уксусной кислоты; некоторых лекарственных веществ. Его применяют также в качестве растворителя лаков и красок.
Перспективным считается использование метилового спирта в качестве моторного топлива, так кА добавка его к бензину повышает октановое число горючей смеси и снижает образование вредных веществ в выхлопных газах.
Пентиловые спирты идут на производство сложных эфиров, необходимых в парфюмерии. Изопентиловый спирт – реагент для определения жирности молочных продуктов.
Высшие спирты применяются во многих отраслях народного хозяйства, например:
С14-С20 – ускорители вулканизации
С18-С20 – медицинские препараты
С12-С20-парфюмерно-косметическая продукция
С16-С20 – антикоррозионные смазки
Основные продукты, получаемые из этанола, и их применение
IV Рефлексия
V. Закрепление
Назовите основные способы получения спиртов
Почему при получении метанола используют селективные катализаторы и что это такое?
Какой спирт называют древесным спиртом и почему?
Какой максимальный объем водорода (н.у) может быть вытеснен натрием из 230г этилового спирта?
230г Хл
2С2Н5ОН + 2Na 2С2Н5О Na +Н2
2х 46=92г 22,4 л
Х= 230 х 22,4 /92 = 52 л Ответ: 52л



















