ГАПОУ ЛО «Сосновоборский политехнический колледж»
Г. Сосновый Бор Ленинградской области
Исследовательская работа по Экологии
«Влияния факторов среды
на рост и развитие растений»
Студентки 101 к группы
Писпонен Ксении
Руководители:
учитель химии экологии Белобородова М.В.
2018 г.
Введение.
В настоящее время в связи с интенсивным воздействием человека на природу резко повысился интерес общества к состоянию окружающей среды, её воздушного бассейна, почвы, а также продуктов питания.
Контроль состояния окружающей среды, оценка её качества – это важнейшая составная часть деятельности человека, которая направлена на освоение и использование природных ресурсов для обеспечения своей жизнедеятельности.
В современное время для полной картины экологической ситуации в конкретной местности необходимо использовать данные биомониторинга и проводить биоиндикационные исследования.
Один из методов оценки качества урбанизированной среды - оценка состояния окружающей среды по растениям. Растения в процессе роста и развития испытывают влияние различных экологических факторов
В данной работе исследуется влияние состава почвы на рост и развитие древесных культур города Сосновый Бор.
Исследовалось влияние факторов, в том числе и состава почв, на дубы, произрастающие в городской черте и за городом.
Дубы занимают первое место в полезащитном лесоразведении; превосходят многие породы по оздоровительному влиянию на окружающую среду (интенсивно выделяют кислород). Дубы, особенно старые деревья, отличаются высокими эстетическими качествами и издавна используются при создании парков, в аллейных посадках.
Проанализирован состав почв с липовой аллеи по улице Солнечной.
На разных площадках взяты пробы для определения состава почв.
Цель работы: изучение влияния состава почв, как одного из факторов среды, на рост и развитие древесных культур города Сосновый Бор.
Задачи:
Изучить имеющуюся литературу по данному вопросу.
2. Изучить влияние катионов и анионов, содержащихся в почве, на рост и развитие растений.
3. Провести практические работы с использованием методов:
-весовой метод Л.В Дорогань;
-исследовательский метод химического состава почвы по книге Н.Я Логинова.
4. Проанализировать полученные данные, сделать выводы.
Работа проводилась с период с мая 2017 г. по сентябрь 2018 г.
I.Состав почвы.
1. Катионы в почве, вред или польза?
Содержание в почве катионов и их состав, оказывают большое влияние на почвообразовательный процесс и многие важные в агрономическом отношении свойства почвы. Наличие в почве коллоидных и предколлоидпых частиц - обязательное условие создания почвенной структуры. Почвы, не содержащие эти частицы или бедные ими, бесструктурны. Коллоиды и близкие к ним по размеру частицы служат тем клеющим началом, которое необходимо для создания агрономически ценной структуры. Клеящая способность коллоидных и предколлоидных частиц зависит от их природы, состава обменных катионов, реакции среды. От структуры почвы зависят водно-воздушные и механические свойства, определяющие ее плодородие.
Большое значение имеет состав обменных катионов для питания растений. В почвах, не содержащих растворимых солей и карбонатов кальция, обменный кальций - единственный источник известкового питания растений. Обменный калий и аммоний также служат одной из наиболее доступных для растений форм соединений. При внесении водорастворимых фосфорных удобрений — суперфосфата, содержащего фосфор в виде монокальцийфосфата Са(H2PO4)2, аммофоса NH4H2PO4 и др.- в почвах происходит интенсивное химическое связывание фосфора. В кислых почвах (в подзолистых и красноземах), содержащих много полуторных окислов, химическое поглощение фосфора идет с образованием труднорастворимых фосфатов железа и алюминия. В почвах, насыщенных основаниями и содержащих бикарбонат кальция в почвенном растворе (черноземы, сероземы), химическое связывание фосфора происходит в результате образования слаборастворимых фосфатов кальция. Способность органических и минеральных коллоидных частиц к обменному поглощению катионов обусловлена тем, что большая часть их имеет отрицательные заряды. В естественном состоянии почвы всегда содержат определенное количество поглощенных катионов (Са 2+ , Mg2+ , Н + , А13+ , Na+ , K+ , NH4+ и др.). Эти катионы могут обмениваться на другие катионы, находящиеся в растворе. Обмен катионами между раствором и почвенным поглощающим комплексом происходит в строго эквивалентных количествах. Реакция обмена катионов протекает быстро. При внесении в почву легкорастворимых удобрений (КСl, NH4Cl, NH4N03 и др.) они сразу же вступают во взаимодействие с ППК, катионы их поглощаются в обмен на катионы, ранее находившиеся в поглощенном состоянии. Реакция обмена катионов обратима, так как поглощенный почвой катион может быть снова вытеснен в раствор: (ППК)Са + 2KCl (ППК) KK + СаСl2; ППК)Са + NH4N03 (ППК) NH4 NH4 В зависимости от концентрации раствора, его объема и природы обменивающихся катионов между катионами раствора и катионами почвенного поглощающего комплекса устанавливается некоторое подвижное равновесие. При изменении состава почвенного раствора это равновесие смещается, в результате одни катионы переходят из раствора в поглощенное состояние, а другие — из поглощенного состояния в почвенный раствор. При внесении минеральных удобрений, например KCl, концентрация почвенного раствора повышается, катионы удобрения вступают в обменную реакцию с катионами почвенного поглощающего комплекса и поглощаются почвой. При усвоении какого-либо катиона растениями концентрация его в растворе уменьшается, он переходит из поглощенного состояния в раствор в обмен па другие катионы, содержащиеся в почвенном растворе. Чем выше степень насыщенности поглощающего комплекса данным катионом, тем легче и быстрее он вытесняется в раствор. Количество катионов, вытесняемых из поглощенного состояния в раствор, возрастает с повышением концентрации раствора, а при одинаковой концентрации — с увеличением объема раствора вытесняющей соли. Разные катионы обладают неодинаковой способностью к поглощению. Чем больше заряд (валентность) катиона и его атомная масса, тем сильнее он поглощается и труднее вытесняется из поглощенного состояния другими катионами. Исключение из этого правила составляют ионы Н + , которые имеют наименьшую атомную массу, но обладают высокой энергией поглощения и способностью вытеснять другие катионы из ППК. Вся совокупность органических и минеральных коллоидных частиц почвы (представленных гумусовыми веществами, глинистыми минералами и гидроксидами железа и алюминия), участвующих в обменном поглощении катионов, была названа К. К- Гедройцем почвенным поглощающим комплексом (ППК). В большинстве почв в составе поглощенных катионов преобладает Са2+, второе место занимает Mg2+ и в значительно меньших количествах находятся К+ и NH4+. Сумма Са2+и Mg2+ обычно составляет около 90% общего количества обменно-поглощенных катионов. В кислых почвах (подзолистых и красноземах) среди поглощенных катионов значительную часть занимают Н+ и А13+ , а в солонцовых почвах — Na+ Состав поглощенных катионов оказывает большое влияние па свойства почвы и условия роста растений. Кальций коагулирует органические и минеральные коллоиды. Поэтому преобладание в составе поглощенных катионов Са2+, например на черноземах, способствует поддержанию прочной структуры и обусловливает хорошие физические свойства почвы. Насыщение почвы натрием (у солонцовых почв) вызывает пептизацию коллоидов, что приводит к их вымыванию, разрушению структурных агрегатов и ухудшению физических свойств почвы (плотное сложение, вязкость и т. д.). Кроме того, при наличии натрия в почвенном поглощающем комплексе происходит вытеснение его в раствор в обмен на другие катионы с образованием соды, что вызывает щелочную реакцию раствора, неблагоприятную для развития растений: (ППК) Na Na + Са(HСO3)2 - (ППК) Са + 2 Na HC O3 При большом содержании в почвенном поглощающем комплексе ионов водорода и алюминия они могут переходить в раствор и подкислять его. Повышенная кислотность раствора и особенно высокое содержание в нем алюминия оказывают вредное действие на растения. [5]
Предостережение. При внесении большого количества одного катиона, другие могут быть вытеснены в почвенный раствор, и вымыты в глубокие слои почвы. Такое может происходить при внесении большого количества несбалансированного минерального удобрения. Особенно это опасно на легких песчаных почвах, где мало мельчайших (коллоидных) частиц, поэтому дозы минеральных удобрений там снижают, разбивают на несколько внесений.
2. Анионы в почве. Вред или польза?
Степень поглощения анионов почвой зависит от природы аниона, состава коллоидов и реакции среды. При химическом поглощении анионы фосфорной кислоты взаимодействуют с кальцием, алюминием и железом. Образующиеся нерастворимые фосфаты кальция, алюминия и железа накапливаются в почве в виде осадков. Физико-химическое поглощение аниона происходит при взаимодействии его с диффузным слоем полуторных оксидов и потенциалопределяющим слоем отрицательно заряженных коллоидов. При этом повышается емкость обмена и усиливается поглощение катионов. В кислой среде активность полуторных оксидов повышается, поэтому усиливается поглощение аниона фосфорной кислоты. Поглощение фосфат-иона почвами имеет отрицательное и положительное значения. С одной стороны, анион поглощенный обменным путем, со временем теряет активность к обмену, а образовавшиеся при химическом поглощении труднорастворимые осадки также малодоступны для растений. С другой стороны, фосфатный ион при всех видах поглощения извлекается из большого геологического круговорота и удерживается в почве. Для более эффективного использования фосфорных удобрений их вносят в почву в гранулированном виде, в результате чего анион фосфорной кислоты может потребляться корнями растений более длительный период. Порошковые формы фосфорных удобрений быстро переходят в недоступные для растений соединения.[6]
В 1860 г. Сакс и Кноп, выращивая растения в сосудах на водном растворе минеральных солей, установили, что для жизнедеятельности растения, кроме С, О, Н, небходимы следующие 7 элементов: N, P, S (неметаллы), К, Са, Mg, Fe (металлы). В начале XX в. при современных методах очистки воды и реактивов была показана необходимость для растений, кроме перечисленных выше, еще шести элементов: бора, марганца, цинка, меди, молибдена и хлора. Предполагают, что для нормального роста некоторых растений необходимы и такие элементы, как кобальт, натрий и др. Все необходимые элементы корневого питания подчиняются основным правилам, сформулированным еще Ю. Либихом: 1) все перечисленные элементы равнозначны и полное исключение любого из них приводит растение к глубокому страданию и гибели; 2) ни один из перечисленных элементов не может быть заменен другим, даже близким по химическим свойствам, т. е. каждый элемент имеет свое специфическое физиологическое значение. Все необходимые для жизни растений элементы в зависимости от их количественного содержания в растении принято разделять на макроэлементы (содержание более 0,01%) - к ним относятся N, Р, S, К, Са, Mg, Fe и микроэлементы (содержание менее 0,01%) —к ним относятся Мn, Си, Zn, В, Mo, C1.[5,6]
3. Физиологическая роль минерального питания
В растительном организме все процессы тесно взаимосвязаны. Исключение из питательной среды какого-либо необходимого элемента быстро вызывает изменение во многих, если не во всех, процессах метаболизма. В связи с этим выделить первичный эффект бывает чрезвычайно трудно. Сказанное относится в первую очередь к тем питательным элементам, которые не входят в состав определенных органических веществ, а играют скорее регуляторную или какую-то иную роль. В общем виде можно сказать, что питательные элементы имеют следующее значение: 1) входят в состав биологически важных органических веществ; 2) участвуют в создании определенной ионной концентрации, стабилизации макромолекул и коллоидных частиц (электрохимическая роль); 3) участвуют в каталитических реакциях, входя в состав или активируя отдельные ферменты.
Во многих случаях один и тот же элемент может играть разную роль. Некоторые элементы выполняют все три функции.
Макроэлементы.
Фосфор. Содержание фосфора в растениях составляет около 0,2% на сухую массу. Фосфор поступает в корневую систему растений в виде окисленных соединений, главным образом остатка ортофосфорной кислоты (Н2РО4, НРО42-, РО43-). Физиологическое значение фосфора определяется тем, что он входит в состав ряда органических соединений, таких, как нуклеиновые кислоты (ДНК и РНК), нуклеотиды, фосфолипиды, витамины и многие другие, играющие центральную роль в обмене веществ. Многие фосфорсодержащие витамины и их производные являются коферментами и принимают непосредственное участие в каталитическом акте, ускоряющем течение важнейших процессов обмена (фотосинтез, дыхание и др.). При всех превращениях в растительном организме фосфор сохраняет степень окисленности. Собственно, все превращения сводятся лишь к присоединению или переносу остатка фосфорной кислоты (фосфорилирование и трансфосфорилирование). Фосфорилирование — это присоединение остатка фосфорной кислоты к какому-либо органическому соединению с образованием эфирной связи, например взаимодействие фосфорной кислоты с карбонильной, карбоксильной или спиртовой группировками. Трансфосфорилирование - это процесс, при котором остаток фосфорной кислоты, включенный в состав одного органического вещества, переносится на другое органическое вещество. Ряд важнейших в биологическом отношении фосфорных соединений содержит несколько остатков фосфорной кислоты. Для фосфора характерна способность к образованию связей с высоким энергетическим потенциалом (макроэргические связи). Такие связи нестабильны, это облегчает их обмен и позволяет использовать энергию на самые различные биохимические и физиологические процессы. Недостаток фосфора влияет практически на все процессы жизнедеятельности растений. Фотосинтез, дыхание, рост требуют для нормального протекания достаточного снабжения фосфором
Сера содержится в растениях в количестве 0,17%. Однако в растениях семейства крестоцветных ее содержание гораздо выше. Поступает сера в растения в виде сульфат-иона SO42-. Сера входит в состав органических соединений, играющих важную роль в обмене веществ организма. Так, сера входит в состав трех аминокислот - цистина, цистеина и метионина. Почти все белки содержат серусодержащие аминокислоты, поэтому становится ясной роль серы в белковом обмене организма. Сера входит также в состав многих витаминов и многих коферментов, таких, как биотин, тиамин, коэнзим А, глютатион, липоевая кислота и др. В связи с этим сера принимает участие в многочисленных реакциях обмена (аэробная фаза дыхания, синтез жиров и др.). Сульфгидрильные группировки (SH) и дисульфидные связи (S—S) играют большую роль, обеспечивая взаимодействие между ферментами и их простетическими группами, а также участвуя в создании определенной конфигурации белковых молекул. Так, 5Н группы связывают белок с такими коферментами, как НАД или ФАД. Часто за счет дисульфидных связей сохраняется трехмер ная структура белка, а следовательно, его активность. Сера входит в состав чесночных и горчичных масел. Именно с этим связан своеобразный вкус и запах ряда крестоцветных. Нельзя не отметить, что соединения серы, такие, как S-аденозилметионин, участвуют в образовании полиаминов, в частности спермедина. Согласно современным представлениям, полиамины играют большую и разностороннюю роль в жизнедеятельности организмов. Они оказывают влияние на структуру нуклеиновых кислот и рибосом, регулируют процессы деления клеток. Полиамины благодаря наличию заряженных аминогрупп во многих реакциях могут в известной мере заменять неорганические катионы.
Кальций входит в состав растений в количестве 0,2%. В старых листьях его содержание доходит до 1 %. Поступает в виде иона Са2+. Роль кальция разнообразна. Кальций, соединяясь с пектиновыми веществами, дает пектаты кальция, которые являются важнейшей составной частью клеточных оболочек растений. Срединные пластинки, склеивающие клеточные оболочки соседних клеток, состоят по преимуществу из пектатов кальция. При недостатке кальция клеточные оболочки ослизняются, что особенно ярко проявляется на клетках корня. Кальций плохо передвигается по растению, поэтому для предупреждения ослизнения необходимо, чтобы ионы Са2+ непосредственно соприкасались с клетками корня. Сказанное было продемонстрировано в опытах, поставленных по методу изолированных водных культур. В этих опытах одну прядь корней помещали в питательный раствор, содержащий все необходимые питательные вещества; другую прядь корня того же растения — в раствор с исключением кальция. Очень скоро клетки корня, которые находились в растворе без кальция, начали ослизнятьcя и загнивать.Кальций повышает вязкость цитоплазмы, что видно на опытах с формами плазмолиза. В солях кальция плазмолиз имеет вогнутую форму, так как более вязкая цитоплазма с трудом отстает от клеточных оболочек. Присутствие кальция важно для нормального функционирования мембран. Кальций принимает участие в поддержании структуры хромосом, являясь связующим звеном между ДНК и белком. При недостатке кальция наблюдаются повреждения хромосом и нарушение митотического цикла. Кальций необходим также для поддержания структуры митохондрий и рибосом. Большое значение имеет связывание Са2+ с белком кальмодулином. Этот процесс регулирует внутриклеточную концентрацию Са2+. Кальций является активатором таких ферментов, как фосфорилаза, аденозинтрифосфатаза. Комплекс Са2+ с белком активирует протеинкиназы, катализирующие процессы фосфорилирования белков. Кальций реагирует с различными органическими кислотами, давая соли, и тем самым является в определенной мере регулятором рН клеточного сока. Магний. Содержание магния в растениях составляет в среднем 0,17 %. Магний поступает в растение в виде иона Mg2+. Магний входит в состав основного пигмента зеленых листьев — хлорофилла. Магний поддерживает структуру рибосом, связывая РНК и белок. Большая и малая субъединицы рибосом ассоциируют вместе лишь в присутствии магния. Отсюда синтез белка не идет при недостатке магния, а тем более в его отсутствие. Магний является активатором многих ферментов. Важной особенностью магния является то, что он связывает фермент с субстратом по типу хелатной связи (клешневидная связь между органическим веществом и катионом). Так, например, присоединяясь к пирофосфатной группе, магний связывает АТФ с соответствующими ферментами. В связи с этим все реакции, включающие перенос фосфатной группы (большинство реакций синтеза, а также многие реакции энергетического обмена), требуют присутствия магния. Магний активирует такие ферменты, как ДНК- и РНК-полимеразы, аденозинтрифосфатазу, глютаматсинтетазу, а также ферменты, катализирующие перенос карбоксильной группы, — реакция карбоксилирования и декарбоксилирования.
Калий. Содержание калия в растении в среднем составляет 0,9 %. Он поступает в растение в виде иона К+. Физиологическую роль калия нельзя считать полностью выясненной. Калий не входит ни в одно органическое соединение. Большая часть его (70 %) в клетке находится в свободной ионной форме и легко извлекается холодной водой, остальные 30% в адсорбированном состоянии. В противоположность кальцию калий снижает вязкость протоплазмы, повышает ее оводненность. Эта особенность действия калия хорошо проявляется в том, что в его солях плазмолиз имеет выпуклую форму, протоплазма легко отстает от клеточной оболочки. Следовательно, калий является антагонистом кальция. Калий активирует работу многих ферментных систем, например фермент, катализирующий фосфорилирование сахаров,— гексокиназу, ферменты, катализирующие перенос фосфорной кислоты с пирувата на АДФ (пируваткиназа), а также ферменты, участвующие в образовании АТФ в процессе окислительного фосфорилирования. В связи с этим, по данным Э.И. Выскребенцевой, при недостатке калия резко падает содержание макроэргических фосфатов. Калий активирует и ряд ферментов цикла Кребса. Многие ферменты, участвующие в синтезе белка, требуют для своего действия присутствия калия. Несмотря на необходимость калия для проявления активности ряда ферментов, механизм этой активации до настоящего времени не представляется ясным. Недостаток калия замедляет транспорт сахарозы по флоэме. Влияние калия на передвижение органических веществ, по гипотезе Спаннера, проявляется благодаря образованию градиента электрического потенциала на ситовидных пластинках, который возникает при циркуляции калия между ситовидной трубкой и сопровождающими клетками. Соли калия растворимы и участвуют в регуляции осмотического потенциала клетки. В частности, большое значение имеет К+ в регуляции работы устьиц. Показано, что открытие устьиц на свету связано с накоплением в замыкающих клетках ионов калия. При этом К+ в обмен на Н+ поступает из клеток, окружающих устьичные.
Железо входит в состав растения в количестве 0,08%. Необходимость железа была показана в тот же период, что и остальных макроэлементов. Поэтому, несмотря на ничтожное содержание, его роль рассматривается вместе с макроэлементами. Железо поступает в растение в виде Fe3+. Роль железа в большинстве случаев связана с его способностью переходить из окисленной формы (Fe3+) в восстановленную (Fe2+) и обратно. Железо входит в состав каталитических центров многих окислительно-восстановительных ферментов. В виде геминовой группировки оно входит в состав таких ферментов, как цитохромы, цитохромоксидаза, каталаза и пероксидаза. Цитохромная система является необходимым компонентом дыхательной и фотосинтетической электронно-транспортной цепи. В силу этого при недостатке железа тормозятся оба этих важнейших процесса. Кроме того, целый ряд ферментов содержит железо в негеминовой форме. К таким ферментам относятся некоторые флавопротеиды, железосодержащий белок ферредоксин. Железо необходимо для образования хлорофилла. При этом железо катализирует образование предшественников хлорофилла аминолевулиновой кислоты и протопорфиринов. Предполагают, что железо играет роль в образовании белков хлоропластов. При недостатке железа нет условий для образования таких важнейших компонентов хлоропластов, как цитохромы, ферредоксин и некоторые другие. Возможно, это косвенно влияет на образование хлорофилла.
Микроэлементы
Практическая значимость исследований по микроэлементам связана с тем, что есть почвенные провинции, где остро недостает того или иного из них. Кроме того, часто в почве микроэлементы находятся в неусвояемом для растительного организма состоянии, поэтому внесение микроудобрений (удобрений, содержащих микроэлементы) в почву очень полезно. Однако надо учитывать, что высокие дозы микроэлементов могут оказать ядовитое влияние. Выяснилось, что микроэлементы в подавляющем большинстве активируют определенные каталитические — ферментативные системы. Это осуществляется различными путями — непосредственным участием в составе молекул ферментов или их активацией. Важным моментом в действии всех микроэлементов является их способность давать комплексные соединения с различными органическими соединениями, в том числе и с белками. Разные микроэлементы могут давать комплексные соединения с одними и теми же органическими веществами, благодаря чему они могут выступать как антагонисты. Отсюда понятно, что для нормального роста растений необходимо определенное соотношение микроэлементов (железа к марганцу, меди к бору).
Марганец поступает в растение в виде ионов Мп2+. Среднее содержание марганца в растениях 0,001%. Марганец активирует ферменты, катализирующие реакции цикла Кребса (дегидрогеназы яблочной кислоты, лимонной кислоты, декарбоксилазу щавелевоуксусной кислоты и др.). В связи с этим понятно большое значение марганца для процесса дыхания, особенно его аэробной фазы. Правда, имеются данные, что в некоторых из этих реакций марганец может быть заменен кобальтом. Марганец принимает участие в азотном обмене в процессе восстановления нитратов до аммиака. Этот процесс проходит через этапы, катализируемые рядом ферментов, некоторые из которых, например, зависимы от марганца. В связи с этим растения, испытывающие недостаток марганца, не могут использовать нитраты в качестве источника азотного питания. Марганец активирует ферменты, участвующие в окислении важнейшего фитогормона — ауксина. В отсутствие марганца хлорофилл быстро разрушается на свету.
Медь поступает в растение в виде иона Сu2+ или Сu+. Она входит непосредственно в состав ряда ферментных систем, относящихся к группе оксидаз, таких, как полифенолоксидаза, аскорбатоксидаза, цитохромоксидаза. В этих ферментах медь соединена с белком, по - видимому, через SH-группы. Кроме того, медь активирует ряд ферментов, в частности нитритредуктазу, а также протеазы. Отсюда вытекает роль меди в азотном обмене. Большая часть меди (75% от всего содержания меди в листьях) концентрируется в хлоропластах. В хлоропластах сосредоточен и медьсодержащий белок синего цвета — пластоцианин. Содержание меди в пластоцианине составляет 0,57%. Медь, подобно железу и марганцу, обладает способностью к обратимому окислению и восстановлению: Сu2++e-→Сu +.Именно поэтому пластоцианин занимает определенное место в цепи переноса электронов между первой и второй фотосистемами. В связи с этим понятно значение меди для процесса фотосинтеза.
Цинк поступает в растение в виде ионов Zn +. Он входит в состав ферментов — фосфатазы, карбоангидразы и др. Карбоангидраза катализирует разложение гидрата окиси углерода на воду и углекислый газ. Эта реакция важна для процесса фотосинтеза. Углекислый газ, поступая в клетку, растворяется в воде, образуя H2СОз. Фермент карбоангидраза, катализируя высвобождение СО2 из гидрата окиси углерода, способствует его использованию в процессе фотосинтеза. Кроме того, цинк активирует такие ферменты, как енолаза, альдолаза, гексокиназа, триозофосфатдегидрогеназа. В этой связи понятно значение цинка для процесса дыхания. Цинк играет важную роль при образовании фитогормона ауксина. Это связано с тем, что цинк, повышая активность триптофансинтетазы, влияет на образование аминокислоты триптофана — предшественника ауксина. Внесение цинка повышает содержание ауксинов и заметно сказывается на темпах роста растений.
Молибден поступает в растение в виде аниона МоО42- При недостатке молибдена происходят заметные изменения в азотном обмене растений — наблюдается уменьшение синтеза белка при одновременном падении содержания аминокислот и амидов. Нарушения в азотном обмене проявляются, особенно на фоне питания растений нитратами. Это связано с тем, что молибден входит в активный центр фермента, восстанавливающего нитраты до нитритов,— нитратредуктазу. Нитратредуктаза — это флавопротеид, простетической группой которого является флавинадениндинуклеотид (ФАД). При восстановлении нитратов молибден действует как переносчик электронов от флавинадениндинуклеотида к нитрату, при этом NОз- переходит в NO2, а Мо5+ переходит в Мо6+. Образование нитратредуктазы является одним из немногих примеров адаптивного синтеза ферментов в растительном организме. Этот фермент образуется, когда в среде имеются нитраты и молибден. Активность нитратредуктазы возрастает в 10 раз и более при питании растений нитратами по сравнению с аммиаком, причем появление фермента происходит уже через 1—3 ч после внесения в среду нитратов. Молибден вместе с железом входит в состав ферментного комплекса нитрогеназы в виде Mo-Fe-белок и участвует в фиксации азота атмосферы различными микроорганизмами. По-видимому, он обладает и другими функциями, так как необходим растению и в условиях достаточного уровня аммиачного питания. При недостатке молибдена содержание аскорбиновой кислоты резко падает. При отсутствии молибдена наблюдаются нарушения в фосфорном обмене растений.
Бор поступает в растение в виде аниона борной кислоты — ВОз3-. Среднее содержание бора в растениях 0,0001%. Роль бора выяснена далеко не достаточно. Это связано с тем, что бор, в отличие от большинства других микроэлементов, не входит в состав ни одного фермента. Большое значение для осуществления функции бора имеет его способность давать комплексные соединения. Комплексы с борной кислотой образуют простые сахара, полисахариды, спирты, фенольные соединения и др. В этой связи можно предположить, что бор влияет на скорость ферментативных реакций, активируя или инактивируя не сами ферменты, а субстраты, на которые действуют ферменты. Комплексы органических соединений с борной кислотой могут иметь и иное значение. Так, способность бора образовывать комплексы с углеводами оказывает влияние на клеточную оболочку, регулируя ориентацию мицелл целлюлозы, что способствует ее большей эластичности (Е. В. Бобко). У растений, испытывающих недостаток бора, наблюдается быстрая потеря эластичности клеточных оболочек, что, в свою очередь, связано с более жесткой ориентацией мицелл целлюлозы. При недостатке бора наблюдается накопление кофейной и хлорогеновой кислот, которые считаются ингибиторами роста растений. Бор усиливает рост пыльцевых трубок, прорастание пыльцы. В этой связи опрыскивание бором способствует оплодотворению.
Хлор поступает в растение в виде С1-. Показана его необходимость при фотосинтетическом окислении воды и переносе e - на Хл680. Имеются еще и такие элементы, которые усиливают рост лишь определенных групп растений.
Кобальт. Благоприятное влияние оказывает кобальт на рост ряда растений. Кобальт входит в состав витамина B12 и некоторых связанных с ним соединений. Витамин B12 не поступает извне, а синтезируется в растениях даже в стерильных условиях. Это говорит в пользу необходимости кобальта. Кобальт, наряду с молибденом, необходим при фиксации азота атмосферы симбиотическими микроорганизмами. В связи с этим понятно, что сильнее нуждаются в кобальте бобовые растения. Установлена необходимость кобальта для сине-зеленых водорослей. Трудность решения вопроса о необходимости кобальта для всех растений заключается в том, что потребность в нем чрезвычайно мала.
Для роста некоторых растений засоленных почв (галофитов) оказывается полезным натрий. Благоприятное влияние оказывает натрий на рост сахарной свеклы и цианобактерий.
Для роста диатомовых водорослей необходим кремний. Он улучшает рост некоторых злаков, таких, как рис и кукуруза. Кремний повышает устойчивость растений против прилегания, так как входит в состав клеточных стенок.
Не все растения одинаково нуждаются и в тех элементах, которые относят к необходимым. Так, уже упоминалось, что бор значительно меньше нужен злакам. Бор и кальций абсолютно необходимы для всех высших растений, что касается низших, то во многих случаях они могут расти и в отсутствие этих элементов. Для некоторых бактерий и грибов кальций может быть заменен стронцием или барием. Бобовые больше нуждаются в молибдене по сравнению с другими семействами. Калий в некоторых случаях и в небольших количествах может быть заменен рубидием или цезием. Бериллий может заменить магний для некоторых грибов и частично для томатов.[5,6]
II. Почвенный мониторинг.
Анализ почвенных образцов (Исследовательский метод химического состава почвы по книге Н.Я Логинова) [8]
Оборудование:
1)Буры почвенные или железные лопаты.
2)Мешочки полиэтиленовые или полотняные.
3)Этикетки для почвенных образцов.
4)Двух метровые вешки.
5)Шагомер и рулетка.
Методика работы.
Наиболее распространенный способ отбора смешанных почвенных образцов – метод «конверта». Сущность метода состоит в том, что с обследуемого элементарного участка берут пять образцов почвы, причем точки отбора проб расположены так, что при мысленном соединении их прямыми линиями получается рисунок запечатанного конверта, длина стороны квадрата которого составляет 2-3 метра.
Масса каждого образца должна составлять примерно 200-300 г. Смешанные образцы упаковывают, помещают в полиэтиленовые или полотняные мешочки и снабжают этикетками с указанием места и даты взятия образца и его номера.
Методика приготовления водной (солевой) вытяжки:
Отобранную пробу почвы очищают от инородных включений, камней. Почва должна быть рассыпчатой.
На технических весах взвешивают примерно 50-60 г воздушно-сухой почвы (средняя проба) в конической колбе.
Добавляют к почве дистиллированную воду в соотношении 1:5.
Колбу закрывают пробкой и энергично перемешивают в течении 3-5 мин.
По окончании встряхивая всю суспензию почвы с водой, не давая ей отстояться, осторожно и быстро пропускают через бумажный фильтр в сухую колбу.
Для получения солевой вытяжки операции повторяются в той же последовательности, но вместо воды используется 1 н раствор хлорида калия. Солевую вытяжку получают после суточного контакта почвы с раствором соли.
Определение концентрации отдельных компонентов - естественных и антропогенных - в водной вытяжке проводят аналогично тому, как проводится данное определение в воде. Однако результат необходимо рассчитывать на навеску взятой пробы почвы.
Анализ почвенных образцов проводился на нескольких площадках:
1 проба - Дендрарий, находящийся на территории школьного участка.
2 проба - Центральная клумба школьного участка.
3 проба - Почва с аллеи лип по улице Солнечная.
4 проба - Почва с аллеи дубов по улице Солнечная.
5 проба- Клумба пришкольного участка.
6 проба – Почва с аллеи ив по улице Солнечная.
В результате работ были получены данные, которые представлены в таблицах (6-17).
III. Оценка влияния состояния окружающей среды на состояние древесных растений на примере дуба.
Один из методов оценки качества урбанизированной среды - оценка состояния окружающей среды по растениям.
В современное время для полной картины экологической ситуации в конкретной местности необходимо использовать данные биомониторинга и проводить биоиндикационные исследования.
Биоиндикация – это обнаружение и определение биологически значимых антропогенных нагрузок на основе реакций на них организмов и их сообществ.
Биоиндикаторы – это организмы, присутствие, количество или особенности, развития которых служат показателем антропогенных изменений среды.
Растение – индикатор – это такое растение, у которого признаки повреждения появляются при воздействии на него фитотоксичной концентрации загрязняющего вещества или смеси таких веществ. Растение – индикатор является химическим сенсором, который может обнаружить в воздухе присутствие загрязняющего вещества. К таким веществам относятся тяжелые металлы, фтористый водород, сероводород, аммиак, оксид серы (IV) и др. в результате их воздействия у растений может измениться скорость роста и созревания, возникнуть ухудшение цветения, состояние листовой пластинки, образования плодов и семян, измениться процесс размножения и, в конечном счете, снизится продуктивность и урожайность.
В данной работе в качестве биоиндикатора был выбран дуб черешчатый.
Дубы занимают первое место в полезащитном лесоразведении; превосходят многие породы по оздоровительному влиянию на окружающую среду (интенсивно выделяют кислород). Дубы, особенно старые деревья, отличаются высокими эстетическими качествами и издавна используются при создании парков, в аллейных посадках.
«Гляжу ль на дуб уединенный,
И мысль: патриарх лесов
Переживет мой век забвенный,
Как пережил он век отцов».
А.С. Пушкин
Дуб – летописец. Живая хронология дней ушедших. Дерево это как бы связало времена. Угасшие эпохи и столетия прислали в наши дни живого свидетеля – они доверили дубу память о себе, о былых днях и подвигах, о предках, которыми мы гордимся. Есть что-то бравое и былинное в самом слове “дубрава”. Слышится в нем гул старины и шелест листвы молодых дубков.
В “Лесном словаре ” начала прошлого века написано о дубе: “Дерево это поставлено на той же ступени, на какой лев находится между четвероногих, а орел между птиц. И дуб сделался эмблемой высоты, силы, долговечности”.
Факторами, влияющими на рост и развитие дуба в наших климатических условиях, помимо недостатка тепла, являются высокая кислотность, сильная оподзоленность и большая влажность почвы.
В нашем городе тоже есть уголки, где растут дубы и используются для оздоровительных и эстетических целей. Поэтому было решено посмотреть, как живется дубам в нашей городской среде и есть ли отличия в их развитии от дубов, произрастающих в естественных условиях.
Для объективности оценки состояния дубов выбрали два участка: аллея вдоль улицы Солнечная с оживленным автомобильным движением [фото 1,2,3,4] и на берегу
р. Глуховка, где они растут в естественных условия [фото 5,6]


Фото 1. Фото 2.


Фото 3. Фото 4.
 Фото 5 .
Фото 5 .  Фото 6.
Фото 6.
Цель: оценить влияние состояния окружающей среды на состояние древесных растений на примере дуба.
Задачи:
Изучить имеющуюся литературу по данному вопросу
Провести практическую работу с использованием весового метода Л.В. Дорогань.
Проанализировать полученные данные, сделать выводы.
Методика. Работа проводилась с использованием весового метода Л.В. Дорогань. Метод заключается в определение площади листьев у древесных растений в загрязненной и чистой зонах.
Для проведения работ использовалось следующее оборудование:
лист белой бумаги, ножницы, весы технические, линейка, авторучка, карандаш, калькулятор, фотоаппарат.
Согласно методике был установлен переводной коэффициент, который основан на сравнении веса квадрата бумаги с весом листа, имеющего такую же длину и ширину.
Для этого брался лист бумаги, очерчивался квадрат, равный длине и ширине листа дуба. Затем аккуратно обводились его контуры. Далее вычислялась площадь квдрата бумаги, взвешивались лист бумаги и вырезанный контур листа. После этого определялся переводной коэффициент по формуле:
К = sл/Sкв
где К – переводной коэффициент; Sл – площадь листа; Sкв. – площадь квадрата бумаги;
Sл = Рл*Sкв/Ркв ,
где Pл – масса контура листа; Sкв – площадь квадрата бумаги; Ркв – масса квадрата бумаги.
Далее было собрано по 100 листьев с деревьев дуба черешчатого, произрастающих вдоль автомагистрали города и в пригородной зоне, вблизи р. Глуховка. У собранных листьев были замерены длина и ширина и вычислена площадь каждого листа по формуле:
S = А*В*К,
где А – длина листа; В – ширина листа; К – переводной коэффициент;
По полученным показателям были построены кривые изменения признака в разных экологических условиях, сделаны выводы.
5. Результаты исследования.
В результате работ были получены данные, которые представлены в таблицах 1, 2,3,4.
Были сделаны фотографии с места сбора листьев [фото 1,2,3,4,5,6].
Таблица 1. Изменения значений у листьев, собранных вдоль автомагистрали.
| №пп | А.(см.) | В. (см.) | S см.2 | №пп | А. см. | В. (см.) | S см.2 |
| 1 | 15,5 | 8,2 | 73,09 | 51 | 11,1 | 5,4 | 34,4 |
| 2 | 14 | 8,1 | 65,2 | 52 | 19 | 10,9 | 119,0 |
| 3 | 11,4 | 5 | 32,7 | 53 | 18 | 10,1 | 104,5 |
| 4 | 9,7 | 5 | 27,8 | 54 | 10,2 | 4,4 | 25,8 |
| 5 | 14 | 7,7 | 61,9 | 55 | 145 | 6,8 | 56,6 |
| 6 | 13,5 | 7,6 | 58,9 | 56 | 12,4 | 8,7 | 62,0 |
| 7 | 14 | 6,9 | 55,5 | 57 | 14,4 | 6,5 | 53,8 |
| 8 | 14,8 | 9,1 | 77,4 | 58 | 13,9 | 7,6 | 60,7 |
| 9 | 10 | 3,5 | 20,1 | 59 | 15,7 | 10,5 | 94,7 |
| 10 | 17 | 6,3 | 61,5 | 60 | 10,1 | 4,7 | 27,2 |
| 11 | 16,2 | 11 | 102,4 | 61 | 14 | 9 | 72,45 |
| 12 | 13 | 7,1 | 53,0 | 62 | 15 | 10,2 | 87,9 |
| 13 | 15,6 | 10,4 | 93,2 | 63 | 18 | 9,9 | 102,4 |
| 14 | 11 | 6,8 | 43,0 | 64 | 19,4 | 10,5 | 117,1 |
| 15 | 11,5 | 5, | 3,0 | 65 | 8,2 | 4,1 | 19,3 |
| 16 | 8,9 | 5,3 | 27,1 | 66 | 8 | 3,9 | 17,9 |
| 17 | 8 | 4,4 | 20,2 | 67 | 78 | 3,2 | 14,3 |
| 18 | 11,2 | 6,3 | 40,5 | 68 | 13 | 9 | 67,2 |
| 19 | 9,9 | 5,9 | 33,5 | 69 | 13,5 | 9,6 | 74,5 |
| 20 | 13,9 | 7,9 | 63,1 | 70 | 9,9 | 5,1 | 29,0 |
| 21 | 14 | 9 | 72,4 | 71 | 12 | 5,6 | 38,4 |
| 22 | 11 | 6,4 | 40,4 | 72 | 11,1 | 6,5 | 41,4 |
| 23 | 14,2 | 7,5 | 61,2 | 73 | 18 | 9,1 | 94,1 |
| 24 | 14,1 | 7,1 | 57,5 | 74 | 11 | 8,2 | 51,8 |
| 25 | 15,5 | 7,7 | 68,8 | 75 | 12,4 | 6,4 | 45,6 |
| 26 | 12 | 5,6 | 38,6 | 76 | 13,2 | 9 | 68,3 |
| 27 | 11,1 | 7,4 | 47,2 | 77 | 17 | 7,3 | 71,3 |
| 28 | 10,6 | 4,3 | 26,2 | 78 | 12,2 | 6,1 | 42,7 |
| 29 | 8 | 4 | 18,4 | 79 | 12 | 7 | 48,3 |
| 30 | 7,3 | 3,9 | 16,3 | 80 | 13,9 | 8,8 | 70,3 |
| 31 | 9,4 | 5,1 | 27,5 | 81 | 6,5 | 3,4 | 12,7 |
| 32 | 14,2 | 9,1 | 74,3 | 82 | 14,2 | 7,3 | 59,6 |
| 33 | 13,5 | 7,7 | 59,7 | 83 | 11 | 8 | 50,6 |
| 34 | 18,1 | 8,4 | 87,4 | 84 | 13 | 9,1 | 68,0 |
| 35 | 15,7 | 6,8 | 61,3 | 85 | 8,2 | 4,3 | 20,2 |
| 36 | 19,5 | 8,9 | 99,7 | 86 | 13,5 | 7,5 | 58,2 |
| 37 | 14 | 8,1 | 65,2 | 87 | 18 | 9,4 | 97,2 |
| 38 | 7,6 | 3,6 | 15,7 | 88 | 16,6 | 7,9 | 75,4 |
| 39 | 13 | 7,2 | 53,8 | 89 | 15,8 | 6,8 | 61,7 |
| 40 | 11,4 | 7,4 | 48,5 | 90 | 18 | 9 | 93,1 |
| 41 | 11,5 | 6,6 | 43,6 | 91 | 195 | 10,9 | 122,2 |
| 42 | 18 | 10,4 | 107,6 | 92 | 7,5 | 3,4 | 14,6 |
| 43 | 15, | 10,2 | 87,9 | 93 | 12,1 | 6,3 | 43,8 |
| 44 | 14,2 | 7,5 | 61,2 | 94 | 14,4 | 6,7 | 55,4 |
| 45 | 13,2 | 7,4 | 56,1 | 95 | 15 | 7,2 | 62,1 |
| 46 | 14,6 | 9,5 | 79,7 | 96 | 19,8 | 11,7 | 133,2 |
| 47 | 13,2 | 7,1 | 53,8 | 97 | 11,6 | 6,6 | 44,0 |
| 48 | 15,1 | 8,3 | 72,0 | 98 | 16,4 | 8,5 | 80,1 |
| 49 | 6,9 | 3,8 | 15,0 | 99 | 6,7 | 4,1 | 15,7 |
| 50 | 7 | 4,1 | 16,5 | 100 | 10,5 | 5,5 | 33,2 |
Таблица 2. Изменения значений у листьев, собранных в чистой зоне.
| №пп | А.(см.) | В. (см.) | S см.2 | №пп | А. см. | В. (см.) | S см.2 |
| 1 | 16,9 | 9,3 | 90,3 | 51 | 13 | 7 | 52,3 |
| 2 | 10,5 | 7 | 42,2 | 52 | 16,8 | 9,2 | 88,8 |
| 3 | 14,7 | 8,1 | 68,4 | 53 | 16,4 | 8,1 | 76,3 |
| 4 | 13,4 | 7,2 | 55,4 | 54 | 13 | 8 | 59,8 |
| 5 | 13,2 | 7,5 | 56,9 | 55 | 13 | 8,1 | 60,5 |
| 6 | 14,4 | 7,6 | 62,9 | 56 | 16,4 | 8,9 | 83,9 |
| 7 | 14 | 7,5 | 60,3 | 57 | 11,4 | 7,9 | 51,7 |
| 8 | 12,3 | 5,3 | 37,4 | 58 | 11 | 6,2 | 39,2 |
| 9 | 16,1 | 8,6 | 79,6 | 59 | 14,6 | 8,6 | 72,1 |
| 10 | 12,1 | 5,8 | 40,3 | 60 | 14,8 | 9 | 76,5 |
| 11 | 13,6 | 8,3 | 64,9 | 61 | 14,4 | 7,5 | 62,1 |
| 12 | 12,3 | 7 | 49,5 | 62 | 13 | 8,8 | 65,7 |
| 13 | 16,4 | 9,4 | 88,6 | 63 | 13,5 | 6,7 | 52,0 |
| 14 | 12,9 | 7,2 | 53,4 | 64 | 13,5 | 8 | 62,1 |
| 15 | 13,5 | 6,5 | 50,4 | 65 | 17,4 | 10,6 | 106,0 |
| 16 | 9,7 | 5,2 | 29,0 | 66 | 13,5 | 6,7 | 52,0 |
| 17 | 12,2 | 7 | 49,1 | 67 | 13,5 | 8 | 62,1 |
| 18 | 11,6 | 6,3 | 42,0 | 68 | 17,4 | 10,6 | 106,0 |
| 19 | 13 | 8 | 59,8 | 69 | 13,5 | 8,5 | 65,9 |
| 20 | 14,9 | 6,7 | 57,4 | 70 | 13 | 7 | 52,3 |
| 21 | 14,4 | 7,4 | 61,2 | 71 | 9,7 | 5,2 | 29,0 |
| 22 | 13,1 | 7 | 52,7 | 72 | 15,3 | 8,2 | 72,1 |
| 23 | 14,9 | 8,5 | 72,8 | 73 | 13,5 | 8,1 | 62,8 |
| 24 | 12,2 | 6,5 | 45,5 | 74 | 14,6 | 7,7 | 64,6 |
| 25 | 9 | 4,8 | 24,8 | 75 | 13,3 | 8 | 61,1 |
| 26 | 11 | 6,2 | 39,2 | 76 | 14,2 | 8,1 | 66,1 |
| 27 | 12,3 | 4,2 | 29,7 | 77 | 18 | 11 | 113,8 |
| 28 | 11,1 | 6,4 | 40,8 | 78 | 15 | 9 | 77,6 |
| 29 | 12,6 | 5,8 | 42,0 | 79 | 11,8 | 6,5 | 44,1 |
| 30 | 13,7 | 8 | 63,0 | 80 | 9,6 | 5,4 | 29,8 |
| 31 | 11,1 | 6,4 | 40,8 | 81 | 16 | 9 | 82,8 |
| 32 | 15,3 | 8,8 | 77,4 | 82 | 11,5 | 7,6 | 50,2 |
| 33 | 11,2 | 5,3 | 34,1 | 83 | 12,2 | 6,3 | 44,1 |
| 34 | 12,3 | 7,6 | 53,7 | 84 | 17,5 | 10,7 | 107,6 |
| 35 | 13,2 | 6,3 | 47,8 | 85 | 19,3 | 10,2 | 113,1 |
| 36 | 13,5 | 7,4 | 57,4 | 86 | 12 | 6 | 41,4 |
| 37 | 16,8 | 9 | 86,9 | 87 | 11,4 | 5,4 | 35,3 |
| 38 | 15,1 | 9,4 | 81,6 | 88 | 12,5 | 5,5 | 39,5 |
| 39 | 12,2 | 6,7 | 47,0 | 89 | 13,2 | 9,1 | 69,0 |
| 40 | 11,2 | 6,4 | 41,2 | 90 | 13,2 | 10 | 75,9 |
| 41 | 11,9 | 7,9 | 54,0 | 91 | 83,5 | 8,3 | 64,4 |
| 42 | 12,8 | 6,6 | 48,5 | 92 | 14,6 | 7 | 58,7 |
| 43 | 12,5 | 6,7 | 48,1 | 93 | 13,6 | 8,2 | 64,1 |
| 44 | 14 | 8,6 | 69,2 | 94 | 13,9 | 8,1 | 64,7 |
| 45 | 19,1 | 7,9 | 86,7 | 95 | 13 | 7,7 | 57,5 |
| 46 | 12,5 | 7,8 | 56,0 | 96 | 14 | 7,8 | 62,7 |
| 47 | 14 | 9 | 72,4 | 97 | 15,2 | 8,5 | 74,2 |
| 48 | 12,1 | 6 | 41,7 | 98 | 16,5 | 9,3 | 88,2 |
| 49 | 14 | 8,4 | 67,2 | 99 | 10,6 | 5,9 | 35,9 |
| 50 | 12,6 | 7 | 50,7 | 100 | 9,2 | 5,5 | 29,0 |
Таблица 3. Частота встречаемости в загрязненной зоне.
| Классы площадей см2 | Частота встречаемости шт. | Классы площадей см2 | Частота встречаемости шт. |
| 10-14 | 1 | 75-79 | 3 |
| 15-19 | 8 | 80-84 | 1 |
| 20-24 | 2 | 85-89 | 3 |
| 25-29 | 7 | 90-94 | 3 |
| 30-34 | 5 | 95-99 | 1 |
| 35-39 | 2 | 100-104 | 2 |
| 40-44 | 8 | 105-109 | 1 |
| 45-49 | 4 | 110-114 | 0 |
| 50-54 | 6 | 115-119 | 2 |
| 55-59 | 9 | 120-124 | 1 |
| 60-64 | 10 | 125-129 | 0 |
| 65-69 | 6 | 130-134 | 1 |
| 70-74 | 8 |
|
|
Таблица 4. Частота встречаемости в чистой зоне.
| Классы площадей см2 | Частота встречаемости шт. | Классы площадей см2 | Частота встречаемости шт. |
| 10-14 | 0 | 65-69 | 6 |
| 15-19 | 0 | 70-74 | 4 |
| 20-24 | 1 | 75-79 | 6 |
| 25-29 | 5 | 80-84 | 3 |
| 30-34 | 1 | 85-89 | 3 |
| 35-39 | 5 | 90-94 | 1 |
| 40-44 | 11 | 95-99 | 0 |
| 45-49 | 5 | 100-104 | 0 |
| 50-54 | 11 | 105-109 | 3 |
| 55-59 | 9 | 110-114 | 2 |
| 60-64 | 12 | 115-119 | 0 |
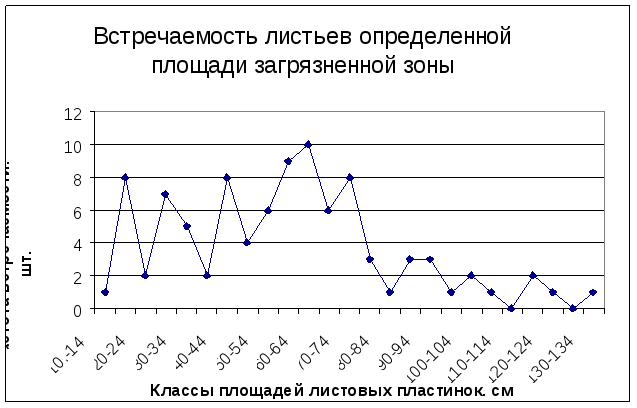
Рис. 1. График встречаемости листьев определенной площади загрязненной зоны.
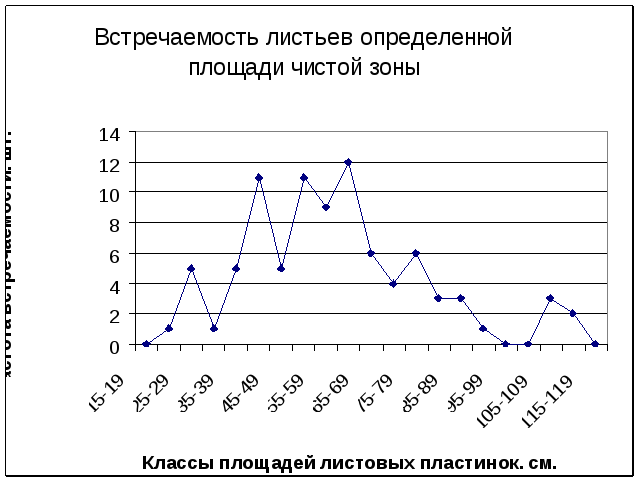
Рис. 2. График встречаемости листьев определенной площади чистой зоны.
Вывод
В результате проведенных работ было установлено, что дубы, высаженные в городской среде на аллее, подвергаются отрицательному воздействию окружающей среды. Об этом свидетельствуют повреждения на листовых пластинках [фото 3, 4]
Размеры листовых пластин широко варьируют, что говорит об изменении условий среды произрастания, и действии негативных факторов, таких, как пыль, загазованность, наличие мелких частиц соли, которые, попадая на листовые пластины, нарушают процессы жизнедеятельности (газообмен, транспирацию).
Широкая норма реакции (широкая приспособляемость) [рис.1] в данном случае играет важное значения для выживания вида.
На р. Глуховка листовые пластины дуба не имеют повреждений [фото 6]. Деревья дают менее выраженную модификационную изменчивость по размеру листовой пластины, что говорит о достаточно однообразных условиях развития дуба, которые являются благоприятными. Этот признак (размер листовой пластины) находится среди средних значений вариационного ряда, что отражено на графике [рис.2.].
Таким образом, видно, что загрязнение окружающей среды оказывает влияние на развитие данного вида древесных пород и его состояние. По изменениям в развитии, в данном случае площади листовой пластины, можно судить о наличии загрязнения в окружающей среде.
А также можно сказать, что метод, предложенный Л. В. Дорогань, отображает реальную ситуацию.
На площадке дубовой аллеи взяты пробы для определения состава почв.
Таблица 5. Содержание катионов и анионов в почве на аллее дубов.
| КАТИОНЫ | АНИОНЫ |
| Дуб | Mg2+ | Ca2+ | Fe2+ | Fe3+ | Cu2+ | Al3+ | Hg2+ | SO42- | Co42- | HPO42- | Cl- | NO3- |
| Наличие катиона | + | + | - | - | +! Сильный раствор. | + | + | - | - | + | + | - |
| Кислотность -основность | pH 6 Слабокислая реакция почвы. |
|
|
|
|
|
|
|
|
|
|
|
Результат:
Анализируя наличие катионов и анионов в почве, делаем вывод, что почва на этом участке содержит катионы Mg2+ и Ca2+ как и большинство почв. В кислых почвах (подзолистых) среди поглощенных катионов значительную часть занимают Н+ и А13+. Отрицательным результатом является е отсутствие Fe2+, Fe3+ и наличие Hg2+ из катионов. Отсутствие NO3- и
SO42- тоже отрицательно сказывается на росте и развитии растений.
Пришкольный учебно-опытный участок.
На разных площадках пришкольного учебно-опытного участка взяты пробы для определения состава почв. В МОУ «СОШ №7» с 1993 года существует пришкольный учебно-опытный участок. К настоящему времени пришкольный участок представляет собой хорошо разработанную и ухоженную территорию с большим видовым разнообразием растений. Почвенный покров создан искусственно и представляет собой неоднородные по механическому и физическому составу участки почвы, которые разбросаны по всей территории. Плодородный слой тонкий, наносной, т.к. он формируется в течение 20 лет с момента закладки и разработки УОУ. На участке почвы в основном слабокислые. В микрорельефе преобладают микропонижения и поэтому степень увлажненности почвенного покрова высокая. Почва легко и хорошо прогревается, что создает достаточно комфортные условия для роста и развития растений, особенно подземной корневой части. Почва подвергается уплотнению и вытаптыванию, а так как почвенный покров небольшой по мощности, то это отражается на свойствах почвы.
Дендрологический отдел занимает площадь 400м2, представлен деревьями и кустарниками. Здесь учащиеся знакомятся с жизненными формами растений, условиями их роста и развития.
Площадь деревьев и кустарников по периметру крон, приходящаяся на одного учащегося рассчитали по формулам:
P = 2πr, где Р –периметр кроны, π – 3, 14, r – радиус.
S = Ph, где S – площадь, h – высота .
Количество деревьев и кустарников на УОУ (1,5 га):
174 дерева + 672 кустарника = 846
Учащихся в школе – 504 чел.
Определение средних значений:
Таблица 6.
Деревья. P ср. = 2πr r1 - 200, r 2 - 108, r 3 - 150,r4 - 176, r5 - 215 r ср.= 200+108+150+176+215:5 r ср. = 170 см =1,7 м Р ср. = 2*3,14 *170=1068см = 10,68 м S=P*h h1 -500, h2 -287, h3 - 435, h4 - 391, h5 - 405 h ср.-500+287+435+391+405:5 h ср. = 404см = 4,04м S ср. = Р ср.*h ср. S ср.= 1068 * 404 = 431472см2 = =43,1472м2 S всех деревьев = Sср.*174 S всех деревьев = 431472 * 174 = =75076128см2 = 7507, 6128м2 | 2. Кустарники: P ср. = 2πr r1 - 183, r 2 - 24, r 3 - 70, r4 - 60, r5 – 45 r ср. =183+24+70+60+45:5 r ср. = 76см = 0,76м Р ср.= 2 * 3,14 * 76 = 480см = 4,8м2 S ср. = Р ср.*h ср. h1 -100, h2 -205,h3 - 296,h4 - 68, h5 - 159 h ср. = 100+205+296+68+159:5 h ср. = 166см = 1,66м S ср. = 480 * 166 * 627 = 49959360см2 = = 4995,9360м2
|
S всех д. и к. = S всех дер. + S всех куст.
S всех д. и к. = 75076128 + 49959360 = 125035488 см2 = 12503, 5488м2
S на одного ребенка = S всех деревьев и кустарников: кол – во всех учащихся
Кол – во всех учащихся = 504 чел.
S на одного ребенка = 125035488: 504 = 248086, 2857 248086см2 25м2
Результаты: 25м2 – площадь деревьев и кустарников по периметру крон, приходящаяся на одного учащегося школы №7.
Исследование состава почвы .
Были взяты пробы почвы из центральной клумбы, дендрария, клумбы с березой [фото 7,8,9]. Было проведено исследование по нахождению катионов и анионов.



Фото7. 1-. Фото 8. 2- Центральная клумба№2. Фото 9. 3- Клумба №3.
В результате работ были получены данные, которые представлены в таблицах (6-17)
Катионы
Таблица 6. Наличие магния в почвах.
|
1 аналитическая группа |
| Mg2+ | Контрольный образец | 1 | 2 | 3 |
| NH4OH | Белый осадок | нет | нет | нет |
Таблица 7. Наличие кальция в почве
|
2 аналитическая группа |
| Ca2+ | Контрольный образец | 1 | 2 | 3 |
| H2SO4 (2 H) | Белые кристаллы | нет | нет | есть |
Таблица 8. Наличие двухвалентного железа в почве
| 3 аналитическая группа |
| Fe3+ | Контрольный образец | 1 | 2 | 3
|
| KCHS | Осадок кроваво-красный | потемневший осадок | есть | нет |
Таблица 9. Наличие трехвалентного железа в почве.
| Fe2+ | Контрольный образец | 1 | 2 | 3 |
| Щелочь | Зеленый осадок | нет | нет | нет |
Таблица 10. Наличие меди в почве.
| 4 аналитическая группа |
| Cu2+ | Контрольный образец | 1 | 2 | 3 |
| Na2S2O3 | Темно-коричневый осадок | есть | есть | есть |
Таблица 11. Наличие алюминия в почве
| Al3+ | Контрольный образец | 1 | 2 | 3 |
| CaSO4*H2O горение | Темно-синий пепел | есть(слабый) | есть(слабый) | есть |
Таблица 12. Наличие ртути в почве.
| Hg2+ | Контрольный образец | 1 | 2 | 3 |
| KY | Красный осадок | есть(сильный) | есть | нет |
Анионы
Таблица 13.
| 1 аналитическая группа |
| SO42- | Контрольный образец | 1 | 2 | 3 |
| Ba2+ | Белый осадок | нет | есть | нет |
Таблица 14.
| HPO42- | Контрольный образец | 1 | 2 | 3 |
| MgCl2 | Белый осадок | есть | есть | есть |
Таблица 15.
| Cl- | Контрольный образец | 1 | 2 | 3 |
| Ag+ | Творожный осадок | есть | есть | есть |
Таблица 16
| NO3- | Контрольный образец | 1 | 2 | 3 |
| H2SO4 | Бурая окраска | нет | есть | есть |
Таблица 17. Кислотно-щелочная среда почвы.
| Индикаторная бумажка | 1 | 2 | 3 |
| pH 6 | pH5 | pH7 |
Результаты:
Анализ результатов исследования состава почвы УОУ показал, что не везде почвы благоприятны для роста и развития растений. Отмечается отсутствие магния, кальция. Неблагоприятным является наличие в почве ртути. Слабокислая почва требует раскисления.
Выводы:
Растения древесных пород подвергаются влиянию факторов внешней среды, в том числе и состава почв.
Рекомендации:
Необходимо проводить мониторинг состава почвы. При необходимости вносить удобрения или химические вещества, необходимые для нормального роста и развития растений.
Список литературы
1.Шабес Л.К., Клейменова Л.М.. « Деревья и кустарники Петербурга и Ленинградской области». С-Петербург, Издательство РГПУ им. Герцена, 1999.
2.Бобров Р. «Беседы о лесе». Москва, Молодая гвардия, 1979.
3.Трайтак Д.И.. «Книга для чтения по ботанике». Москва, Просвещение, 1985.
4.Сергеев Б. «Жизнь лесных дебрей». Москва, Молодая гвардия, 1988.
5. http://bluebells.narod.ru/ground/kisl.html
6. Агрохимия. - 2-е изд., перераб. и доп. под ред. Смирнов П.М., Муравин Э.А
7. http://www.cottagesspb.ru/ekologiya/tehnogennye/
8. Н.Я Логинов «Исследовательский метод химического состава почвы»
Содержание стр.
Введение 2
I. Состав почвы 3
II Почвенный мониторинг 10
III Оценка влияния состояния окружающей среды на состояние 11
древесных растений на примере дуба
IV Пришкольный учебно-опытный участок 18
Вывод 22
Рекомендации 22
Список литературы 23
:
13









 Фото 5 .
Фото 5 .  Фото 6.
Фото 6.