Занятие по химии на тему : «Решение задач на растворы» (задания ЕГЭ №27 )
Подготовила:
учитель химии
МКОУ Аверьяновская СОШ
Кизлярского района
ИСМАИЛОВА ХАДИЖАТ АМИРАРСЛАНОВНА

- массовая доля вещества в растворе
𝙢 р.в = × 𝙢 р-ра
𝙢 р-ра = 𝙢 р.в (соли)+ 𝙢 растворителя (воды)

27 задания, по оказываемым воздействиям на первоначальный раствор, условно делим на три группы:
I гр
1-й раствор (воздействия)
2-й раствор
а) разбавление
II гр
б) выпаривание
Изменяется только 𝙢 р-ра ,
+ 𝙢 (воды)
а 𝙢 р.в остается такой же
1-й раствор (воздействия)
- 𝙢 (воды)
2-й раствор
а) добавление соли
Изменяются 𝙢 р.в и 𝙢 р-ра
б) выпадение соли в осадок
III гр
+ 𝙢 (соли)
1-й раствор (воздействия)
- 𝙢 (соли)
3-й раствор
Приливают 2-й раствор
3 раствор
Изменяются 𝙢 р.в и 𝙢 р-ра
𝙢 (1 р.в) + 𝙢 (2 р.в)
𝙢 (1 р-ра) + 𝙢 (2 р-ра)
либо дана по условию, либо вычисляем.
Чтобы выразить в %, умножаем на 100 %.
Чтобы выразить в долях, % делим на 100%.

1. Упариванием 500 г раствора с массовой долей соли 10 % получен раствор с массовой долей соли 14 % . Вычислите массу выпаренной при этом воды. Ответ укажите в граммах с точностью до целых.
=
𝙢 р.в
×
𝙢 р-ра
𝙢 р.в
По условию задачи:
- Определяем, что известно для 1-го и 2-го растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
=
×
1 р-р
50
0,1
=
×
50
500
0,1
=
×
1 р-р
0,14
=
50
2–й р-р
×
×
0,14
50
=
2–й р-р
(500 – 𝝌)
50 = 0,14 × (500- 𝝌 )
50 = 70 – 0,14 𝝌
0,14 𝝌 = 70-50
× 𝝌 = 20 : 0,14
𝝌 = 142, 9
ответ до целых: 143г

2. К 240 г раствора с массовой долей соли 10% добавили 160 мл воды. Вычислите массовую долю соли в полученном растворе. Ответ дайте в процентах с точностью до целых .
𝙢 р-ра
𝙢 р.в
По условию задачи:
- Определяем, что известно для 1-го и 2-го растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
=
×
24
0,1
240
=
×
1-й р-р
𝝌
24
(240 +160)
2–й р-р
=
×
24 = 𝝌 × 400
𝝌 = 24: 400
𝝌 = 0,06
ответ в процентах до целых:
0,06 × 100% = 6%

3. К 75 г раствора с массовой долей соли 14% добавили 10 г этой же соли и 10 мл воды . Вычислите массовую долю соли в полученном растворе ( в процентах). (Запишите число с точностью до десятых.)
𝙢 р-ра
𝙢 р.в
По условию задачи:
- Определяем, что известно для 1-го и 2-го растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
=
×
10,5
75
0,14
=
×
1-й р-р
𝝌
10,5+10
(75+10 +10)
2–й р-р
=
×
20,5 = 𝝌 × 95
𝝌 = 20,5: 95
𝝌 = 0,216
ответ в процентах до десятых:
0,216 × 100% = 21,6%
6

4. При охлаждении 400 г горячего 50%-го раствора нитрата калия выпал осадок , не содержащий кристаллизационной воды. Чему равна масса осадка (в г), если раствор над осадком содержал 34% нитрата калия по массе? Ответ округлите до ближайшего целого числа.
𝙢 р-ра
𝙢 р.в
По условию задачи:
- Определяем, что известно для 1-го и 2-го растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
=
×
200
400
0,5
=
×
1-й р-р
0,34
200 - 𝝌
2–й р-р
(400- 𝝌)
=
×
200 - 𝝌 = 0,34 × (400- 𝝌 )
200 - 𝝌 = 136 – 0,34 𝝌
200 - 136 = 𝝌 - 0,34 𝝌
64 = 0, 66 𝝌
𝝌 = 64:0,66
𝝌 =96,97
ответ до целого числа: 97г
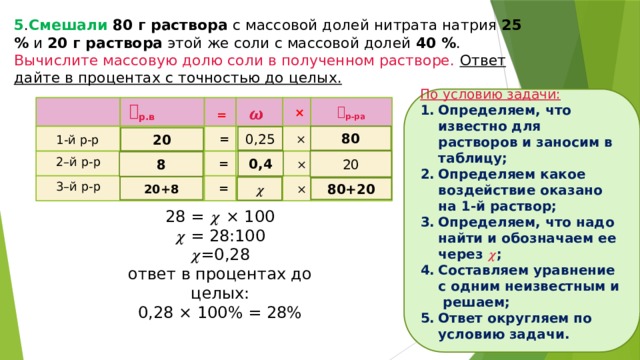
5 . Смешали 80 г раствора с массовой долей нитрата натрия 25 % и 20 г раствора этой же соли с массовой долей 40 % . Вычислите массовую долю соли в полученном растворе. Ответ дайте в процентах с точностью до целых.
По условию задачи:
- Определяем, что известно для растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
𝙢 р-ра
𝙢 р.в
×
=
80
0,25
20
=
×
1-й р-р
20
0,4
2–й р-р
8
=
×
3–й р-р
20+8
𝝌
80+20
=
×
28 = 𝝌 × 100
𝝌 = 28:100
𝝌 =0,28
ответ в процентах до целых:
0,28 × 100% = 28%
8
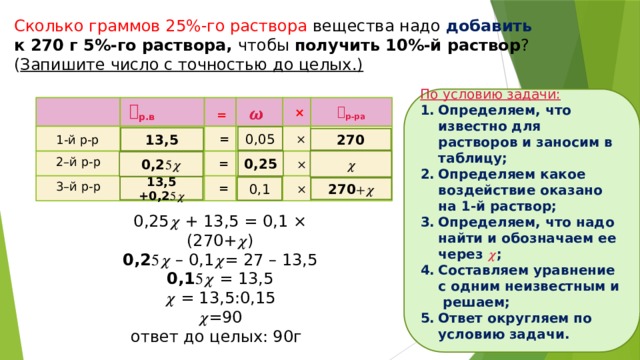
Сколько граммов 25%-го раствора вещества надо добавить к 270 г 5%-го раствора, чтобы получить 10%-й раствор ? ( Запишите число с точностью до целых.)
По условию задачи:
- Определяем, что известно для растворов и заносим в таблицу;
- Определяем какое воздействие оказано на 1-й раствор;
- Определяем, что надо найти и обозначаем ее через 𝝌 ;
- Составляем уравнение с одним неизвестным и решаем;
- Ответ округляем по условию задачи.
𝙢 р-ра
𝙢 р.в
×
=
0,05
13,5
270
=
×
1-й р-р
𝝌
0,25
2–й р-р
0,25𝝌
=
×
3–й р-р
13,5 +0,25𝝌
0,1
270+𝝌
=
×
0,25 𝝌 + 13,5 = 0,1 × (270+ 𝝌 )
0,25𝝌 – 0,1 𝝌 = 27 – 13,5
0,15𝝌 = 13,5
𝝌 = 13,5:0,15
𝝌 =90
ответ до целых: 90г 0
9

Задания для закрепления:
1. При выпаривании 25%-го водного раствора получено 60 г сухого вещества. Вычислите массу испарившейся воды. Ответ дайте в граммах с точностью до целых.
Ответ: 180
2. Вычислите массу гидроксида калия, который необходимо растворить в 150 г воды для получения раствора с массовой долей щёлочи 25 %. Ответ дайте в граммах с точностью до целых.
Ответ: 50
3.Растворяя соль в горячей воде, приготовили 300 г 40%-го раствора. При охлаждении раствора из него выпало 50 г осадка безводной соли. Вычислите массовую долю соли в растворе над осадком. Ответ дайте в процентах с точностью до целых.
Ответ: 40
4. Вычислите массу твёрдого нитрата аммония, который надо добавить к 210 г воды, чтобы получить 16%-й раствор соли. Ответ укажите в граммах с точностью до целых.
Ответ: 40

Спасибо за внимание!
9