Урок № Тема: Строение атома. Схема опыта Резерфорда
Цель урока: познакомить учеников со строением атома, планетарной моделью атома по Резерфорду.
Демонстрации:
Таблицы со схемой опыта Резерфорда и схемой планетарной модели атома.
Таблица «Периодическая система химических элементов Менделеева»
Ход урока
Повторение изученного материала
От каких факторов зависит сила взаимодействия заряженных тел?
Чем окружено всякое заряженное тело? Что называют электрическим полем?
Как можно обнаружить наличие электрического поля?
Раскройте механизм взаимодействия наэлектризованных тел с помощью представлений об электрическом поле.
Какую силу называют электрической силой?
Сравните действие электрического поля заряженного тела вблизи него и по мере удаления от него.
Наблюдение экранирующего действия проводника
Приборы и материалы: стрелка бумажная (или из фольги) на острие, линейка измерительная из оргстекла, кусок капроновой ткани, пластинка жестяная размером 60x90 мм.
Порядок выполнения работы:
Наэлектризуйте линейку, потерев ее о кусок капроновой ткани.
Поднесите конец заряженной линейки на некоторое расстояние 14- стрелке и, перемещая линейку то вправо, то влево, наблюдайте за движением стрелки.
Расположите металлическую пластинку вертикально между стрелкой и концом заряженной линейки. Затем снова перемещайте конец линейки около стрелки.
- Влияет ли электрическое поле заряженной линейки на стрелку?
Изучение нового материала
План изложения нового материала:
Модели атома, существовавшие до начала XIX в.
Опыты Резерфорда.
Ядерная модель атома Резерфорда.
Модели атома, существовавшие до начала XIX в
В начале века в физике бытовали самые разные и часто фантастические представления о строении атома.
Например, ректор Мюнхенского университета Фердинанд Линдеман в 1905 г. утверждал, что «атом кислорода имеет форму кольца, а атом серы - форму лепешки».
Продолжала жить и теория «вихревого атома» лорда Кельвина, согласно которой, атом устроен подобно кольцам дыма, выпускаемым изо рта опытного курильщика.
Но большинство физиков склонялись к мысли, что прав Дж. Дж. Томсон: атом - равномерно положительно заряженный шар диаметром 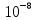 см, внутри которого плавают отрицательные электроны, размеры которых
см, внутри которого плавают отрицательные электроны, размеры которых 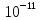 см. Сам Томсон относился к своей модели без энтузиазма.
см. Сам Томсон относился к своей модели без энтузиазма.
Джон Стоней еще в 1891 г. предполагал, что электроны движутся вокруг атома, подобно спутникам планет. Японский физик Хантаро Насаока в 1903 г. говорил, что атом представляет своего рода сложную астрономическую систему, подобно кольцу Сатурна.
Вопрос о строении атома изучали и русские физики: Петр Николаевич Лебедев и известный ученый-народник Николай Морозов.
Ни один из сторонников идеи планетарного атома не мог подтвердить опытом. Такой опыт в 1909 г. поставил Эрнест Резерфорд.
Опыты Резерфорда.
Английский физик Эрнест Резерфорд, исследуя излучение радиоактивных веществ, особое внимание уделил излучению, состоящему из положительно заряженных частиц, называемых 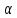 -частицами. Он установил, что каждая
-частицами. Он установил, что каждая  -частица, попадая на экран из сернистого цинка, вызывает вспышку света. Испытав рассеяние в золотой фольге,
-частица, попадая на экран из сернистого цинка, вызывает вспышку света. Испытав рассеяние в золотой фольге, 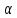 -частицы ударялись затем в экран и регистрировались с помощью микроскопа.
-частицы ударялись затем в экран и регистрировались с помощью микроскопа.
Согласно предложенной Томсоном -модели атома, 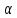 -частицы должны были бы свободно проходить сквозь атомы золота и только отдельные
-частицы должны были бы свободно проходить сквозь атомы золота и только отдельные 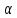 -частицы могли слегка отклоняться в электрическом поле электрона. Поэтому следовало ожидать, что пучок
-частицы могли слегка отклоняться в электрическом поле электрона. Поэтому следовало ожидать, что пучок 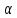 -частиц при прохождении через тонкую фольгу слегка расплывется на небольшие углы. Такое рассеивание на малые углы действительно наблюдалось, но совершенно неожиданно оказалось, что примерно одна
-частиц при прохождении через тонкую фольгу слегка расплывется на небольшие углы. Такое рассеивание на малые углы действительно наблюдалось, но совершенно неожиданно оказалось, что примерно одна 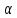 -частица из 20 000, падающих на золотую фольгу толщиной всего лишь 4 •
-частица из 20 000, падающих на золотую фольгу толщиной всего лишь 4 • 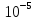 см, возвращается назад в сторону источника.
см, возвращается назад в сторону источника.
Резерфорду понадобилось несколько лет, чтобы окончательно понять столь неожиданное рассеяние 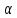 -частиц на большие углы. Он пришел к выводу, что положительный заряд атома сосредоточен в очень малом объеме в центре атома, а не распределен по всему атому, как в модели Томсона.
-частиц на большие углы. Он пришел к выводу, что положительный заряд атома сосредоточен в очень малом объеме в центре атома, а не распределен по всему атому, как в модели Томсона.
Ядерная модель атома Резерфорда
Резерфорд предложил ядерную («планетарную») модель атома:
атомы любого элемента состоят из положительно заряженной части, получившей название ядра;
размеры ядра малы по сравнению с размерами самого атома;
в ядре сконцентрирована почти вся масса атома;
в состав ядра входят положительно заряженные элементарные частицы - протоны (позднее было установлено, что и нейтральные нейтроны);
вокруг ядра вращаются электроны, образующие так называемую электронную оболочку;
отрицательный заряд всех электронов распределен по всему объему атома.
Пользуясь схемой, можно объяснить сначала строение атома водорода, имеющего один протон и один электрон. Затем рассматривается ядерная модель строения более сложных атомов - гелия и лития. В качестве упражнения может быть рассмотрено строение атомов более сложных элементов.
В процессе рассмотрения строения атомов различных элементов учитель задает вопросы:
Чем отличаются друг от друга атомы различных химических элементов?
Что является главной характеристикой определенного химического элемента?
Какие частицы входят в состав ядра?
Необходимо отметить, что атом, потерявший (или приобретший) один или несколько электронов, уже не является нейтральным, а будет иметь положительный (или отрицательный) заряд. Его называют положительным (или отрицательным) ионом.
Заряд ядра атома 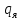 =
= 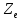 где е - элементарный электрический заряд; Z - порядковый номер элемента в таблице Менделеева, определяет число электронов в атоме.
где е - элементарный электрический заряд; Z - порядковый номер элемента в таблице Менделеева, определяет число электронов в атоме.
Химические свойства зависят только от зарядового числа.
Ядро состоит из протонов и нейтронов:
А = Z + N и 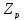 =
=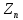 ,
,
где Z - число протонов в ядре, N - число нейтронов; А - массовое число (суммарное число нуклонов в ядре). 1 а.е.м. = 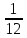 ·
· 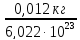 = 1,66058·
= 1,66058· 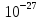 кг.
кг.
Закрепление изученного материала
В ядре атома углерода содержится 12 частиц. Вокруг ядра движутся 6 электронов. Сколько в ядре этого атома протонов и нейтронов?
Сколько протонов, нейтронов, электронов в положительном ионе лития?
Во что превратится атом натрия, если «убрать» из его ядра один протон, не изменяя количество электронов?
Что имеет большую массу: атом лития или положительный ион лития? Атом хлора или отрицательный ион хлора?
Домашнее задание: §30, вопросы к параграфу; выполнить упражнения к параграфу; № 1218, 1219.
Дополнительный материал
Эрнест Резерфорд
Эрнест родился 30 августа 1871 г. вблизи г. Нелсон (Новая Зеландия) в семье переселенца из Шотландии. Эрнест был четвертым из 12 детей. Мать работала сельской учительницей. Отец организовал деревообрабатывающее предприятие. Под руководством отца мальчик получил хорошую подготовку для работы в мастерской, что впоследствии помогало ему при конструировании и постройке научной аппаратуры. Окончив школу в Хавслоке, где в это время жила семья, он получил стипендию для продолжения образования в колледже Нелсон, куда поступил в 1887 г. В колледже на него оказали большое влияние его учителя: преподаватели физики, химии и математики.
Его магистерская работа касалась обнаружения высокочастотных волн.
В 1891 г., будучи студентом 2-го курса, Эрнест выступил в кружке с докладом «Эволюция элементов». Название доклада удивило всех слушателей. Он заявил, что все атомы - сложные вещества и построены из одних и тех же составных частей. Большинство участников кружка посчитало доклад лишенным здравого смысла. Но через 12 лет молодой ученый уже имел первые неопровержимые экспериментальные доказательства.
В 1903 г. его избирают членом Лондонского Королевского общества, а в 1907 г. Эрнест возвращается в Англию и занимает должность профессора кафедры физики Манчестерского университета. В университете Резерфорд вместе с Гейгером развернул работы по подсчету  -частиц с помощью сцинтилляционного метода. В 1908 г. Резерфорд становится Нобелевским лауреатом за исследование радиоактивных элементов.
-частиц с помощью сцинтилляционного метода. В 1908 г. Резерфорд становится Нобелевским лауреатом за исследование радиоактивных элементов.
С 1925-1930 гг. Эрнест Резерфорд - президент Королевского общества, а в 1931 г. получил титул барона и стал лордом. Школа Резерфорда становится самой большой в Манчестере.
В 1937 г. 19 октября умер Эрнест Резерфорд. Его смерть стала огромной утратой для науки.
«С уходом из жизни Эрнеста закончился путь одного из величайших людей, работавших в науке. Безграничный энтузиазм и неутомимое дерзание Резерфорда вели его от открытия к открытию», говорил про Эрнеста Н. Бор.






 см, внутри которого плавают отрицательные электроны, размеры которых 10-11
см, внутри которого плавают отрицательные электроны, размеры которых 10-11 см. Сам Томсон относился к своей модели без энтузиазма.
см. Сам Томсон относился к своей модели без энтузиазма.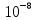 см, внутри которого плавают отрицательные электроны, размеры которых
см, внутри которого плавают отрицательные электроны, размеры которых 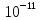 см. Сам Томсон относился к своей модели без энтузиазма.
см. Сам Томсон относился к своей модели без энтузиазма.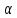 -частицами. Он установил, что каждая
-частицами. Он установил, что каждая  -частица, попадая на экран из сернистого цинка, вызывает вспышку света. Испытав рассеяние в золотой фольге,
-частица, попадая на экран из сернистого цинка, вызывает вспышку света. Испытав рассеяние в золотой фольге, 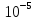 см, возвращается назад в сторону источника.
см, возвращается назад в сторону источника.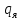 =
= 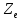 где е - элементарный электрический заряд; Z - порядковый номер элемента в таблице Менделеева, определяет число электронов в атоме.
где е - элементарный электрический заряд; Z - порядковый номер элемента в таблице Менделеева, определяет число электронов в атоме. 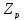 =
=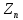 ,
,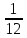 ·
· 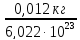 = 1,66058·
= 1,66058· 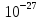 кг.
кг.









