Просмотр содержимого документа
«Угольная кислота. Карбонаты . Жесткость воды. mp4»

Угольная кислота.
Карбонаты.
Жёсткость воды
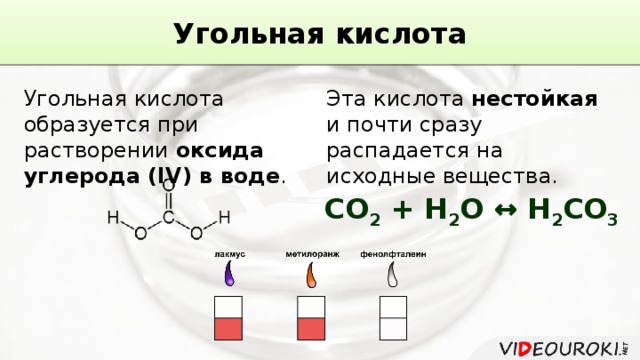
Угольная кислота
Угольная кислота образуется при растворении оксида углерода (IV) в воде .
Эта кислота нестойкая и почти сразу распадается на исходные вещества.
СО 2 + Н 2 О ↔ Н 2 СО 3

Получение угольной кислоты и исследование её свойств
СО 2 + Н 2 О ↔ Н 2 СО 3
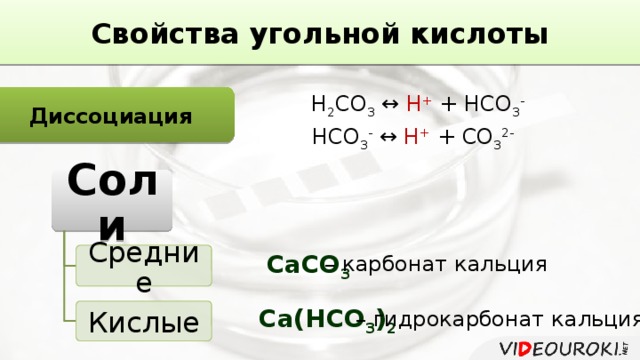
Свойства угольной кислоты
Диссоциация
Н 2 CO 3 ↔ H + + HCO 3 -
HCO 3 - ↔ H + + CO 3 2-
Соли
СаСО 3
Средние
– карбонат кальция
Са(НСО 3 ) 2
Кислые
– гидрокарбонат кальция

Соли угольной кислоты
- В воде растворимы только карбонаты калия, натрия и аммония .
- Карбонаты других металлов нерастворимы в воде .
- При нагревании эти карбонаты разлагаются на оксид металла и углекислый газ.
t
MgCO 3 = MgO + CO 2 ↑
в воде.
t
CaCO 3 = CaO + CO 2 ↑
t
(NH 4 ) 2 CO 3 = 2NH 3 ↑ + CO 2 ↑ + H 2 O
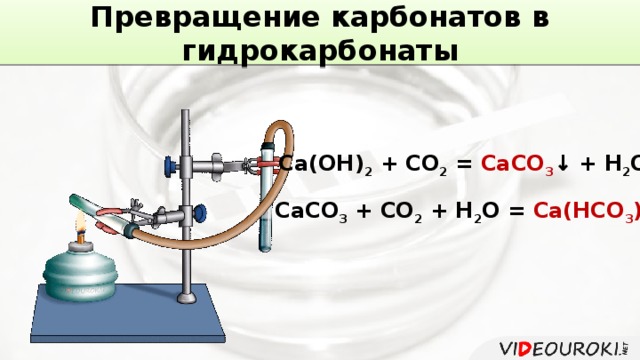
Превращение карбонатов в гидрокарбонаты
Ca(OH) 2 + CO 2 = CaCO 3 ↓ + H 2 O
CaCO 3 + CO 2 + H 2 O = Ca(HCO 3 ) 2

Жёсткость воды
Жёсткость воды
Временная
Ca 2+
HCO 3 -
Mg 2+
Постоянная
t
Ca(HCO 2 ) 2 = CaCO 3 ↓ + H 2 O + CO 2 ↑

Образование накипи на стенках котлов,
чайников, труб парового отопления.

Сталактиты и сталагмиты

Жёсткость воды
Жёсткость воды
Mg 2+
Временная
Ca 2+
Cl -
SO 4 2-
Постоянная
Na 2 CO 3
сода
CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl

Качественные реакции на карбонаты и гидрокарбонаты
CO 3 2- + 2H + = H 2 O + CO 2 ↑
HCO 3 - + H + = H 2 O + CO 2 ↑

Применение солей угольной кислоты
Na 2 CO 3 · 10H 2 O
кристаллическая сода
Na 2 CO 3
кальцинированная сода

Её добывали из содовых озёр и извлекали из месторождений.
Сода была известна человеку примерно за 1,5 – 2 тыс. лет до н. э.
Первые сведения о получении относятся к 64 г. н. э.
Диоскорид Педания

Применение солей угольной кислоты
NaHCO 3
питьевая сода
K 2 CO 3
поташ

Применение солей угольной кислоты
СаСО 3
известняк,
или мрамор

Выводы
- Угольная кислота – это двухосновная слабая неустойчивая кислота.
- Угольная кислота образуется при растворении в воде углекислого газа .
- Она диссоциирует по двум ступеням .
- Угольная кислота образует два типа солей – карбонаты и гидрокарбонаты .
- Карбонаты многих металлов нерастворимы в воде и при нагревании разлагаются, а гидрокарбонаты – это растворимые соли .

Выводы
- Карбонаты можно перевести в гидрокарбонаты и наоборот: для перевода карбоната в гидрокарбонат через карбонат пропускают углекислый газ в воде, а при нагревании гидрокарбонатов образуются карбонаты.
- Качественными реакциями на карбонат и гидрокарбонат-ион является действие кислот на эти соли, при этом наблюдается бурное выделение углекислого газа.
- Различают временную и постоянную жёсткость.
- Временная жёсткость обусловлена наличием гидрокарбонатов кальция и магния и устраняется кипячением , постоянная жёсткость обусловлена наличием других солей кальция и магния , а устраняется добавлением соды.
- Карбонаты и гидрокарбонаты многих металлов находят широкое применение во многих отраслях народного хозяйства.









































