| Этапы урока, время | Деятельность учителя | Деятельность учащихся |
| 1. Организационный, 1-2 мин. | Проверка готовности к уроку |
|
| 2. Проверка домашнего задания, 7 мин. | На предыдущем уроке мы научились решать задачи на определение молекулярной формулы вещества. Что нужно знать для решения таких задач? Задача 1. Определите формулу соединения, имеющего состав: К – 39,7%, Mn – 27,9%, O – 32,4%. Это вещество называется манганат калия, на вид - порошок черно-зеленого цвета (демонтрация вещества) | 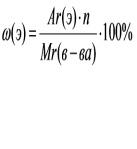
Решают задачу. Ответ K2MnO4 |
| 3. Актуализация, систематизация знаний, 3 мин. | Перед вами формулы веществ. Найдите общее в этих формулах | 1. Все они состоят из двух видов атомов (бинарные) 2. В их состав входит водород. |
| 2. Атомы в веществе располагаются не как придется, их расположение строго определено химической связью. Давайте предположим, что атом водорода может образовать одну химическую связь. Нарисуйте с помощью черточек, как соединены атомы в этих веществах. Такую форму записи вещества называют графической формулой | 2. Составляют формулы (1 учащийся у доски)
H-Cl, H-S-H и.п. |
| О составе вещества и его формуле можно судить, зная закономерности соединения атомов. | Записывают в тетрадь |
| 4. Изучение нового материала, 25 мин. | Такую закономерность называют ВАЛЕНТНОСТЬЮ. Это тема нашего урока. Придумайте определение валентности. | Записывают тему в тетрадь. Это количество химических связей, которые может образовать атом химического элемента с другими атомами. |
|
| Найдите в тексте учебника определение валентности, прочитайте, есть ли вопросы? Запишите определение в тетрадь | Работа с учебником. Записывают определение. |
| Чему равна валентность углерода на ваших схемах? Чему равна валентность остальных элементов? Чтобы узнать валентность элемента у вас в учебнике есть таблица 3. Ознакомьтесь с ней. Что вы можете сказать о валентности элементов? | Валентность водорода = 1 С-4, P – 3, S – 2, Cl – 1
Валентность одних элементов постоянна, у других – нет. |
| Определите валентность для веществ из предыдущего задания, используя табл.3. Обозначьте валентность римской цифрой над знаком элемента. | Работа с учебником, выполняют задание в тетради (1 уч-ся у доски) |
| Сегодня мы научились определять валентность. Найдите закономерности при ее определении.
Посчитайте количество единиц валентности для каждого элемента в соединениях. Какую вы видите закономерность?
Запишите эти закономерности в тетрадь и запомните их. Это очень важно. | 1.За единицу валентности принята валентность атома водорода 2.Сколько связей может образовать атом, такова его валентность 3.Значение валентности обозначается римскими цифрами НАД символом химического элемента В бинарном соединении число единиц валентности одного элемента равно числу единиц валентности другого элемента |
| Закрепление, 5 мин. | Решите задачи: 1. Среди формул выберите формулы бинарных соединений и определите валентность элементов, используя таблицу 3 (стр.56) K2MnO4 , ZnS , CaO , Cl2O5 , SiO2 , HClO4 (слайд) 2. Распределите формулы веществ по группам, согласно валентности образующих их элементов ZnO, P2O5, CaO, Fe2O3 , HCl и т.д. (слайд)
|
Ответ ученика: ZnS , CaO , Cl2O5 , SiO2
Ответ ученика. |
| Подведение итогов, Выставление оценок Домашнее задание, 2 мин. | -Что важного мы узнали на уроке? Было ли что-то для вас трудным? Домашнее задание. §16, №3-5 письменно
| На сегодняшнем уроке вы изучили валентность, научились составлять формулы веществ. |

























