ВСЕРОССИЙСКАЯ ПРОВЕРОЧНАЯ РАБОТА
ХИМИЯ
11 КЛАСС
Инструкция по выполнению работы
Проверочная работа включает в себя 15 заданий. На выполнение работы по химии отводится 1 час 30 минут (90 минут).
Оформляйте ответы в тексте работы согласно инструкциям к заданиям. В случае записи неверного ответа зачеркните его и запишите рядом новый. При выполнении работы разрешается использовать следующие дополнительные материалы:
– Периодическая система химических элементов Д.И. Менделеева;
– таблица растворимости солей, кислот и оснований в воде;
– электрохимический ряд напряжений металлов;
– непрограммируемый калькулятор.
При выполнении заданий Вы можете использовать черновик. Записи в черновике проверяться и оцениваться не будут. Советуем выполнять задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, Вы сможете вернуться к пропущенным заданиям.
Баллы, полученные Вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
Желаем успеха!
ВАРИАНТ 2.
1.Из курса химии Вам известны следующие способы разделения смесей: отстаивание, фильтрование, дистилляция (перегонка), действие магнитом, выпаривание, кристаллизация. На рисунках 1–3 представлены примеры использования некоторых из перечисленных способов.


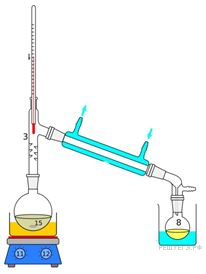
Какие из названных способов разделения смесей можно применить для очищения:
1) этанола и воды;
2) воды и песка?
Запишите в таблицу номер рисунка и название соответствующего способа разделения смеси.
| Смесь | Номер рисунка | Способ разделения смеси |
| Этанол и вода | 
| 
|
| Вода с песком | 
| 
|
2.На рисунке изображена модель электронного строения атома некоторого химического элемента.
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
Ответы запишите в таблицу.
| Символ химического элемента | № периода | № группы | Металл/неметалл |
| 
| 
| 
| 
|
3.Известно, что с увеличением порядкового номера элемента в периодах металлические свойства атомов уменьшаются, а в группах увеличиваются. Расположите в порядке увеличения металлических свойств, следующие элементы: С, Ca, B, Al
![]() Запишите обозначения элементов в нужной последовательности. В ответе укажите обозначения элементов разделяя - . Например, 11 - 22.
Запишите обозначения элементов в нужной последовательности. В ответе укажите обозначения элементов разделяя - . Например, 11 - 22.
4. В приведённой ниже таблице перечислены характерные свойства веществ, которые имеют молекулярное и ионное строение.
Характерные свойства веществ
| Молекулярного строения | Ионного строения |
| — при обычных условиях имеют жидкое, газообразное и твёрдое агрегатное состояние; — имеют низкие значения температур кипения и плавления; — неэлектропроводные; — имеют низкую теплопроводность | — твёрдые при обычных условиях; — хрупкие; — тугоплавкие; — нелетучие; — в расплавах и растворах проводят электрический ток |
Используя данную информацию, определите, какое строение имеют вещества водород H2 и соль нитрат калия KNO3![]()
Запишите ответ в отведённом месте:
1) водород H2 
2) соль нитрат калия KNO3![]()

5.Вещества имеют названия в соответствии с международной номенклатурой. В эту схему для каждого из четырёх веществ впишите пропущенные названия солей или химические формулы.

Прочитайте следующий текст и выполните задания 6—8.
Диоксид серы — это очень распространённая добавка, используемая в пищевой промышленности. На этикетках её можно обнаружить как E220, а сам консервант образуется в результате сжигания серы. Данное вещество можно встретить почти везде: фрукты и овощи (консервированные, сушёные, замороженные). Чтобы избавиться от плесени и грибка с целью обеззараживания складов, погребов, теплиц, иногда используют окуривание помещений сернистым газом (оксид серы(IV)). Для этого в помещении поджигают серу. Однако сернистый газ для обработки погреба можно получить взаимодействием сульфита натрия с раствором серной кислоты. Иногда для этих целей смешивают сульфит кальция с раствором соляной кислоты.
6. 1. Составьте молекулярное уравнение реакции получения сернистого газа, которая первой упоминается в тексте.
2. Объясните, какие, по Вашему мнению, свойства оксида серы(IV) позволяют использовать его как консервант.
7
1. Составьте молекулярное уравнение реакции между сульфитом натрия и соляной кислотой.
2. Объясните, какие особенности сернистой кислоты позволяют использовать эту реакцию для получения сернистого газа.
8
1. Составьте сокращённое ионное уравнение упомянутой в тексте реакции между сульфитом натрия и серной кислотой.
2. Объясните, почему такая реакция возможна.
9. Дана схема окислительно-восстановительной реакции: P + KClO3= P2O5+ KCl ![]()
![]() 1. Составьте электронный баланс этой реакции.
1. Составьте электронный баланс этой реакции.
2. Укажите окислитель и восстановитель.
3. Расставьте коэффициенты в уравнении реакции.
10. Дана схема превращений: Mg → MgCl2 → Mg(OH)2 → MgSO4
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения.
11.Установите соответствие между формулой органического вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | | КЛАСС/ГРУППА |
| А) С6Н7N ![]() Б) С3Н7NO2 В) С2Н7N | | 1) ароматические амины 2) предельные амины 3) предельные двухатомные спирты 4) аминокислоты ряда глицина |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
12. В предложенные схемы химических реакций вставьте формулы пропущенных веществ и расставьте коэффициенты.
1) CH3CH2OH + …… → CH3COH + …… + Cu 2) C2H6 + …. → С2Н5Cl + ……
13. Этиловый спирт используется в производстве бутадиенового каучука по способу С. В. Лебедева, при получении душистых веществ, в качестве растворителя, в производстве лекарственных препаратов, то есть находит широкое применение. Сколько граммов глюкозы минимально необходимо для получения 115 г этилового спирта? Запишите подробное решение задачи.
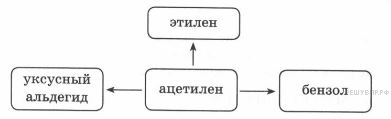
14.Ацетилен используется для получения разнообразных органических веществ и в качестве топлива. В соответствии с приведённой ниже схемой составьте уравнения реакций получения некоторых веществ, используя ацетилен как исходное вещество. При написании уравнений реакций используйте структурные формулы органических веществ.
15. K 150 г 8 %-ного раствора нитрата натрия добавили некоторое количество соли и получили раствор с массовой долей соли 20%. Рассчитайте массу добавленного нитрата натрия и массу полученного раствора. Запишите подробное решение задачи.


































