| Актуализация знания, целеполангание
Время: 7 мин
Этапы: 3 | 1.Этап актуализации знания Предлагает определить тему урока, цели и задачи урока, актуальность темы. Организует деятельность по актуализации понятий «аминокислоты», «функциональные группы», «заменимые аминокислоты», «незаменимые аминокислоты», «белки», «биополимеры», «карбоксильная группа. Проводит фронтальный опрос: - Вспомните, какую тему вы изучали на прошлом уроке? - Какое строение имеют АК? Из каких функциональных групп состоят? (демонстрация строения АК)
- Среди аминокислот есть заменимые, они могут синтезироваться в организме и незаменимые. Проводит демонстрацию компьютерных моделей аминокислот аланина и валина, не называя их: - Определите модели каких аминокислот представлены на экране? Как вы это определили?
- Отлично! Теперь вспомните, каким очень важным в биологическом цикле свойством обладают аминокислоты? - Верно! Между АК образуется пептидная связь. Но как вы думаете, такая связь может образовываться только между 2-мя АК с образованием дипептида, или эта цепь может быть больше? Внимание на экран (демонстрация модели процесса образования полипептида - белков) - Как думаете, что из себя представляют такие длинные цепи из последовательно располагающихся АК? 2. Этап целеполагания. Я хотела бы продолжить наш урок словами Фридриха Энгельса: «Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка». ( К. Маркс, Ф.Энгельс. Собрание сочинений. Т.20). - Догадались, какая тема урока? Сформулируйте цель урока. | Отвечают на вопросы фронтального опроса.
Предполагаемые ответы:
- Аминокислоты
- Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
Изучают компьютерные модели аминокислот, угадывают их название по их модели:
- Аланин и фенилаланин. По функциональным группам и соответствующим радикалам
- способностью образовывать пептидную связь
- нет, может быть больше
- полипептиды или белки
Отгадывают тему урока, формируют цель совместно с учителем. | - давать определение понятиям, - осуществлять сравнение и классификацию, - строить логические рассуждения, - устанавливать межпредметные связи, - анализировать объекты с выделением существенных и несущественных признаков. - осознанно и произвольно строить речевые высказывания
| Личностные: - установление учащимися связи между целью учебной деятельности и её мотивом.
Регулятивные: - саморегуляция и самоорганизация
Коммуникативные: - участие в коллективной работе;
Познавательные: - Давать определение понятиям, обобщать понятия; делать выводы. - Осознанно и произвольно строить речевые высказывания.
|
| Основная часть
Время: 25
Этапы:3
| Этап планирования и первичного усвоения материала. Вместе с учениками составляют план изучения белков. План 1. Определение 2. Состав и строение 3. Классификация 4. Химические свойства белков. 6. Тестирование.
1. Определение белка. Давайте попробуем дать определение белкам. В начале урока мы с вами уже говорили про образование дипептидной и возможному образованию полипептидной связи. Поэтому белки по – другому называют пептидами.
- Давайте запишем сформулируем и запишем определение белка.
- Назовите известные Вам белки и запишите пару примеров.
2. Строение и состав. - В природе существует около 100 аминокислот, в организме встречается 25. Но в каждом белке 20, из них может быть образовано 2 432 902 008 176 640 000 комбинаций, т. е. различных белков, которые будут обладать совершенно одинаковым составом, но различным строением - Как из 20 аминокислот получаются миллионы белковых молекул? - Какие химические элементы входят в состав белков?
- Давайте вспомним из биологии, сколько структур имеет белок. Структура белка (пользуемся материалом комьютерной модели организации структур белка). Составляем схему уровни организации белка. Вопросы по повторению строения белков 1. Кто хочет показать как образуется 1 структура белка. Напишите трипептид гли-ала-вал? (формулы АК выведены на экран для подсказки) Давайте с вами попробуем ответить на вопросы? 1. Чем отличается вторичная структура белка от первичной? 2. За счет чего удерживается форма молекулы белка во вторичной структуре? 3. В чем отличие третичной структуры белка от первичной и вторичной? 4. Какая структура является самой прочной? Почему?
3.Классификация белков. - Сложность строение белковых молекул и чрезвычайная разнообразие их функций крайне затрудняет создание классификации белков на какой – либо одной основе. Принято выделять несколько классификаций белков (проецирование схемы на экран). - На основании какого свойства белки классифицируются?
4.Физкультминутка для глаз.
5. Химические свойства белков. - Для раскрытия природы белка изучим его свойства.
Для белков характерны следующие химические свойства. 1) гидролиз (при нагревании с растворами кислот, щелочей, при действии ферментов)- происходит разрушение 1 структуры с образованием АК. Как вы думаете, в организме человека и животных происходит гидролиз белков ()? 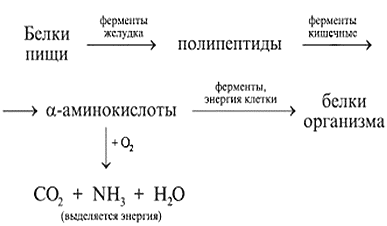
Это интересно: Зачем маринуют мясо?
2) денатурация Связи, поддерживающие 2,3 если есть 4 структуру белка, относительно легко разрушаются, под действием нагревания, механического действия и химических реагентов. нарушение природной структуры белка - денатурация. 1 структура и химический состав сохраняются. Поэтому денатурация может быть обратимой: при условии достаточно быстрого устранения фактора, ее вызвавшего, происходит восстановление пространственной сруктуры белка – ренатурация. Живой организм находится постоянно под воздействием внешних факторов, способных вызвать денатурацию белка. Запомните: как можно меньше контакта с солями, содержащими ионы Pb2+, Сu2+, Нg2+ и др. Не только тяжелые металлы могут влиять на состояние здоровья человека, но и радиоактивность, как особый тип загрязнения окружающей среды. Мы должны приложить все силы к тому, чтобы оставить чистыми почвы и воды нашим потомкам. Не менее губительное действие на живой организм оказывают и органические вещества, например этанол. О вреде алкоголя необходимо не только знать, но и запомнить на всю жизнь.
Таким образом, денатурация белка в организме может привести к: 1. Нарушение обмена веществ. 2. Воспаление слизистой оболочки органов пищеварения 3. Камнеообразование (камни имеют белковую основу).
3. Амфотерность (содержат большое число способных к диссоциации карбоксильных и аминогрупп). Белок состоит из АК, а вы знаете. что АК состоят из каких функциональных групп (СООН- и NН2-) ведут себя как кислоты и как основания. Как мы называем такие соединения?
4) цветные реакции белков – качественные реакции на белки? а) ксантопротеиновая реакция. Белок + HNO3 конц. → желтое окрашивание б) биуретовая реакция. Белок + Cu(OH)2↓ → раствор фиолетового цвета.
- Давайте сделаем небольшой вывод: какие реакции на белки являются качественными?
Этап первичного закрепления материала: Выполните тест (индивидуальная работа). 1. Сколько аминокислот участвуют в образовании белков? 1) 30 2) 20 3) 26 4) 10 2. На каком рисунке изображена вторичная структура белка: 1. 2. 3. 4. 3. Пептидная (ковалентная) связь образует: Первичную структуру белка; Вторичную структуру белка; Третичную структуру белка; Четвертичную структуру белка. 4. Денатурация происходит под действием: Химических реагентов; Механического действия; Нагревания; Спиртных напитков. Белки обладают Кислотными свойствами; Основными свойствами; Двойственной природой; Амфотерными свойствами.
Выполни самопроверку | Вместе с учителем составляют план изучения белков.
Ученики дают определение белкам. Белки – это высокомолекулярные нерегулярные полимеры, мономерами будут АК. Пептидной. кератин – рога, шерсть коллаген – кожа гемоглобин – кровь фибрин – кровь пепсин – желуд.сок трипсин – поджелуд сок миозин – мышцы глобулин – вакцина инсулин – подж. железа казеин – молоко альбумин – яичный белок
- Явление изомерии
- В белке содержатся следующие химические элементы: С, Н, О, N, S, P, Fe. Железо в гемоглобине крови, фосфор в казеине молока. Незначительное количество меди, кальция, цинка, брома, йода.
Изучают структурную организацию белка по компьютерной модели, составляют схему.
Работают у доски.
Отвечают на вопросы.
- большая компактизация за счет обр-я Н-связи - Н-связи
- Компактизация молекулы - третичная
Помечают в тетради схему
Отвечают на вопросы: по форме белка.
Выполняют физкультминутку
Да, под влиянием ферментов образующиеся аминокислоты попадают в кровь и далее поступают в клетки организма, где образуются необходимые организму белки. Часть аминокислот подвергается окислению и распаду, в результате чего образуется аммиак, углекислый газ и вода. Аммиак превращается в мочевину и выводится из организма.
Ответы обучающихся: Под воздействием уксусной кислоты или лимонной происходит частичный гидролиз белков. Белки распадаются на поли – и дипептиды. В желудке под влиянием ферментов этот процесс продолжается и в итоге приводит к образованию аминокислот. Таким образом, маринование облегчает переваривание белка. Гидролиз белков сводится к гидролизу полипептидных связей. К этому же сводится и переваривание белков: Белки + Н2О — полипептид + Н2О — дипептиды + вода — α-аминокислоты→ кровь во все клетки и ткани организма.
Записываю свойства амфотерности
- амфотерные
Качественными называют реакции, с помощью которых можно определить вещества разных классов. Пишут качественные реакции.
- качественными на белки являются реакции с концентрированной азотной кислотой (желтое окрашивание), со свежеосажденным гидроксидом меди (II) (раствор фиолетового цвета)
- Выполняют тест, по завершении осуществляют самопроверку по образцу на слайде | - Знать понятие «белки» - знать структуру белковой молекулы, понятие пептидной связи - знать уровни организации белковой молекулы - знать основные химические свойства белков и качественные реакции на белки - уметь интерпретировать информацию представленную в различной форме (структурные формулы, схемы, компьютерные модели молекул и химических процессов)
| Личностные: - адекватное понимание причин успешности/неуспешности учебной деятельности;
Регулятивные: - Планировать учебную деятельность в соответствии с учебным заданием. - умение сосредоточиться, анализировать, проявить настойчивость, умение преодолеть импульсивность.
Познавательные: - умение осознанно построить речевое высказывание; - умение самостоятельно осознанно выполнить задание.
Коммуникативные: - Организовывать учебное сотрудничество и совместную деятельность с учителем и одноклассниками. - Устанавливать рабочие отношения в классе, планировать общие способы работы. - Строить понятные для собеседника речевые высказывания, уметь слушать собеседника, адекватно и осознанно использовать устную и письменную речь, владеть монологической контекстной речью
|
| Итог урока Время: 5 мин Этапы : 2 | Подводит итоги. Выставляет оценки. Проводит рефлексию. - Мы закончили изучение белков. Вам я предлагаю совершить “Подъем по лестнице знаний”, составив синквейн о белках (парная работа). Одно существительное, выражающее главную тему синквейна. Два прилагательных, выражающих главный смысл. Три глагола, описывающее действие в рамках темы. Фраза несущая определенный смысл (высказывают своё отношение к теме). Заключение в форме существительного (ассоциация с первым словом). Рефлексия Оцените как изменились за урок ваши знания? Выберите стикер и приклейте в тетрадь напротив темы урока. Зеленый – у меня все получилось, я все понял. Желтый – трудно сказать, не все понял, что-то понял, что-то нет. Красный – было скучно, я ничего не выполнил. С каким настроением вы уходите с урока? Понравился ли вам урок? Инструктаж домашнего задания - повторить конспект. - многие белковые тела способны обугливаться в сильных кислотах. У вас на столах есть памятки. Выполните этот виртуальный эксперимент, следуя указаниям. - Вот и подошел к концу наш с вами урок. Надеюсь, ваш багаж знаний пополнился еще одной темой. Спасибо за урок. До свидания! | Несколько учеников зачитывают свой синквейн. 1. Белки 2. Глобулярные, фибриллярные 3. Защищают, регулируют, катализируют. 4. Мономерами являются аминокислоты. 5. Жизнь.
Выполняют рефлексию, делятся впечатлениями
Записываю ДЗ, задают вопросы |
| Личностные: - адекватное понимание причин успешности /неуспешности учебной деятельности; - умение установить связь между результатом учебной деятельности и тем, ради чего она осуществлялась.
Регулятивные: - умение провести самоорганизацию по завершении урока ; Коммуникативные: - Строить понятные для собеседника речевые высказывания, уметь слушать собеседника, адекватно и осознанно использовать устную и письменную речь, владеть монологической контекстной речью
Познавательные: - умение провести рефлексию деятельности на уроке |


























