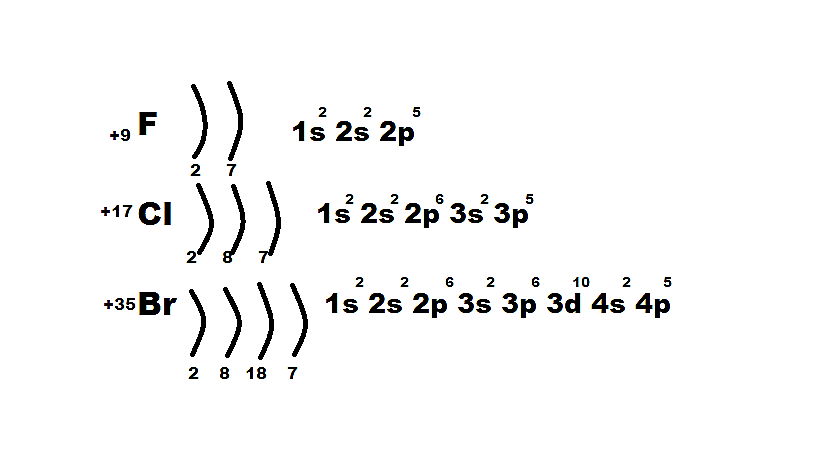СЦЕНАРИЙ ОТКРЫТОГО УРОКА
по химии в 9-м классе на тему:
«ОБЩАЯ ХАРАКТЕРИСТИКА ГАЛОГЕНОВ»
Цель урока: Дать общую характеристику галогенов и рассмотреть их физические и
химические свойства.
Задачи урока: 1) Продолжить формирование умений сравнивать свойства простых
веществ;
2) Закрепить общие представления о неметаллах и их свойствах;
3) Развивать умения и навыки в решении задач и составлении уравнений
Химических реакций с участием неметаллов.
Тип урока: урок усвоения новых знаний
Методы урока: беседа, рассказ, самостоятельная работа
Оборудование: Периодическая система химических элементов Д.И. Менделеева,
мультимедийная система, компьютер.
ХОД УРОКА:
Организационный момент. (1-2 мин)
Приветствие друг друга, настрой на работу, сообщение темы и целей сегодняшнего урока.
Проверка домашнего задания. (10-12 мин)
Вызвать 3 человека к доске: 1 решает цепочку по середине доски,2-е за досками решают задачи:
Цепочка превращений:
Н2 → NaH → Н2 → HCl
NaOH
H2 + 2Na = 2NaH
NaH + HCl = NaCl + H2↑
H2 + Cl2 = 2HCl
NaH + H2O = NaOH + H2↑
2NaOH + 2Al + 6H2O = 2Na[Al(OH)4] +3H2↑
Задача №2 с.93
![]()
Дано: Решение:
V( возд.)=100 л V(O2)= V( возд.)* ᵠ (O2)= 100*0,21=
ᵠ (O2)=21% 21 л.

ᵠ (N2) =78% n (O2)= V/ Vm = 21л / 22,4 л/моль = 0,94 моль
n (O2)=? V(N2) = 100*0,78 = 78 л
n (N2) =? n (N2)=78л / 22,4л/моль = 3,48моль
Ответ: 0,94 моль, 3,48 моль.
Задача №3 с.103
![]()
Дано: Решение:
mтех.(WO3) =928 кг W(WO3) = 100%-25%=75%

W(примес.) = 25% m (WO3) = mтех. * W (WO3) =
V(H2)=? 928кг * 0,75 = 696 кг
n(W)=? n(WO3)=m/M=696кг/232кг/кмоль = 3 кмоль
WO3 + 3Н2 = W + 3Н2О
1 моль 3моль 1моль
3 кмоль 9 кмоль 3 кмоль
V(H2)= nVm = 9 кмоль * 22,4 м3/кмоль = 201,6 м3
Ответ: 201,6 м3, 3 кмоль.
Все остальные пишут тест: выбрать номера свойств и характеристик для (1 вариант) металлов, для (2 вариант) неметаллов:
Маленький радиус атомов
Большой радиус атомов
На внешнем уровне от 1 до 3 электронов
На внешнем уровне от 4 до 8 электронов
Ковкость
Металлический блеск
Газообразное агрегатное состояние
Пластичность
Различная окраска
Плохая электропроводность
Твердое агрегатное состояние
Хорошая теплопроводность
Хорошая электропроводность
Ярко выраженные восстановительные свойства
Ярко выраженные окислительные свойства
Аллотропия
Правильные ответы: 1вариант – 2,3,5,6,8,11,12,13,14
2 вариант – 1,4,7,9,10,11,15,16
Изучение нового материала. (20 мин)
Положение в ПСХЭ и строение их атомов.
Галогены F, Cl, Br, I, At – элементы 7 группы главной подгруппы Периодической системы хим. элементов.
на внешнем уровне 7 электронов;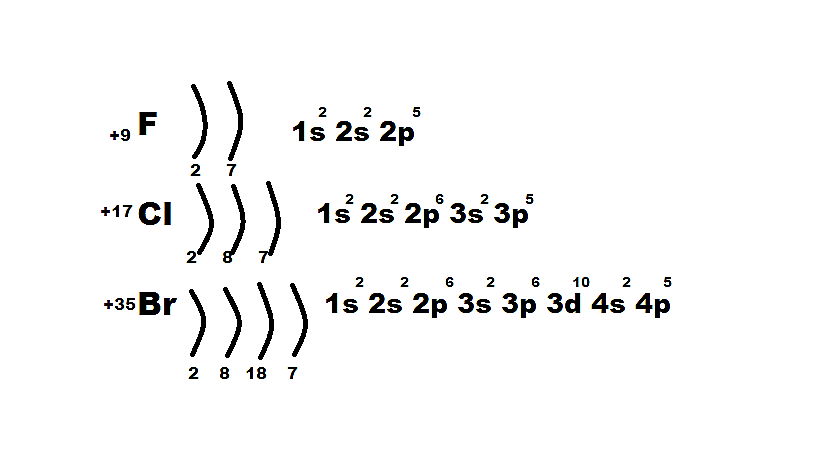
увеличивается радиус атомов;
ослабевают неметаллические свойства;
окислительная способность уменьшается.
Фтор – самый сильный окислитель (с.о.-1)
У остальных: с.о. -1, +1, +3, +5, +7
П
Помимо фтора, хлора, брома и йода в этой группе есть еще один элемент, относящийся к галогенам – это астат. Он был предсказан самим Д.И. Менделеевым как эка-йод, он является радиоактивным элементом, поэтому в школьном курсе не изучается.
Галогены - простые вещества и нахождение их в природе.
Заслушивание сообщений о фторе, хлоре броме и йоде. (4 человека, ориентируясь на слайды презентации, рассказывают о галогенах, истории их открытия, о соединениях, в которых они встречаются в природе) Остальной класс кратко конспектируют за докладчиками.
Химические свойства галогенов.
Взаимодействие с простыми веществами:
а) с водородом Н2
Н2 + Г2 = 2НГ
Фтор взаимодействует с водородом в любых условиях со взрывом, хлор – со взрывом только при поджигании или облучении прямым солнечным светом, бром реагирует с водородом только при нагревании и без взрыва. Эти реакции экзотермические, реакция же йода с водородом слабо эндотермическая, она протекает медленно даже при нагревании.
б) с металлами – образуются соли – галогениды металлов.
Так фтор уже при обычных условиях реагирует с большинством металлов, а при нагревании реагирует даже с Au, Ag и Pt, известными своей химической пассивностью.
Остальные галогены реагируют с металлами в основном при нагревании. Так, в колбе, наполненной хлором, красиво вспыхивают и сгорают кристаллики измельченной сурьмы:
2Sb + 3Cl2 = 2SbCl3 (просмотр видеофрагмента опыта сурьмы с хлором)
2Sb + 5Cl2 = 2SbCl5
Самостоятельное задание – написать уравнения реакций взд-я железа с хлором, меди с бромом.
2. Взаимодействие со сложными веществами:
а) с водой
2F2 + 2H2O = 4HF + O2
б) с галогенидами металлов (искл. составляет фтор, который в первую очередь взаимодействует с водой)
Cl2 → Br2 → I2
окислительная способность уменьшается от хлора к йоду:
Cl2 + 2NaBr = 2NaCl + Br2
Br2 + 2KI = 2KBr + I2
Закрепление. (5мин.)
Ответить на 5 тестовых вопросов по изученной теме (см.слайды презентации)
Анализ оценок за урок. (1мин.)
Оценить отвечавших у доски д/з, выступавших с сообщениями о галогенах.
Домашнее задание: (1мин.)
Параграф 18, задания после него №4,5
Параграф 20, задание после него №1