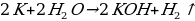| Окутуунун максаттары (ТК) Сабактын аягында окуучулар төмөндөгүдөй жөндөмгө ээ болушу керек: а) Щелочтуу металлдардын жалпы мүнөздөмөсүн жана алардын алынышын үйрөнүшөт. б) Натрий жана калийдин физикалык жана химиялык касиеттерин салыштырып, химиялык тажрыйба жасап, өз билимдерин өркүндөтүшөт. в) Щелочтуу металлдардын кеңири колдонулушун билишет жана турмушта маанилүү экенин түшүнүшөт.
| 1. Окуу китеби (СБ) 2.Практикалык эмгек китеби (ПБ) 3.Теориялык эмгек китеби (TWB) |
| 5-мин | 1-С: Кызыгууну ойготуу |   Кайсы металлдар суу менен бат реакцияга кирет? Аш тузунун курамында кайсы металл бар? Кайсы металлдарды керосиндин же майдын ичинде сакташат? Жер семирткичтердин курамында кайсы металл бар? Щелочтуу металлдар — элементтер мезгилдик системасы I группа негизги группа түзгөн хим. элементтер: литий (ат. н. 3) Li, натрий (11) Na, калий (19) К, рубидий (37) Rb, цезий (55) Сs, франций (87) Fr, Li 1817-ж Арфедсон, Nа менен Сs 1861-ж. Бунзен, Fi 1939-ж М. Пере тарабынан ачылган. | НК1 НК2 |
| 5-мин | 2-С: Түшүнүктү калыптандыруу | Суу менен аракеттенишип, щелочторду–сууда эрүүчү негиздерди пайда кылгандыгы үчүн щелочтуу металлдар деп аталат. Бардык щелочтуу металлдардын S –электрондук катмарында 1Е болот, ошондуктан калыбына келтиргичтер катары металлдык касиеттерди алып жүрɵт, кычкылдануу даражасы +1 барабар, I валенттүү болот. 
Жаратылышта кездешүүсү: Щелочтук металлдар реакцияга активдүү киргендиктен, жаратылышта эркин түрдɵ эмес, туздардын курамында кездешет. Алардын ичинен эң кеңири таралганы NaCl (таш тузу, кайнатма туз, галит) болуп саналат. Ал эми соданы (Na2CO3) адамдар байыртадан эле билишкен. Калий селитрасы (KNO3) мылтыктын дарысынын курамына киргендиктен, адамзаттын тарыхында чоң мааниге ээ болгон. Щелочтуу металлдардын табиятта таралышы: Литий 0,003%, натрий 2,6%, калий 2,4%, рубидий 0,012%, цезий 0,0001%, франций жасалма жол менен алынат. Алынышы: Щелочтук металлдар балкыган хлориддердин же гидроксиддерди электролиздөө жолу менен алынат. 2NaCl Электролиз→ 2Na + Cl2↑, 4NaOH Электролиз→ 4Na + 2H2O + O2↑ 2KCl Электролиз→2K+Cl2↑ 4KOH Электролиз→4K+O2↑+2H2O Физикалык касиеттери: Күмүшкө окшогон боз түстөгү, жумшак, тыгыздыгы төмөн, салыштырмалуу төмөнкү температурада эриген жана кайнаган, жеңил металлдар. Литий (0,53 г/см3) жана натрий (0,97 г/см3) суудан жеңил болот, суу менен реакцияга киргенде анын үстүндө сүзөт. Балкып эрүү температурасы төмөн болот, мисалы, цезий адамдын колунун жылуулугунан эле балкып эрийт. Химиялык касиеттери боюнча алар эң активдүү келишет. Өздөрүнүн ичинен алардын калыбына келтиргич касиети – бир электронду берүү жөндөмдүүлүгү атом радиустарынын чоңоюшуна ылайык литийден францийди көздөй жогорулайт. Li, Na, K, Rb, Cs, Fr ―――――――――→ калыбына келтиргич касиети Щелочтуу металлдар дээрлик бардык металл эместер менен реакцияланышат. Мисалы: 4Na+O2→2Na2O – натрий оксиди 2K+Cl2→2KCl – калий хлориди 2Na+S→Na2S – натрий сульфиди 2К+Н2→2КН – калий гидриди Щелочтуу металлдар суу менен өтө активдүү реакцияга кирет: 2Na+2H2O→2NaOH+H2↑ Щелочтуу металлдар башка активдүү металлдар сыяктуу кислоталардан суутекти бөлүп чыгарат: 2K+2HCl→2KCl+H2↑ Щелочтуу металлдар кычкылтекке күйгөндө литийдин оксиди, ал эми калгандарынан пероксиддери алынат: 2Li+O2→2Li+O – литийдин оксиди, 2Na+O2→Na2O2 – натрий пероксиди Галогендер менен оңой кошулуп, туздарды түзөт: 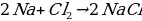 Колдонулушу: Щелочтуу металлдар биздин күнүмдүк жашоодо жана өнөр жайда абдан маанилүү. Литий батареяларда, натрий самында жана айнекте, калий жер семирткичтерде, ал эми цезий так убакыт өлчөөдө негизги ролду ойнойт. Франций болсо сейрек кездешкендиктен, негизинен лабораториялык изилдөөлөрдө гана колдонулат. | ПК1 ПК2 |
| 8-мин | 3-С: Үйрөнүү, билимди чыңдоо, бекемдөө | Күмүш тобу – «Изилдөөчүлөр». Натрий жана калийдин физикалык жана химиялык касиеттерин изилдеп, формула жана реакция мисалдарын тактап чыгуу. Жез тобу – «Илимий журналисттер». Щелочтуу металлдардын турмуштагы колдонулушу боюнча кыскача макала жазып класска окуп берүү. Темир тобу – «Креативдүү дизайнерлер». Илимди турмуш менен байланыштырган “Театр же ролдук оюн” чагылдыруу. | НК1 ПК1 НК2 ПК2 НК3 |
| 5-мин | 1-Е. Байытуу, тереңдетүү | Эксперимент жасоо: Калийдин суу менен болгон реакциясы. Керектелүүчү жабдуулар (приборлор): Петри табагы же айнек идиш, пинцет (кысуучу аспап), лабораториялык бычак (калийди кесүү үчүн), фильтр кагазы (кургатуу үчүн), коргоочу каражаттар (колкап, көз айнек). Реактивтер: Калий (K), суу (H₂O). Калийди сууга салганда ал тез реакцияга кирет: Суунун үстүндө кыймылдайт жана күлгүн жалын пайда болушу мүмкүн. Суутек газы бөлүнөт, калий гидроксиди (KOH) түзүлөт. Теңдемеси: 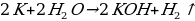 Бул мисал щелочтуу металлдардын абдан активдүү экенин далилдейт. ● Эмне үчүн калий натрийден активдүү? ● Щелочтуу металлдар эмне үчүн керосинде сакталат? ● Реакция учурунда эмне үчүн суутек бөлүнөт?
Окуучулардын алган билимдерин дагы да тереңдетүү, теманы канчалык түшүнгөндөрүн текшерип алуу максатында “Кахуут” платформасын колдонуп, окуучулар тест тапшырышат. https://create.kahoot.it/share/9/e26c014c-f388-456e-93fa-59fac7d1491d | НК1 ПК2 НК2 ПК3
|