Просмотр содержимого документа
«8-синф ХИМИЯ. ИОН БОҒЛАНИШ.»

8-синф ХИМИЯ Мавзу: 53§ Ион боғланиш.
Cl -
С. Шарипов атындагы орто мектептин
химия-биология мугалими Абдирахманов А.

Ҳар қандай молекуладаги атомларнинг бир-бири билан маълум куч орқали боғланиб туриши.
Химиявий боғланиш деганда нимани тушунасиз?

Ион боғланиш
Ион боғланиш назариясини 1916-йили немис олими В.Косиль таклиф қилган. Бу назария бўйича ион боғланиш типга хос металлар билан типга хос металлмаслар ўртасида пайдо бўлади деб тушунтирилади.
Типга хос металлар: Li, K, Na, Rb, Mg, Ca ва б.
Типга хос металлмаслар: F, Cl, Br, I, P, S, N ва б.
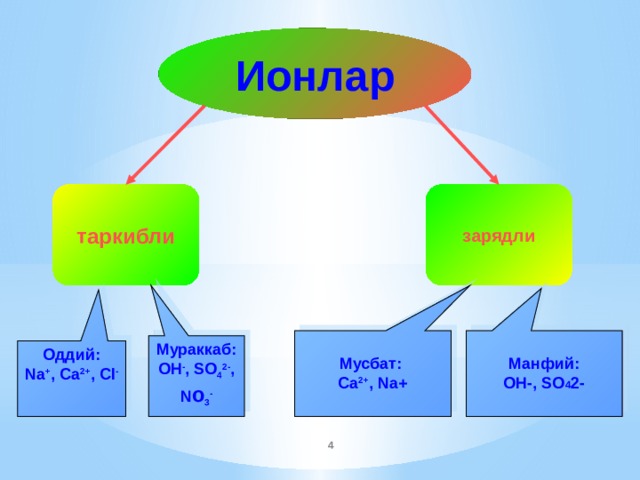
Оддий:
Na + , Ca 2+ , Cl -
Мураккаб:
OH - , SO 4 2- , N o 3 -
Мусбат:
Ca 2+ , Na+
Манфий:
OH-, SO 4 2-
Ионлар
таркибли
зарядли

Ион боғланиш.
- қарама-қарши зарядли ионларнинг электростатик тортишув кучлари воситасида юзага келувчи химиявий боғланишга айтилади – катион ва анион .
Эл 0 – nе - = Эл n+
Эл 0 + nе - = Эл n-
-
-
+
+
-
-
ион-катион
ион-анион

- [
Ион боғланиш механизми
Атомларнинг электрон ва график формулаларининг таркиби:
1s 2 2s 2 2p 6 3s 1
+11 Na
+17 Cl
1s 2 2s 2 2p 6 3s 2 3p 5
3s
3p
2p
3s
2s
2p
1s
2s
1s
Cl -
Na +
Na 0 – 1e - =
Cl 2 0 + 2e - = 2
натрий хлорид
.
.
.
.
.
.
.
.
.
.
.
.
[
.
.
.
.
Na +
+
=
Na
Cl
Cl
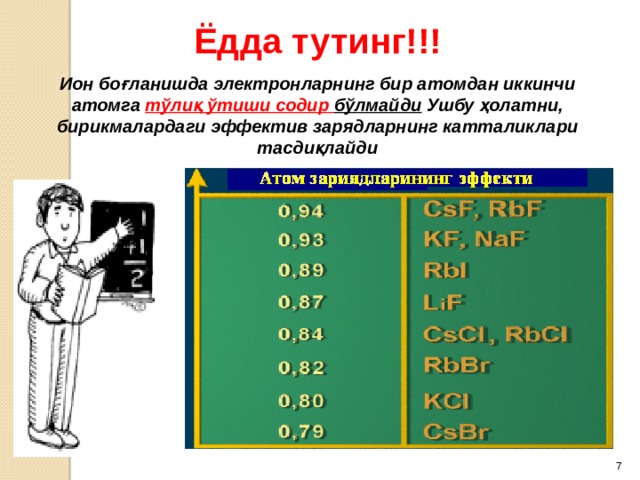
Ёдда тутинг!!!
Ион боғланишда электронларнинг бир атомдан иккинчи атомга тўлиқ ўтиши содир бўлмайди Ушбу ҳолатни, бирикмалардаги эффектив зарядларнинг катталиклари тасдиқлайди

Ион боғланиш хусусиятлари
Cl -
Cl -
K +
Cl -
1. Йўналувчанлик йўқ;
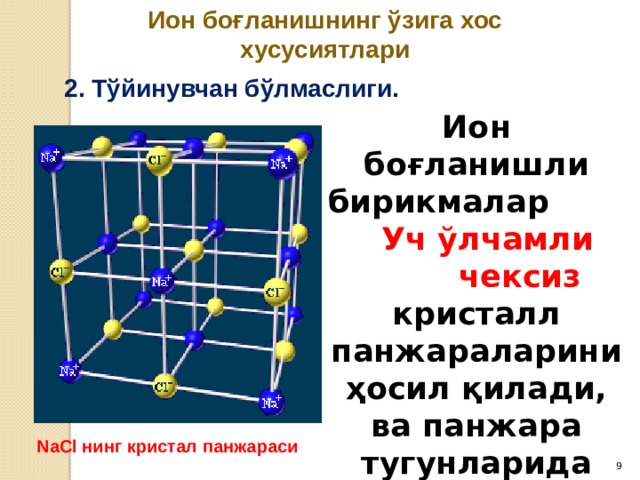
Ион боғланишнинг ўзига хос хусусиятлари
2. Тўйинувчан бўлмаслиги.
Ион боғланишли бирикмалар Уч ўлчамли чексиз кристалл панжараларини ҳосил қилади, ва панжара тугунларида анион ва катионлар жойлашган бўлади.
NaCl нинг кристал панжараси

Уйга вазифа
Реакция тенгламаларини ечинг:
1. NaCl + H 2 SO 4 =
2. Cu(OH) 2 + HNO 3 =
3. K 2 S + HCl =
4. BaSO 4 + HNO 3 =
5. FeCl 3 + Na 2 SO 4 =

ЭЪТИБОРИНГИЗ УЧУН РАҲМАТ!




























