
Окислительно-восстановительные реакции

Окислительно-восстановительными называют химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества.
+1 -1 0 +2 -1 0
2HCl + Zn = ZnCl 2 + H 2

Историческая справка
В XVII в. считали, что окисление – потеря флогистона (особого невидимого горючего вещества), а восстановление – его приобретение. Но после создания А. Лавуазье кислородной теории горения к началу XIX века химики всего мира согласились считать окислением – соединения веществ с кислородом, а восстановлением – их превращения под действием водорода. Однако:
Fe + 2HCI = FeCI 2 + H 2 ↑
Здесь нет кислорода, но железо окисляется. В этой реакции окислитель – ион водорода протон Н+, а железо является восстановителем.

Историческая справка
С введением в химию электронных представлений точно установлено, что окислитель - вещество, которое получает электроны, а восстановитель - вещество, которое их отдает.

Восстановление
Под восстановлением понимают процесс присоединения электронов атомами, ионами или молекулами.
При этом:
- происходит понижение степени окисления какого-либо атома в данной частице;
- частица (атом, ион или молекула) принимает один или несколько электронов;
- органическое вещество теряет атомы кислорода и (или) приобретает атомы водорода.

Восстановление
Например:
- атомы неметаллов могут присоединять электроны, превращаясь при этом в отрицательные ионы, т.е. восстанавливаясь:
0 -1
Cl + 1ē → Cl
атом хлора хлорид-ион
- электроны могут присоединяться к положительным ионам, которые при этом превращаются в атомы:
+2 0
Cu + 2ē → Cu
ион меди( II ) атом меди

Восстановление
- принимать электроны могут и положительные ионы, у которых при этом понижается степень окисления:
+3 +2
Fe + 1 ē → Fe
ион железа ( III ) ион железа ( II )

Окисление
Под окислением понимают процесс отдачи электронов атомами, ионами или молекулами.
В некоторых случаях при окислении молекула исходного вещества может стать нестабильной и распасться на более стабильные и более мелкие составные части. При этом некоторые из атомов получившихся молекул имеют более высокую степень окисления, чем те же атомы в исходной молекуле.

Окисление
Например:
- атомы металлов, теряя электроны, превращаются в положительные ионы, т.е. окисляются:
0 + 1
Na - 1ē → Na
атом натрия ион натрия
- отдавать электроны могут отрицательные ионы :
-1 0
Cl - 1 ē → Cl
хлорид-ион атом хлора

Окисление
- терять электроны могут и некоторые положительные ионы с низшими степенями окисления:
+ 1 +2
Cu - 1 ē → Cu
ион меди (I) ион меди ( II )
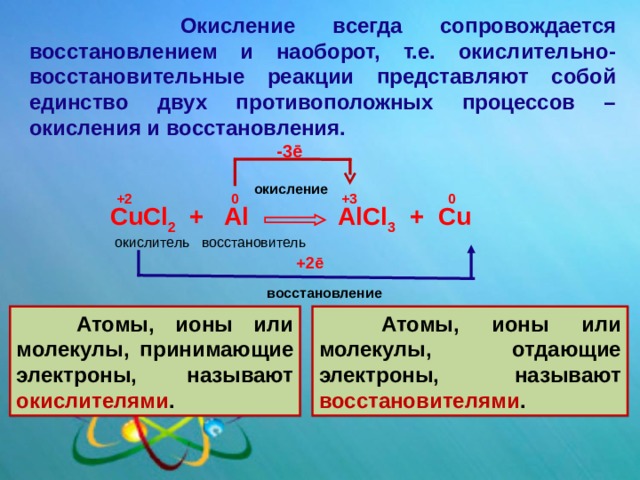
Окисление всегда сопровождается восстановлением и наоборот, т.е. окислительно-восстановительные реакции представляют собой единство двух противоположных процессов – окисления и восстановления.
-3 ē
окисление
+2 0 +3 0
CuCl 2 + Al AlCl 3 + Cu
окислитель восстановитель
+2 ē
восстановление
Атомы, ионы или молекулы, принимающие электроны, называют окислителями .
Атомы, ионы или молекулы, отдающие электроны, называют восстановителями .

Электронный баланс
В окислительно-восстановительных реакциях число электронов, отдаваемых восстановителем, равно числу электронов, принимаемых окислителем, т.е. соблюдается
электронный баланс .
Например, реакция алюминия с хлоридом меди ( II) :
+2 -1 0 +3 -1 0
CuCl 2 + Al → AlCl 3 + Cu

Электронный баланс
А электронные уравнения будут иметь вид:
+2 восстановление 0
Cu + 2ē → Cu 3
0 окисление +3
Al - 3ē → Al 2
Молекулярное уравнение:
3CuCl 2 + 2Al = 2AlCl 2 + 3Cu

Электронный баланс
Для правильного уравнивания следует придерживаться определенной последовательности действий:
1. Найти окислитель и восстановитель.
2. Составить для них схемы (полуреакции) переходов электронов, отвечающие данному окислительно-восстановительному процессу.
3. Уравнять число отданных и принятых электронов в полуреакциях.
4 . Просуммировать порознь левые и правые части полуреакций.
5 . Расставить коэффициенты в уравнении окислительно-восстановительной реакции.
Например:

Электронный баланс
Дана реакция Li + N 2 = Li 3 N
1 . Находим окислитель и восстановитель:
Li 0 + N 2 0 = Li 3 +1 N −3
N присоединяет электроны – окислитель.
Li отдает электроны – восстановитель.
2. Составляем полуреакции :
Li 0 — 1ē = Li +1
N 2 0 + 6ē = 2N −3

Электронный баланс
3. Уравниваем число отданных и принятых электронов в полуреакции:
6* | Li 0 — 1ē = Li +1
1* | N 2 0 + 6ē = 2N −3
Получаем:
6Li 0 — 6ē = 6Li +1
N 2 0 + 6ē = 2N −3

Электронный баланс
4. Просуммируем порознь левые и правые части полуреакций:
6Li + N 2 = 6Li +1 + 2N −3
5. Расставим коэффициенты в окислительно-восстановительной реакции:
6Li + N 2 = 2Li 3 N

Биологическое значение окислительно-
восстановительных процессов
Жизнь – непрерывная цепь
окислительно-восстановительных
процессов
А.-П.Лавуазье

Использованные источники
О.С.Габриелян. Химия. 8 класс. М.Дрофа.2013.
О.С.Габриелян, И.П.Воскобойникова, А.В.Яшукова. Настольная книга учителя. Химия. 8 класс. М. Дрофа. 2012.
Иллюстрация «обмен веществ» (слайд 18):
http://www.med.az/2013/02/01/
Иллюстрация «дыхание» (слайд 18):
http://studiofminus.com/cv/breathing-meditation




































