Просмотр содержимого документа
«Анилин. Получение, свойства, применение.»


Цель урока :
Продолжить изучение аминов на примере анилина ;познакомиться с его строением, свойствами, получением и применением.
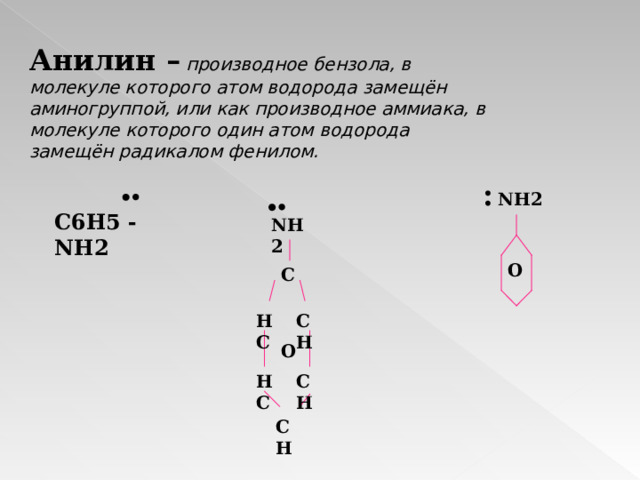
Анилин – производное бензола, в молекуле которого атом водорода замещён аминогруппой, или как производное аммиака, в молекуле которого один атом водорода замещён радикалом фенилом.
NH2
C6H5 - NH2
NH2
O
C
CH
HC
O
CH
HC
CH

Физические свойства
Анилин – бесцветная, маслянистая жидкость со слабым характерным запахом. Он немного тяжелее воды и в ней мало растворим. Но хорошо растворяется в спирте, эфире. В бензоле. Ядовит. Затвердевает при температуре – 6 °C , температура кипения 174 °C .
![Химические свойства 1 Взаимодействие с кислотами С 6 Н 5 N Н 2 + Н CL = [ C 6 H 5 NH 3 ] CL или С 6 Н 5 N Н 2 ⸳ HCL хлорид фениламмония соляно – кислый анилин C 6 H 5 NH 2 HCL + NaOH = C 6 H 5 NH 2 + NaCL + H 2 O 2 Взаимодействие с бромной водой C 6 H 5 NH 2 + 3 Br 2 = C 6 H 2 Br 3 NH 2 + 3HBr](https://static.multiurok.ru/multiurok/html/2022/11/05/s_636693e756e09/img4.jpg)
Химические свойства
1 Взаимодействие с кислотами
С 6 Н 5 N Н 2 + Н CL = [ C 6 H 5 NH 3 ] CL или С 6 Н 5 N Н 2 ⸳ HCL
хлорид фениламмония
соляно – кислый анилин
C 6 H 5 NH 2 HCL + NaOH = C 6 H 5 NH 2 + NaCL + H 2 O
2 Взаимодействие с бромной водой
C 6 H 5 NH 2 + 3 Br 2 = C 6 H 2 Br 3 NH 2 + 3HBr

Получение
1 Реакция Николая Николаевича Зинина – это метод получения ароматических аминов ( и анилина ) восстановление нитросоединений.
А) Сначала
C 6 H 5 NO 2 + 3(NH 4 ) 2 S = C 6 H 5 NH 2 + 3S + 6 NH 3 + 2H 2 O
нитробензол
сульфид аммония
анилин
сера аммиак
вода
Б) Позже восстановление нитробензола стали проводить чугунными стружками в присутствии небольшого количества соляной кислоты
4C 6 H 5 NO 2 + 9 Fe + 4 H 2 O = 4 C 6 H 5 NH 2 + 3 Fe 3 O 4
анилин
нитробензол

В) В последние годы и этот способ постепенно вытесняется более перспективным – контактным способом – пропусканием смеси паров нитробензола и водорода над катализатором при температуре 300 °C .
C 6 H 5 NO 2 + 3 H 2 = C 6 H 5 NH 2 + 2H 2 O
t °

« Если бы Зинин не сделал ничего более, кроме превращения нитробензола в анилин, то и тогда его имя осталось бы записанным золотыми буквами в истории химии »
А.Гофман

Применение

- Выполнение на местах теста «Улыбка»


Домашнее задание :
параграф 18, записи в тетради.

Все молодцы!










![Химические свойства 1 Взаимодействие с кислотами С 6 Н 5 N Н 2 + Н CL = [ C 6 H 5 NH 3 ] CL или С 6 Н 5 N Н 2 ⸳ HCL хлорид фениламмония соляно – кислый анилин C 6 H 5 NH 2 HCL + NaOH = C 6 H 5 NH 2 + NaCL + H 2 O 2 Взаимодействие с бромной водой C 6 H 5 NH 2 + 3 Br 2 = C 6 H 2 Br 3 NH 2 + 3HBr](https://static.multiurok.ru/multiurok/html/2022/11/05/s_636693e756e09/img4.jpg)


















